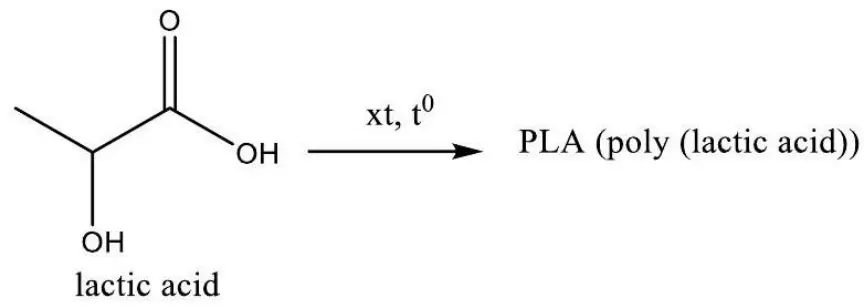
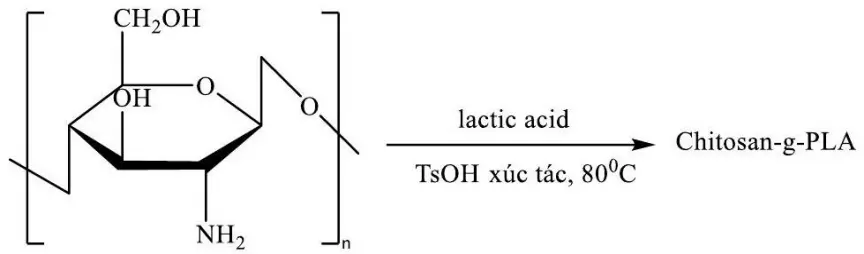
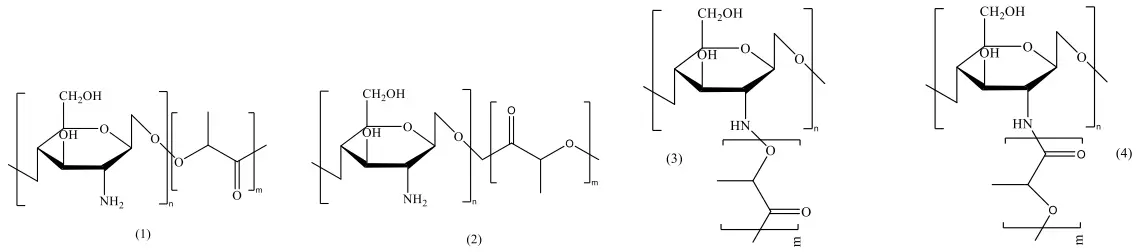
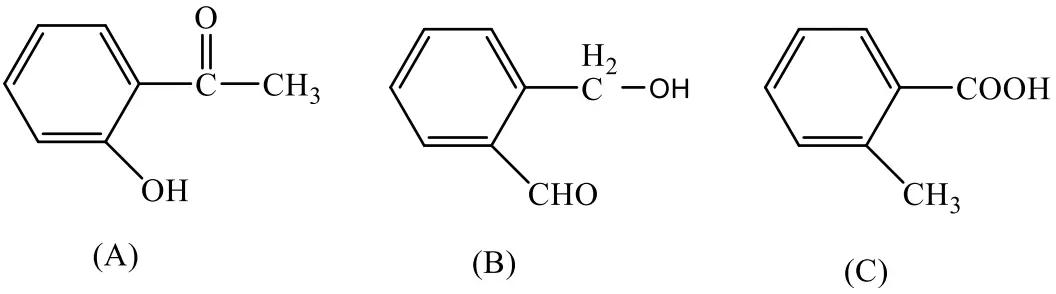
Đề thi thử Tốt nghiệp THPT năm 2026 môn Hóa học Sở GD&DT TP. Hồ Chí Minh - Đề 2
28 câu hỏi 60 phút
Kim loại Fe không phản ứng với dung dịch chất nào sau đây?
\({\rm{CuS}}{{\rm{O}}_4}\)
\({\rm{MgC}}{{\rm{l}}_2}\)
\({\rm{FeC}}{{\rm{l}}_3}\)
\({\rm{AgN}}{{\rm{O}}_3}\)
Kim loại Fe không phản ứng với dung dịch \({\rm{MgC}}{{\rm{l}}_2}\).
Đáp án đúng là B.
Danh sách câu hỏi:
Kim loại Fe không phản ứng với dung dịch \({\rm{MgC}}{{\rm{l}}_2}\).
Đáp án đúng là B.
Triolein có công thức cấu tạo thu gọn là \({{\rm{C}}_3}{{\rm{H}}_5}{\left( {{\rm{OOC}}{{\rm{C}}_{17}}{{\rm{H}}_{33}}} \right)_3}\).
Đáp án đúng là C.
C là phát biểu đúng về nguyên tử \(\;_{20}^{40}{\rm{Ca}}\).
Đáp án đúng là C.
\(\mathrm{Ca}(\mathrm{OH})_2\) rẻ tiền tạo kết tủa với các ion kim loại nặng \(\left(\mathrm{Hg}^{2+}, \mathrm{Pb}^{2+}, \mathrm{Fe}^{3+}\right)\) giúp loại bỏ chúng.
Đáp án đúng là A.
Có 4 phát biểu đúng: (b), (c), (d), (e). Ý (a) sai vì Isoamyl acetate là \(\mathrm{C}_7 \mathrm{H}_{14} \mathrm{O}_2\) nhưng mùi chuối chín.
Đáp án đúng là B.
Câu 19:
Cho giản đồ năng lượng của phản ứng ở \(680{\rm{\;K}}\): \(\mathrm{H}_{2(\mathrm{~g})}+\mathrm{I}_{2(\mathrm{~g})} \rightleftarrows 2 \mathrm{HI}(\mathrm{g})\ \ \ \ \Delta_{\mathrm{r}} \mathrm{H}=-17 \mathrm{~kJ}\)
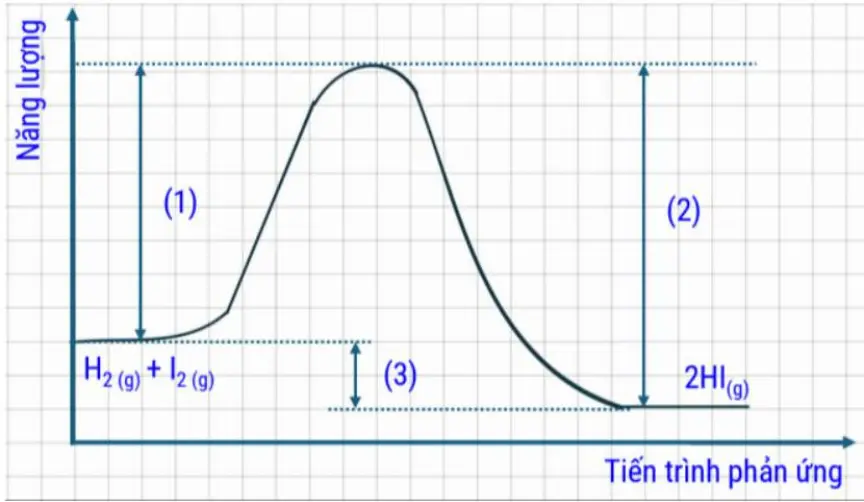
Cho các phát biểu sau:
Các giá trị (1), (2), (3) là năng lượng hoạt hóa của các phản ứng trong cân bằng
Giá trị (1) là năng lượng hoạt hóa của phản ứng thuận và giá trị (2) là năng lượng hoạt hóa của phản ứng nghịch
Giá trị (3) là \( - 17{\rm{\;kJ}}/{\rm{mol}}\)
Cho biết công thức liên hệ năng lượng hoạt hóa ( \({E_a}\) ) và hằng số tốc độ ( \(k\) ) như sau: \({\rm{ln}}k = - \frac{{{E_a}}}{{RT}} + {\rm{ln}}A\) (với A là hằng số) thì trong cân bằng trên, tốc độ phản ứng thuận gấp 20 lần tốc độ phản ứng nghịch nên phản ứng thuận sẽ thuận lợi về mặt năng lượng
Câu 20:
Công nghệ kết tủa struvite hay còn gọi là MAP (magnesium ammonium phosphate hexahydrate) là phương pháp thu hồi phosphorus (dưới dạng ion phosphate, \({\rm{P}}{{\rm{O}}_4}{\;^{3 - }}\) ) trong việc xử lí nước thải. Người ta thu hồi phosphorus bằng cách thêm \({\rm{MgS}}{{\rm{O}}_4}\) và \({\rm{N}}{{\rm{H}}_3}\) vào mẫu nước thải, khuấy kỹ và để lắng thì thu được kết tủa có CTTQ như sau: \({\rm{Mg}}{\left( {{\rm{N}}{{\rm{H}}_4}} \right)_{\rm{x}}}{\left( {{\rm{P}}{{\rm{O}}_4}} \right)_{\rm{y}}} \cdot 6{{\rm{H}}_2}{\rm{O}}\) (gọi là MAP). Cho các phát biểu sau:
Khi xác định thành phần phần trăm nguyên tố theo khối lượng thì có các giá trị sau:

Các giá trị x , y lần lượt là 1 và 2
MAP có thể được xem là một dạng phức chất
Cho lượng dư \({\rm{MgS}}{{\rm{O}}_4}\) và \({\rm{N}}{{\rm{H}}_3}\) vào 100 mL dung dịch chứa muối phosphate, thu được \(10,496\ {\rm{mg}}\) kết tủa MAP . Giả thiết toàn bộ ion \({\rm{P}}{{\rm{O}}_4}{\;^{3 - }}\) trong dung dịch đều được thu hồi trong kết tủa MAP . Hàm lượng phosphorus (\({\rm{mg}}/{\rm{L}}\)) trong dung dịch là \(6,64\ {\rm{mg}}/{\rm{L}}\)
Khi đun nóng, một mẫu MAP sẽ thay đổi khối lượng do mất dần các thành phần dễ bay hơi và được biểu diễn bằng đồ thị sau:
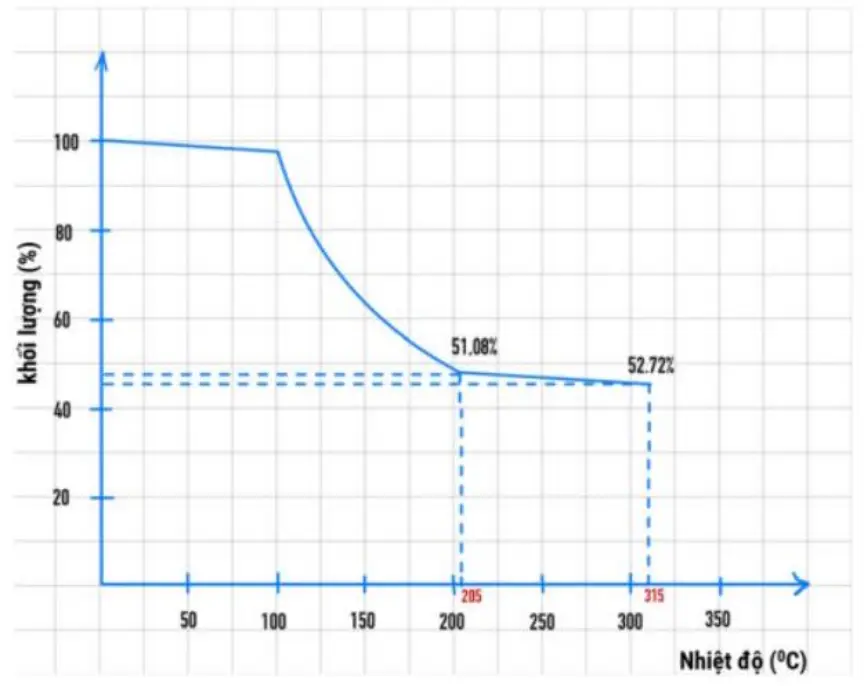
Chất rắn còn lại ở \({205^ \circ }{\rm{C}}\) là một hợp chất A; ở \({315^ \circ }{\rm{C}}\) là hỗn hợp gồm A và một hợp chất B (tỷ lệ khối lượng của A và B là \(1,256:1\)). Công thức của A là \({\rm{MgHP}}{{\rm{O}}_4}\) và của B là \({\rm{M}}{{\rm{g}}_2}{\rm{P}}{{\rm{O}}_7}\)
Câu 21:
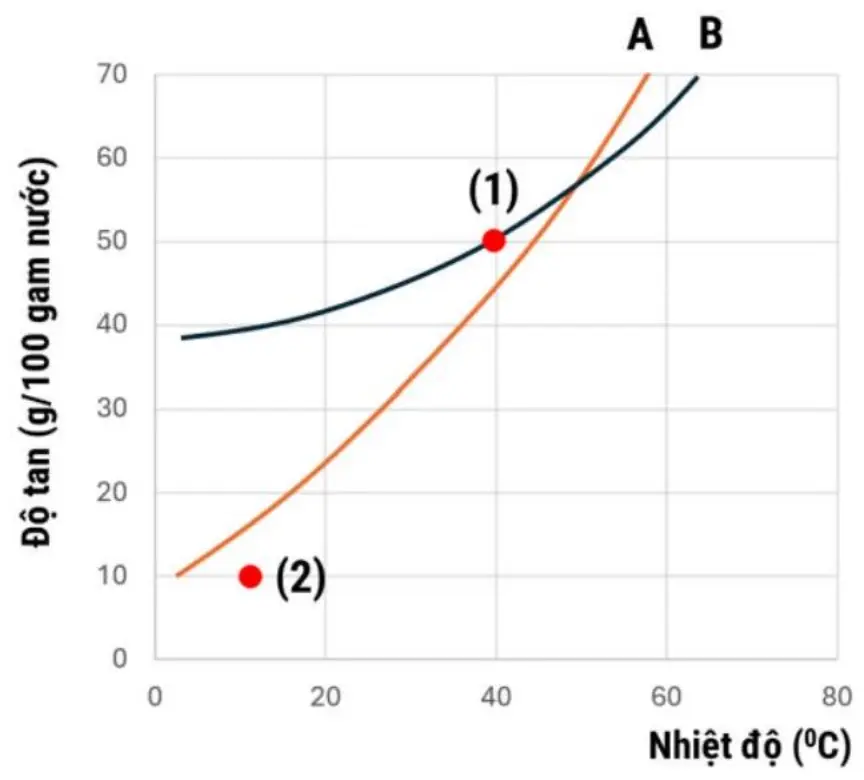
Hàm lượng \({\rm{C}}{{\rm{O}}_2}\) trong không khí có ảnh hưởng lớn đến pH của nước biển. Cho các cân bằng sau:
(1) \(\mathrm{CO}_{2(\mathrm{~g})} \rightleftarrows \mathrm{CO}_{2(\mathrm{dd})}\), \(\mathrm{K}_1=\frac{5}{151}\)
(2) \(\mathrm{CO}_{2(\mathrm{dd})}+\mathrm{H}_2 \mathrm{O} \rightleftarrows \mathrm{HCO}_3^{-}+\mathrm{H}^{+}, \mathrm{K}_2=7,31.10^{-10}\)
Vào năm 2019, hàm lượng \({\rm{C}}{{\rm{O}}_2}\) trung bình trong khí quyển là \(0,0385{\rm{\% }}\) về thể tích (coi áp suất khí quyển là 1 atm).
Cho công thức tính \(\mathrm{K}_1, \mathrm{~K}_2\) như sau: \(\left\{\begin{array}{l}\mathrm{K}_1=\frac{\left[\mathrm{CO}_{2(\mathrm{dd})}\right]}{\mathrm{p}_{\mathrm{CO}_2}} \\ \mathrm{~K}_2=\frac{\left[\mathrm{H}^{+}\right] .\left[\mathrm{HCO}_3^{-}\right]}{\left[\mathrm{CO}_{2(\mathrm{dd})}\right]}\end{array}\right.\)
Với \({{\rm{p}}_{{\rm{C}}{{\rm{O}}_2}}}\) là áp suất riêng của \({\rm{C}}{{\rm{O}}_2}\) và \({{\rm{p}}_{{\rm{C}}{{\rm{O}}_2}}} = {{\rm{p}}_{{\rm{kk}}}}.{\rm{\% \;}}{{\rm{V}}_{{\rm{C}}{{\rm{O}}_2}{\rm{\;trongkk\;}}}}\) ( \({{\rm{p}}_{{\rm{kk}}}}\) là áp suất không khí có giá trị là 1 atm).
Cho các phát biểu sau:
Sự gia tăng nồng độ \({\rm{C}}{{\rm{O}}_2}\) hòa tan sẽ làm tăng nồng độ ion \({{\rm{H}}^ + }\)trong nước biển
Áp suất riêng của \({\rm{C}}{{\rm{O}}_2}\) ở năm 2019 là \(3,85 \cdot {10^{ - 3}}{\rm{\;atm}}\)
Trong môi trường nước biển, nếu nồng độ \({\rm{C}}{{\rm{O}}_2}\) hòa tan tiếp tục tăng do phát thải khí nhà kính, cân bằng giữa \({\rm{C}}{{\rm{O}}_2}\) và \({\rm{HC}}{{\rm{O}}_3}{\;^ - }\)sẽ chuyển dịch theo chiều thuận, làm tăng nồng độ \({{\rm{H}}^ + }\)và góp phần vào hiện tượng acid hóa đại dương
Vào năm 2019 thì pH của nước biển đo được là 8,26. (cho phép làm tròn đáp án đến hàng phần trăm)
Câu 22:
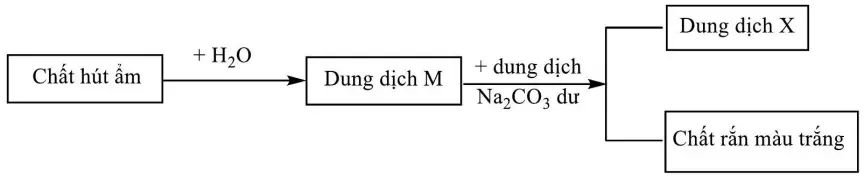
Hợp chất E là muối ngậm nước của một carboxylic acid A (mạch hở) có dạng: \({({\rm{RCOO}})_2}{\rm{Cu}} \cdot {\rm{xH}}2{\rm{O}}\). Kết quả phân tích nhiệt (nung nóng trong môi trường chân không) của hợp chất E như sau:
- Ở nhiệt độ \({150^ \circ }{\rm{C}}\) hợp chất E mất nước hoàn toàn thu được một chất rắn là muối khan X . Khối lượng chất rắn thu được giảm \({\rm{a\% }}\) so với khối lượng E ban đầu.
- Ở nhiệt độ \({250^ \circ }{\rm{C}}\) muối khan X phân huỷ theo phương trình sau (đúng tỉ lệ mol): \(\mathrm{X} \xrightarrow{\mathrm{t}^0} \mathrm{Y}+\mathrm{Z}+\mathrm{T}\).
Cho biết: Y là oxide kim loại, T là chất khí làm đục nước vôi trong và Z là hợp chất hữu cơ đơn chức. Khi cho Z vào dung dịch iodine trong dung dịch NaOH , thu được kết tủa màu vàng và dung dịch chứa muối sodium của carboxylic acid A . Biết rằng khối lượng phân tử của E bằng \(200{\rm{\;g}}/{\rm{mol}}\).
Cho các phát biểu sau:
\(Z\) có tên thông thường là acetone
Công thức cấu tạo của muối khan X là \(\left( {{\rm{HCOO}}} \right)_2{\rm{Cu}}\)
Số phân tử nước trong tinh thể \(E\) là 2
Giá trị của a là \(9{\rm{\% }}\)