Đề thi thử Tốt nghiệp THPT năm 2026 môn Hóa học Sở GD&DT Hà Nội - Đề 1
28 câu hỏi 60 phút
Trong sản xuất xà phòng thủ công, người ta đun chất béo với dung dịch NaOH. Quá trình này là
Ester hóa
Trung hòa
Xà phòng hóa
Trùng ngưng
Trong sản xuất xà phòng thủ công, người ta đun chất béo với dung dịch NaOH. Quá trình này là xà phòng hóa.
Đáp án đúng là C.
Danh sách câu hỏi:
Trong sản xuất xà phòng thủ công, người ta đun chất béo với dung dịch NaOH. Quá trình này là xà phòng hóa.
Đáp án đúng là C.
Ethyl acetate sẽ tham gia phản ứng thủy phân khi được đun nóng với dung dịch \({{\rm{H}}_2}{\rm{S}}{{\rm{O}}_4}\) loãng.
Đáp án đúng là C.
Một học sinh dùng giấm ăn \(({\rm{C}}{{\rm{H}}_3}{\rm{COOH}}\) loãng) để tẩy vết gỉ trên đinh sắt. Hiện tượng xảy ra là bọt khí bay lên, gỉ sắt tan dần.
Đáp án đúng là A.
Trong dung dịch có pH thấp, nhóm \( - {\rm{N}}{{\rm{H}}_2}\) trong amine có xu hướng nhận proton \(\left( {{{\rm{H}}^ + }} \right)\).
Đáp án đúng là B.
Giải pháp nào sau đây được đánh giá là hiệu quả và bền vững nhất để xử lý tình trạng này là dùng hệ thống trao đổi ion để loại bỏ ion \({\rm{C}}{{\rm{a}}^{2 + }},{\rm{M}}{{\rm{g}}^{2 + }}\) trước khi sử dụng.
Đáp án đúng là B.
Câu 19:
Xét quá trình điện phân dung dịch NaCl bão hòa, có màng ngăn, với điện cực trơ theo sơ đồ sau:
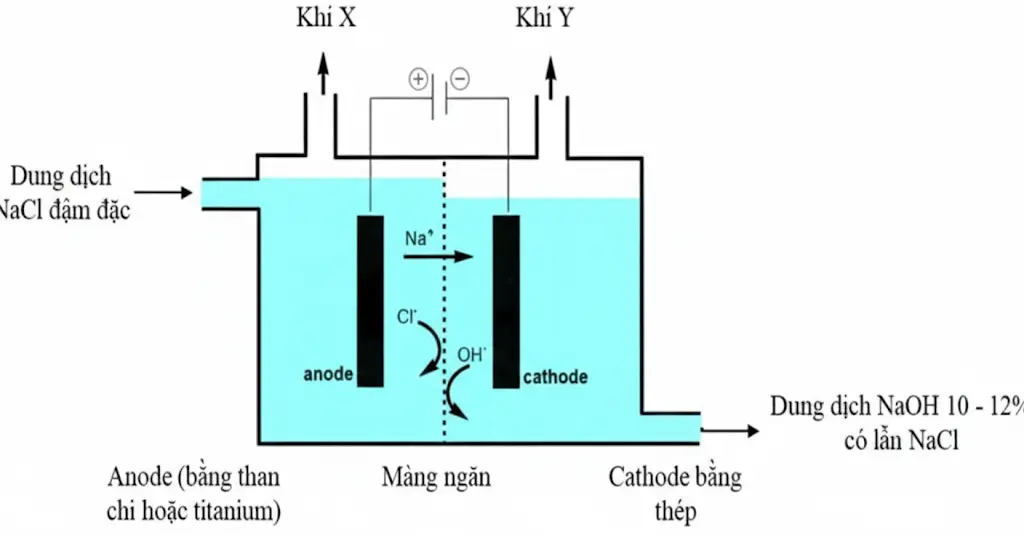
Cho các phát biểu sau:
Trong sơ đồ, tại cathode (cực âm) xảy ra quá trình khử \({{\rm{H}}_2}{\rm{O}}\) tạo khí \({{\rm{H}}_2}\) và ion \({\rm{O}}{{\rm{H}}^ - }\), làm dung dịch xung quanh có pH tăng lên
Sản phẩm thu được ở cathode trong sơ đồ là kim loại Na
Trong sơ đồ điện phân dung dịch NaCl với điện cực trơ, cực thu electron từ nguồn điện được gọi là cathode, nơi xảy ra phản ứng khử
Tiến hành điện phân 1 lít dung dịch NaCl bão hòa bằng dòng điện một chiều không đổi cường độ 5 A trong 1 giờ, sử dụng điện cực trơ và có màng ngăn, hiệu suất điện phân là \(80{\rm{\% }}\). Biết rằng sau quá trình điện phân, khí clorine sinh ra ở anode được dẫn vào chính dung dịch kiềm NaOH ở ngăn cathode để tạo thành nước Gia-ven (có chứa hỗn hợp NaCl và NaClO ), trong đó khối lượng NaClO thu được sau quá trình điện phân là \(5,56\ {\rm{gam}}\). (Cho: \({\rm{F}} = 96500\ {\rm{C}}/{\rm{mol}}\), (làm tròn kết quả đến hàng trăm)
Câu 20:
Một hợp chất E được điều chế từ phản ứng giữa một alcohol no đơn chức mạch hở X và một acid carboxylic Y. Trong đó, Y là một acid dị vòng thơm có nhân pyridine (vòng thơm 6 cạnh chứa 1 nguyên tử N thay cho nguyên tử C trong benzene), đồng thời mang nhóm -COOH liên kết trực tiếp với vòng. Hợp chất E được sử dụng trong một số chế phẩm xoa bóp, giảm đau, hỗ trợ điều trị các triệu chứng như đau cơ, mỏi lưng, bong gân, ...
Thành phần phần trăm khối lượng các nguyên tố trong E như sau: \(63,58{\rm{\% C}};5,96{\rm{\% H}};9,27{\rm{\% \;N}};21,19{\rm{\% O}}\). Kết quả phổ hồng ngoại (IR) của E ghi nhận:
- Một peak đặc trưng cho liên kết \({\rm{C}} = {\rm{O}}\) (ester) ở vùng số sóng \(1740{\rm{\;c}}{{\rm{m}}^{ - 1}}\).
- Peak liên quan đến dao động \({\rm{C}} - {\rm{N}}\) ở vùng số sóng khoảng \(1350{\rm{\;c}}{{\rm{m}}^{ - 1}}\).
- Peak dao động \({\rm{C}} - {\rm{H}}\) thơm ở vùng khoảng \(3100{\rm{\;c}}{{\rm{m}}^{ - 1}}\).
Phổ khối lượng (MS) cho thấy phân tử khối của E là 151 amu.
Cho các phát biểu sau:
Sự xuất hiện peak ở vùng số sóng \( \sim 1740{\rm{\;c}}{{\rm{m}}^{ - 1}}\) trong phổ IR cho thấy E có nhóm chức ester
Công thức phân tử của E là \({{\rm{C}}_8}{{\rm{H}}_9}{\rm{N}}{{\rm{O}}_2}\)
Trong phân tử E có chứa nhóm chức -OH
Ester E không có khả năng làm mất màu dung dịch bromine
Câu 21:
Cho các phản ứng tạo phức chất sau đây:
\(\mathrm{Cu}^{2+}(\mathrm{aq})+4 \mathrm{NH}_3(\mathrm{aq}) \rightarrow\left[\mathrm{Cu}\left(\mathrm{NH}_3\right)_4\right]^{2+}(\mathrm{aq})\ (I) \)
\({\left[\mathrm{Cu}\left(\mathrm{NH}_3\right)_4\right]^{2+}(\mathrm{aq})+\mathrm{Cl}^{-}(\mathrm{aq}) \rightarrow\left[\mathrm{Cu}\left(\mathrm{NH}_3\right)_3 \mathrm{Cl}\right]^{+}(\mathrm{aq})+\mathrm{NH}_3(\mathrm{g})} \ (II)\)
\({\left[\mathrm{Cu}\left(\mathrm{NH}_3\right)_4\right]^{2+}(\mathrm{aq})+\mathrm{H}_2 \mathrm{O}(\mathrm{l}) \rightleftharpoons \mathrm{Cu}(\mathrm{OH})_2(\mathrm{~s})+\mathrm{NH}_4^{+}(\mathrm{aq})+\mathrm{NH}_3(\mathrm{g})}\ (III)\)
Biết rằng dung dịch \({\rm{C}}{{\rm{u}}^{2 + }}\) có màu xanh lam, phức \({\left[ {{\rm{Cu}}{{\left( {{\rm{N}}{{\rm{H}}_3}} \right)}_4}} \right]^{2 + }}\) có màu xanh tím, phức \({\left[ {{\rm{Cu}}{{\left( {{\rm{N}}{{\rm{H}}_3}} \right)}_3}{\rm{Cl}}} \right]^ + }\)có màu xanh nhạt, \({\rm{Cu}}{({\rm{OH}})_2}\) là kết tủa màu xanh.
Cho các phát biểu sau:
Khi cho dung dịch \({\rm{N}}{{\rm{H}}_3}\) vào dung dịch \({\rm{C}}{{\rm{u}}^{2 + }}\), màu dung dịch chuyển từ xanh lam sang xanh tím là do sự tạo thành phức chất \({\left[ {{\rm{Cu}}{{\left( {{\rm{N}}{{\rm{H}}_3}} \right)}_4}} \right]^{2 + }}\) tan trong nước
Phức chất \({\left[ {{\rm{Cu}}{{\left( {{\rm{N}}{{\rm{H}}_3}} \right)}_4}} \right]^{2 + }}\) bền trong môi trường có dư \({\rm{N}}{{\rm{H}}_3}\). Khi thêm từ từ HCl loãng, ion \({{\rm{H}}^ + }\)phản ứng với \({\rm{N}}{{\rm{H}}_3}\) tạo thành \({\rm{N}}{{\rm{H}}_4}{\;^ + }\), làm giảm nồng độ \({\rm{N}}{{\rm{H}}_3}\) tự do, cân bằng bị dịch chuyển ngược và phức bị phân hủy
Khi thêm NaCl vào dung dịch \({\left[ {{\rm{Cu}}{{\left( {{\rm{N}}{{\rm{H}}_3}} \right)}_4}} \right]^{2 + }},{\rm{C}}{{\rm{l}}^ - }\)có thể thay thế \({\rm{N}}{{\rm{H}}_3}\) trong phức, tạo \({\rm{ra}}{\left[ {{\rm{CuC}}{{\rm{l}}_4}} \right]^{2 - }}\) có màu vàng đặc trưng
Khi cho 100 mL dung dịch \({\rm{CuS}}{{\rm{O}}_4}\ 0,1\ {\rm{M}}\) tác dụng hoàn toàn với dung dịch \({\rm{N}}{{\rm{H}}_3}\) dư, sẽ tạo ra \(0,01{\rm{\;mol}}\) phức \({\left[ {{\rm{Cu}}{{\left( {{\rm{N}}{{\rm{H}}_3}} \right)}_4}} \right]^{2 + }}\). Để tạo được lượng phức này, cần tối thiểu \(0,4{\rm{\;mol}}\ {{\rm{NH}}_3}\), tương đương 400 mL dung dịch \({\rm{N}}{{\rm{H}}_3}\ 1\ {\rm{M}}\)