Câu hỏi:
Xét quá trình điện phân dung dịch NaCl bão hòa, có màng ngăn, với điện cực trơ theo sơ đồ sau:
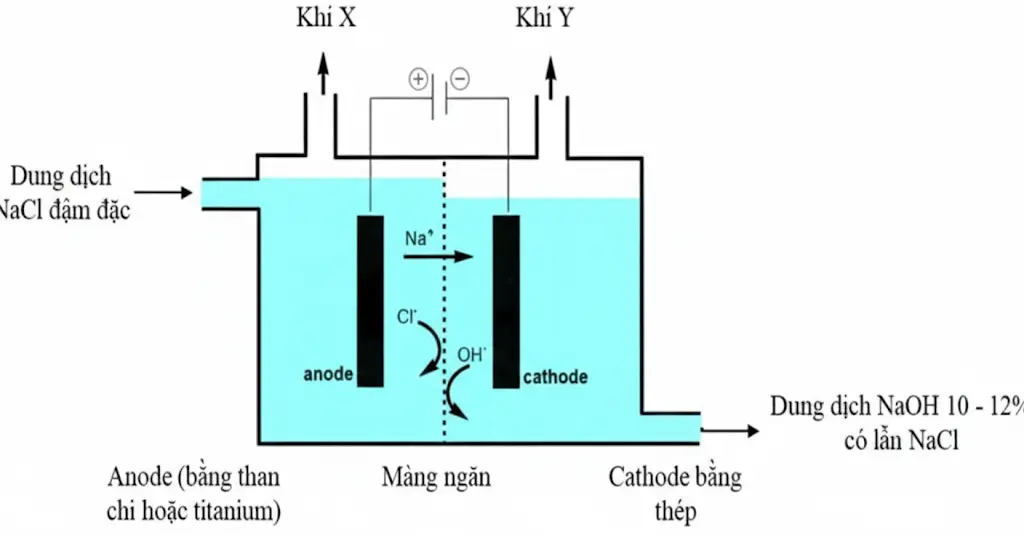
Cho các phát biểu sau:
Trong sơ đồ, tại cathode (cực âm) xảy ra quá trình khử \({{\rm{H}}_2}{\rm{O}}\) tạo khí \({{\rm{H}}_2}\) và ion \({\rm{O}}{{\rm{H}}^ - }\), làm dung dịch xung quanh có pH tăng lên.
Sản phẩm thu được ở cathode trong sơ đồ là kim loại Na.
Trong sơ đồ điện phân dung dịch NaCl với điện cực trơ, cực thu electron từ nguồn điện được gọi là cathode, nơi xảy ra phản ứng khử.
Tiến hành điện phân 1 lít dung dịch NaCl bão hòa bằng dòng điện một chiều không đổi cường độ 5 A trong 1 giờ, sử dụng điện cực trơ và có màng ngăn, hiệu suất điện phân là \(80{\rm{\% }}\). Biết rằng sau quá trình điện phân, khí clorine sinh ra ở anode được dẫn vào chính dung dịch kiềm NaOH ở ngăn cathode để tạo thành nước Gia-ven (có chứa hỗn hợp NaCl và NaClO ), trong đó khối lượng NaClO thu được sau quá trình điện phân là \(5,56\ {\rm{gam}}\). (Cho: \({\rm{F}} = 96500\ {\rm{C}}/{\rm{mol}}\), (làm tròn kết quả đến hàng trăm)
Đáp án đúng: Đúng, Sai, Đúng, Đúng
a. Trong sơ đồ, tại cathode (cực âm) xảy ra quá trình khử \({{\rm{H}}_2}{\rm{O}}\) tạo khí \({{\rm{H}}_2}\) và ion \({\rm{O}}{{\rm{H}}^ - }\), làm dung dịch xung quanh có pH tăng lên.
Đáp án đúng là Đúng.
b. Vì \(\mathrm{H}_2 \mathrm{O}\) dễ bị khử hơn do thế khử của \(\mathrm{H}_2 \mathrm{O}\) (-0,83 V) lớn hơn thế khử của \(\mathrm{Na}^{+}\) (-2,71 V) nên \(\mathrm{H}_2\) bị khử trước.
Đáp án đúng là Sai.
c. Trong sơ đồ điện phân dung dịch NaCl với điện cực trơ, cực thu electron từ nguồn điện được gọi là cathode, nơi xảy ra phản ứng khử.
Đáp án đúng là Đúng.
d. Vì \(\mathrm{n}_{\mathrm{e}}= \frac{\text { I.t }}{\mathrm{F}}=\frac{5.1 .3600}{96500} \approx 0,1865\ (\mathrm{mol})\).
Do H = 80% nên \(\mathrm{n}_{\mathrm{e} \text { thực tế }}=0,1865.0,8=0,1492\ (\mathrm{mol})\).
\(\mathrm{n}_{\mathrm{Cl}_2}=\frac{1}{2} \mathrm{n}_{\mathrm{e}}=0,0746\ (\mathrm{mol})\).
\(\mathrm{Cl}_2+2 \mathrm{NaOH} \rightarrow \mathrm{NaCl}+\mathrm{NaClO}+\mathrm{H}_2 \mathrm{O}\).
Theo phương trình phản ứng: \(\mathrm{n}_{\mathrm{Cl}_2}=\mathrm{n}_{\mathrm{NaOH}}=0,0746\ (\mathrm{mol})\).
\(\mathrm{m}_{\mathrm{NaClO}}=0,0746 \cdot 74,5\approx5,56\ (\mathrm{gam})\)
Đáp án đúng là Đúng.
Câu hỏi này thuộc đề thi trắc nghiệm dưới đây, bấm vào Bắt đầu thi để làm toàn bài
Tuyển Tập Đề Thi Tham Khảo Tốt Nghiệp THPT Năm 2026 – Hoá Học – Bộ Đề 02Tài liệu tổng hợp các đề thi tham khảo bám sát cấu trúc đề thi tốt nghiệp THPT năm 2026.Nội dung bao quát kiến thức Hoá học lớp 12, có phân hoá rõ ràng theo mức độ.Hệ thống câu hỏi giúp học sinh rèn luyện kỹ năng tư duy và làm bài trắc nghiệm.Phù hợp cho ôn tập, củng cố kiến thức và đánh giá năng lực trước kỳ thi.Là nguồn tài liệu hữu ích cho học sinh và giáo viên trong quá trình dạy – học.
Câu hỏi liên quan

Bộ 50 Đề Thi Thử Tốt Nghiệp THPT Giáo Dục Kinh Tế Và Pháp Luật Năm 2026 – Theo Cấu Trúc Đề Minh Họa Bộ GD&ĐT

Bộ 50 Đề Thi Thử Tốt Nghiệp THPT Lịch Sử Học Năm 2026 – Theo Cấu Trúc Đề Minh Họa Bộ GD&ĐT

Bộ 50 Đề Thi Thử Tốt Nghiệp THPT Công Nghệ Năm 2026 – Theo Cấu Trúc Đề Minh Họa Bộ GD&ĐT

Bộ 50 Đề Thi Thử Tốt Nghiệp THPT Môn Hóa Học Năm 2026 – Theo Cấu Trúc Đề Minh Họa Bộ GD&ĐT

Bộ 50 Đề Thi Thử Tốt Nghiệp THPT Môn Sinh Học Năm 2026 – Theo Cấu Trúc Đề Minh Họa Bộ GD&ĐT