Đề thi thử Tốt nghiệp THPT năm 2026 môn Hóa học Sở GD&ĐT Thừa Thiên Huế - Đề 1
28 câu hỏi 60 phút
Bản chất chung của ăn mòn hóa học và ăn mòn điện hóa là
Cả hai quá trình đều kèm theo sự phát sinh dòng điện
Electron của kim loại được chuyển trực tiếp vào môi trường
Nhiệt độ càng cao thì tốc độ ăn mòn càng giảm
Cả hai đều là quá trình oxi hóa - khử
Cả hai đều là quá trình oxi hóa - khử.
Đáp án đúng là D.
Danh sách câu hỏi:
Cả hai đều là quá trình oxi hóa - khử.
Đáp án đúng là D.
Tên của hợp chất này là sodium hydrogen carbonate.
Đáp án đúng là A.
Nguyên tử có 3 lớp electron → Lớp thứ 3 là lớp ngoài cùng.
Lớp ngoài cùng có 4 electron → Cấu hình lớp ngoài cùng là \(3 s^2 3 p^2\).
Viết đầy đủ từ trong ra ngoài: \(1 s^2 2 s^2 2 p^6 3 s^2 3 p^2\).
Đáp án đúng là B.
- Các tính chất vật lý chung của kim loại bao gồm: tính dẻo, tính dẫn điện, tính dẫn nhiệt và ánh kim. Cả 4 tính chất này đều do các electron tự do trong mạng tinh thể kim loại gây ra.
- Tính cứng, khối lượng riêng, hay nhiệt độ nóng chảy phụ thuộc chủ yếu vào mật độ điện tích, bán kính nguyên tử và kiểu mạng tinh thể.
Đáp án đúng là D.
PVC được trùng hợp từ monomer vinyl chloride có công thức là \(\mathrm{CH}_2=\mathrm{CHCl}\).
Khi trùng hợp, liên kết đôi đứt ra để tạo mạch dài: \(-\left(\mathrm{CH}_2-\mathrm{CHCl}\right)_n-{ }\).
Đáp án đúng là A.
Câu 10:
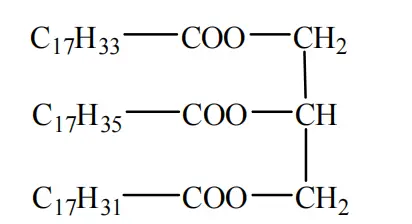
Hợp chất nào sau đây là ester?
Câu 12:
Phát biểu nào sau đây sai?
Câu 16:
Phát biểu nào sau đây sai?
Câu 19:
Cho khí \({\rm{N}}{{\rm{O}}_2}\) vào bình kín, cân bằng hoá học sau xảy ra: \(2 \mathrm{NO}_{2(\mathrm{~g}) \text { (nâu đỏ) }} \rightleftarrows \mathrm{N}_2 \mathrm{O}_{4(\mathrm{~g}) \text { (không màu) }} \triangle_{\mathrm{r}} \mathrm{H}_{298}^0=-57 \mathrm{~kJ}\).
Đồ thị biểu diễn nồng độ \({\rm{N}}{{\rm{O}}_2}\) và \({{\rm{N}}_2}{{\rm{O}}_4}\) theo thời gian như sau:
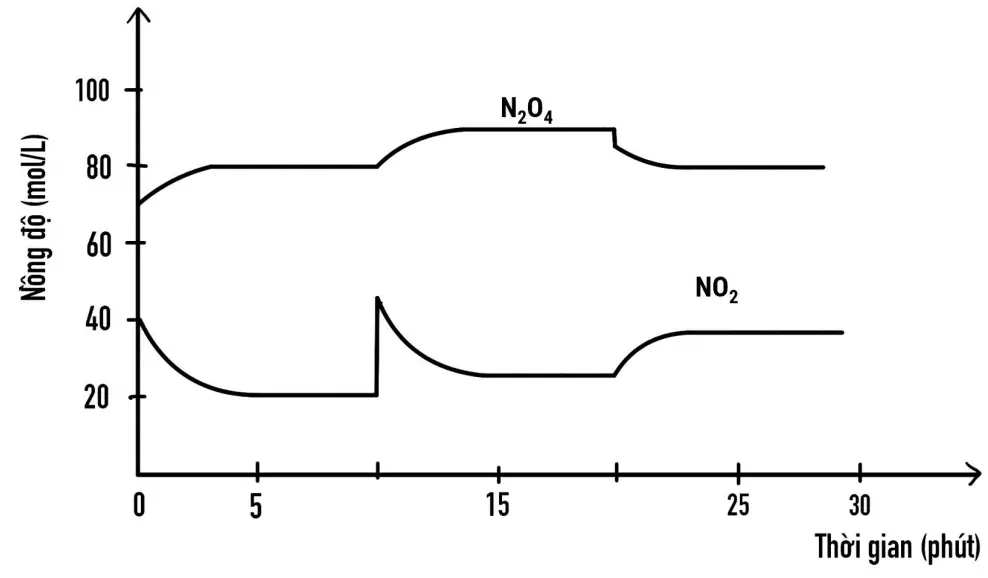
Tại thời điểm 5 phút, tốc độ phản ứng thuận bằng tốc độ phản ứng nghịch
Thời điểm 10 phút, người ta tác động yếu tố làm giảm nồng độ \({\rm{N}}{{\rm{O}}_2}\)
Thời điểm 10 phút đến 20 phút, cân bằng chuyển dịch sang chiều thuận
Từ 20 phút người ta tác động yếu tố làm tăng nhiệt độ
Câu 20:
Cho CTCT của amine sau:
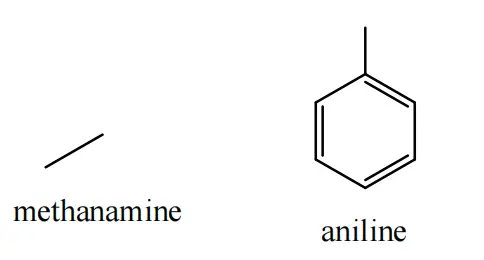
Cho các phát biểu sau:
Phân tử khối của methylamine nhỏ hơn nên tính base lớn hơn
Tính base của methylamine mạnh hơn aniline
Nhóm \( - {\rm{N}}{{\rm{H}}_2}\) có hiệu ứng đẩy electron, làm tăng mật độ electron trên vòng benzene, đặc biệt ở các vị trí ortho và para. Điều này làm cho aniline dễ dàng tham gia phản ứng thế với \({\rm{B}}{{\rm{r}}_2}\) hơn benzene
Aniline được điều chế bằng cách cho nitrobenzene phản ứng với hydrogen theo phản ứng:
\(\mathrm{C}_6 \mathrm{H}_5 \mathrm{NO}_2+2 \mathrm{H}_2 \longrightarrow \mathrm{C}_6 \mathrm{H}_5 \mathrm{NH}_2+2 \mathrm{H}_2 \mathrm{O}\).
Cho biết trong sản phẩm đi ra khỏi thiết bị phản ứng có thành phần phần trăm về khối lượng như sau:16,1% \({{\rm{C}}_6}{{\rm{H}}_5}{\rm{N}}{{\rm{O}}_2};\ 18,6{\rm{\% }}\ {{\rm{C}}_6}{{\rm{H}}_5}{\rm{N}}{{\rm{H}}_2}\) với lượng còn lại là các sản phẩm vô cơ khác. Hiệu suất của phản ứng điều chế là \(65,5{\rm{\% }}\). (Cho biết hiệu suất tính theo nitrogenbenzene và cho phép làm tròn đáp án đến hàng phần mười)
Câu 21:
Menthol là hợp chất hữu cơ được tìm thấy trong cây bạc hà. Nó được sử dụng làm hương liệu trong nhiều chất như: kem đánh răng, kẹo cao su và xi-rô ho, ...
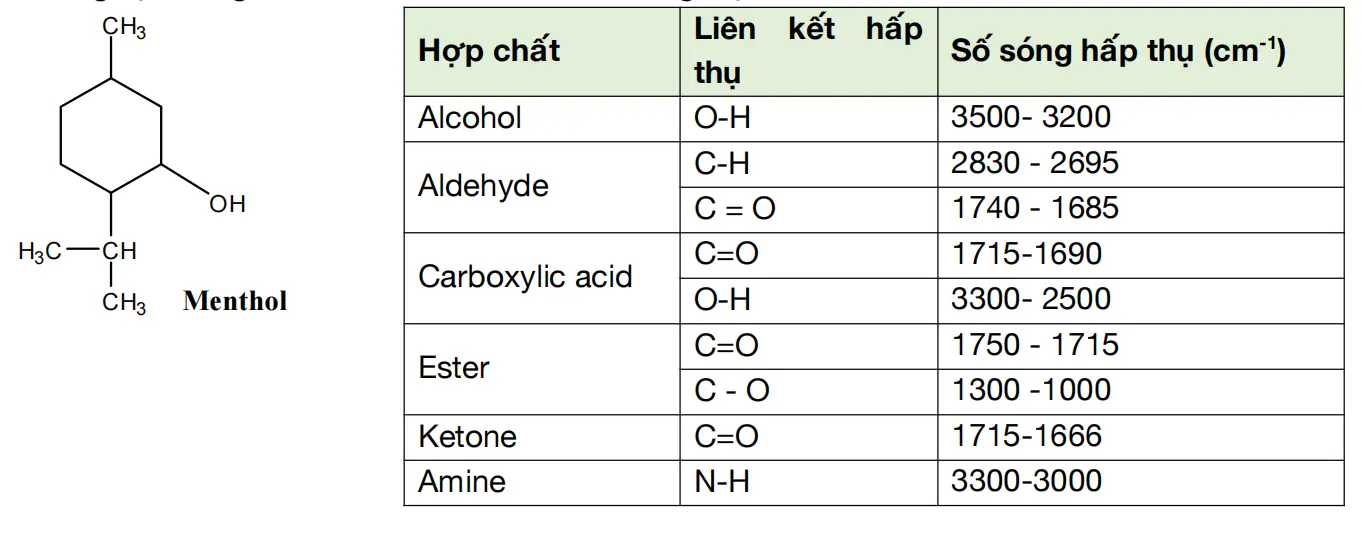
Cho các phát biểu sau
Menthol thuộc loại hợp chất hydrocarbon
Công thức phân tử của menthol là \({{\rm{C}}_{10}}{{\rm{H}}_{20}}{\rm{O}}\)
Trên phổ IR của menthol có tín hiệu đặc trưng cho nhóm alcohol ở vùng \(2250 - 2150{\rm{\;c}}{{\rm{m}}^{ - 1}}\)
Khi tách nước menthol (đun với \({{\rm{H}}_2}{\rm{S}}{{\rm{O}}_4}\) đặc ở nhiệt độ thích hợp), có thể thu được hydroccabon có công thức:
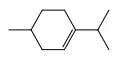
Câu 22:
Muối Mohr có công thức \({\left( {{\rm{N}}{{\rm{H}}_4}} \right)_2}{\rm{Fe}}{\left( {{\rm{S}}{{\rm{O}}_4}} \right)_2} \cdot 6{{\rm{H}}_2}{\rm{O}}\). Để xác định độ tinh khiết của một loại muối Mohr(cho rằng trong muối Mohr chỉ có muối kép ngậm nước nêu trên và tạp chất trơ), một học sinh tiến hành các thí nghiệm sau: Cân chính xác 7,237 gam muối Mohr, pha thành 100 mL dung dịch X. Lấy chính xác 10 mL dung dịch X, thêm 10 mL dung dịch \({{\rm{H}}_2}{\rm{S}}{{\rm{O}}_4}\ 10{\rm{\% }}\) được dung dịch Y. Chuẩn độ dung dịch Y bằng dung dịch chuẩn \({\rm{KMn}}{{\rm{O}}_4}\ 0,023\ {\rm{M}}\). Thực hiện chuẩn độ 3 lần.
Kết quả đạt được như sau:

Cho các phát biểu sau:
Dung dịch \({{\rm{H}}_2}{\rm{S}}{{\rm{O}}_4}\) được thêm vào dung dịch chuẩn độ để tạo thành môi trường acid, giúp phản ứng xảy ra theo hướng tạo thành \({\rm{M}}{{\rm{n}}^{2 + }}\)
Có thể thay dung dịch \({{\rm{H}}_2}{\rm{S}}{{\rm{O}}_4}\) bằng dung dịch acid mạnh như \({\rm{HCl}},{\rm{HN}}{{\rm{O}}_3}\) nhưng phải đảm bảo lượng \({{\rm{H}}^ + }\) dư sau phản ứng
Trong mỗi lần chuẩn độ, dung dịch \({\rm{KMn}}{{\rm{O}}_4}\) được xem là phản ứng vừa đủ với muối Mohr (điểm dừng) khi giọt dung dịch \({\rm{KMn}}{{\rm{O}}_4}\) cuối cùng nhỏ vào dung dịch Y không mất màu
Theo kết quả chuẩn độ ở trên, độ tinh khiết (% khối lượng \({\left( {{\rm{N}}{{\rm{H}}_4}} \right)_2}{\rm{Fe}}{\left( {{\rm{S}}{{\rm{O}}_4}} \right)_2} \cdot 6{{\rm{H}}_2}{\rm{O}})\) của muối Mohr khoảng 98,45%