Đề thi thử Đánh giá năng lực ĐHQG Hà Nội năm 2025 - Đề 4 - Đề 4
17 câu hỏi 60 phút
Biết rằng mùi tanh của cá (đặc biệt là cá mè) là hỗn hợp các amine và một số chất khác. Để khử mùi tanh của các trước khi nấu chúng ta có thể sử dụng dung dịch chất nào dưới đây?
Dung dịch xút
Nước vôi trong
Giấm ăn
Nước muối
Đáp án đúng là \(C\)
Phương pháp giải
Amine gây mùi tanh của cá nên có thể làm mất mùi tanh khi cho amine tác dụng với acid.
Lời giải
Khi dùng giấm ăn làm sạch cá, acetic acid trong giấm ăn sẽ tác dụng với amine gây mùi khó chịu của cá tạo ra muối, làm mất đi mùi tanh.
Chọn C.
Danh sách câu hỏi:
Đáp án đúng là \(C\)
Phương pháp giải
Amine gây mùi tanh của cá nên có thể làm mất mùi tanh khi cho amine tác dụng với acid.
Lời giải
Khi dùng giấm ăn làm sạch cá, acetic acid trong giấm ăn sẽ tác dụng với amine gây mùi khó chịu của cá tạo ra muối, làm mất đi mùi tanh.
Chọn C.
Phương pháp giải:
- Cân bằng phương trình theo nguyên tắc thăng bằng electron.
- Tính nồng độ của dung dịch \(\mathrm{KMnO}_{4}\) theo đúng hệ số tỉ lượng của mỗi lần chuẩn độ.
- Nồng độ dung dịch \(\mathrm{KMnO}_{4}\) cuối cùng là trung bình cộng của 3 nồng độ \(\mathrm{KMnO}_{4}\) đã tính.
Lời giải:
- Phương trình hóa học đã được cân bằng là:
\(2 \mathrm{KMnO}_{4}+5 \mathrm{H}_{2} \mathrm{C}_{2} \mathrm{O}_{4}+3 \mathrm{H}_{2} \mathrm{SO}_{4} \rightarrow 2 \mathrm{MnSO}_{4}+10 \mathrm{CO}_{2}+8 \mathrm{H}_{2} \mathrm{O}+\mathrm{K}_{2} \mathrm{SO}_{4}\)
- Nồng độ của dung dịch \(\mathrm{KMnO}_{4}\) trong thí nghiệm 1 là:
\(C_{K M n O_{4}(1)}=\frac{C_{H_{2} \mathrm{C}_{2} \mathrm{O}_{4}} . V_{\mathrm{H}_{2} \mathrm{C}_{2} \mathrm{O}_{4}} . 2}{V_{\mathrm{KMnO}_{4}} . 5}=\frac{0,05 . 10 . 2}{5,70.5} \approx 0,035 \mathrm{M}\)
- Tính toán tương tự với thí nghiệm 2 và 3 , ta có:
\(C_{K M n O_{4}(2)}=\frac{C_{H_{2} \mathrm{C}_{2} \mathrm{O}_{4}} . V_{\mathrm{H}_{2} \mathrm{C}_{2} \mathrm{O}_{4}} . 2}{V_{\mathrm{KMnO}_{4}} . 5}=\frac{0,05 . 10 . 2}{5,80 . 5} \approx 0,034 \mathrm{M}\)
\(C_{K M n O_{4}(3)}=\frac{C_{H_{2} \mathrm{C}_{2} \mathrm{O}_{4}} . V_{\mathrm{H}_{2} \mathrm{C}_{2} \mathrm{O}_{4}} . 2}{V_{\mathrm{KMnO}_{4}} . 5}=\frac{0,05 . 10.2}{5,85.5} \approx 0,034 \mathrm{M}\)
Vậy nồng độ của dung dịch \(\mathrm{KMnO}_{4}\) là:
\(\frac{0,034+0,034+0,035}{3} \approx 0,034 M\)
Đáp án đúng là \(\mathbf{A}\)
Phương pháp giải:
Dung dịch acid mà trong dung dịch còn phân tử acid là acid yếu, phân li không hoàn toàn.
Lời giải:
Trong các dung dịch hydrohalic acid, chỉ có HF là acid yếu, trong nước acid này phân li không hoàn toàn:. Vậy trong dung dịch acid này có cả phân tử HF tồn tại trong dung dịch.
Đáp án đúng là \(\mathbf{C}\)
Phương pháp giải:
Các phương pháp tinh chế và tách chiết hợp chất hữu cơ.
Lời giải:
Khi ngâm rượu thuốc người ta đã ứng dựng cơ sở của phương pháp chiết lỏng - rắn. Các hợp chất hữu cơ có trong chất rắn là các vị thuốc ngâm cùng rượu được hòa tan bởi dung môi là rượu.
Đáp án đúng là \(B\).
Phương pháp giải:
Dựa vào công thức cấu tạo của terpinen-4-ol để kiểm chứng các đáp án.
Lời giải:
Nhận định sai là nhận định: "Terpinen-4-ol là một alcohol đơn chức bậc 2 ". Terpinen-4-ol là alcohol đơn chức bậc 3.
 Thể tích \(\mathrm{KMnO}_{4}\) xác định được là (làm tròn đến chữ số thập phân thứ ba)
Thể tích \(\mathrm{KMnO}_{4}\) xác định được là (làm tròn đến chữ số thập phân thứ ba)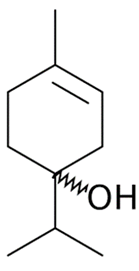 Nhận định nào dưới đây là sai về terpine-4-ol?
Nhận định nào dưới đây là sai về terpine-4-ol?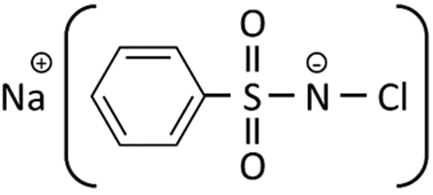
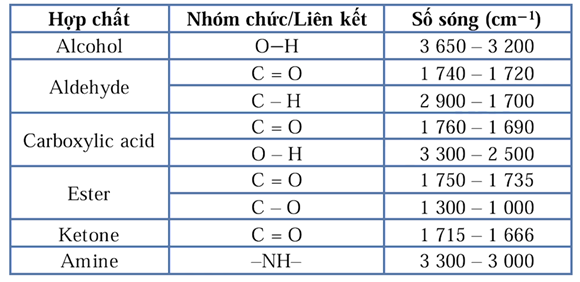
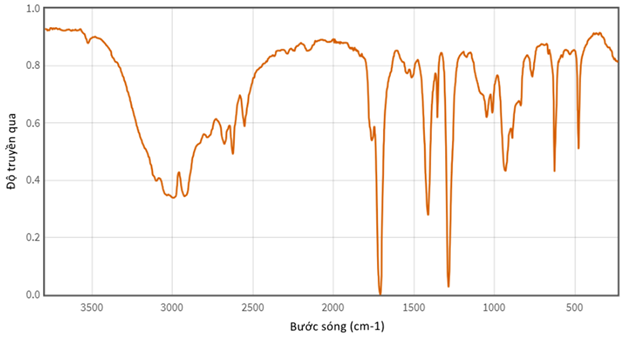 - Thu thập kết quả của phép đo khối lượng của hợp chất X thông qua kết quả phép đo phổ khối lượng (MS):
- Thu thập kết quả của phép đo khối lượng của hợp chất X thông qua kết quả phép đo phổ khối lượng (MS):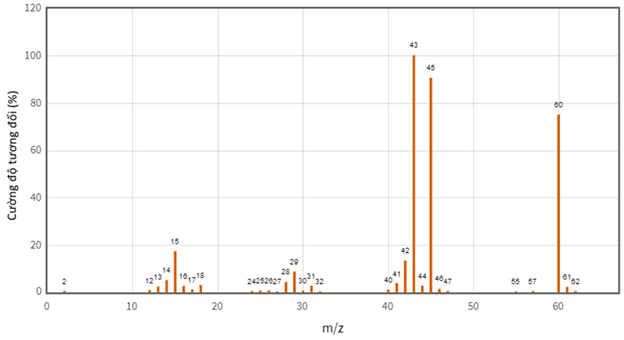 Đốt chất hợp chất hữu cơ X thấy thành phần phần trăm các nguyên tố về khối lượng: \(\% \mathrm{mC}=40 \%\); \(\% \mathrm{mH}=6,67 \%\), còn lại là của nguyên tố oxygen.
Đốt chất hợp chất hữu cơ X thấy thành phần phần trăm các nguyên tố về khối lượng: \(\% \mathrm{mC}=40 \%\); \(\% \mathrm{mH}=6,67 \%\), còn lại là của nguyên tố oxygen.
 Phát biểu nào sau đây không đúng?
Phát biểu nào sau đây không đúng?