Câu hỏi:
Ở điều kiện tiêu chuẩn, 1 lít nước hòa tan tối đa 2,2 lít khí \(\mathrm{Cl}_{2}\). Nồng độ \(\mathrm{mol} / \mathrm{L}\) của nước chlorine bão hòa là
Đáp án đúng: D
Đáp án đúng là D.
Phương pháp giải:
Công thức tính nồng độ \(\mathrm{mol} / \mathrm{L}\) là: \(C_{M}=\frac{n(\mathrm{mol})}{V(L)}\)
Lời giải:
Số mol khí của khí chlorine là: \(n_{C_{2}}=\frac{V_{C l_{2}}}{22,4}=\frac{2,2}{22,4}=0,098 \mathrm{mol}\)
Nồng độ \(\mathrm{mol} / \mathrm{L}\) tối đa của dung dịch nước chlorine bão hòa là: \(C_{M C l_{2}}=\frac{n_{C l_{2}}}{V_{d d}}=\frac{0,098}{1}=0,098 \mathrm{mol} / \mathrm{L}\)
Câu hỏi này thuộc đề thi trắc nghiệm dưới đây, bấm vào Bắt đầu thi để làm toàn bài
Với cấu trúc mới lạ và đa dạng, Đề Thi Tham Khảo Đánh Giá Năng Lực Năm 2025 – ĐHQG Hà Nội – Đề Số 4 giúp thí sinh phát huy tối đa khả năng Giải Quyết Vấn Đề, Sáng Tạo và Tư Duy Định Lượng. Bài thi bao gồm ba phần chính: Toán Học Và Xử Lí Số Liệu, Văn Học - Ngôn Ngữ, Khoa Học/Tiếng Anh. Mỗi phần thi đều được thiết kế với các dạng câu hỏi phong phú, không chỉ đánh giá kiến thức lý thuyết mà còn kiểm tra khả năng phân tích dữ liệu, xử lý thông tin và vận dụng thực tế. Đây là lựa chọn hoàn hảo cho học sinh muốn tự tin chinh phục kỳ thi đánh giá năng lực.
Câu hỏi liên quan
Đáp án đúng là \(C\).
Phương pháp giải:
Tính khối lượng chloramine cần để khử khuẩn cho bể nước có dung tích \(2,5 \mathrm{m}^{3}\) rồi tình số viên chloamine B cần dùng.
Lời giải:
Để khử khuẩn bể nước có dung tích là \(2,5 \mathrm{m}^{3}\) cần khối lượng chloramine là: \(\frac{2,5 . 10^{3}}{1000} . 10=25 \mathrm{gam}\)
Môi viên nén có chứa 250 mg chloramine \(B\) nên số viên chloramine \(B\) cần là: \(\frac{25.10^{3}}{250}=100\) viên.
Đáp án đúng là C.
Phương pháp giải:
- Dựa vào phổ IR để dự đoán liên kết hóa học và suy ra nhóm chức của hợp chất hữu cơ X.
- Dựa vào tỉ lệ phần trăm của các nguyên tố hóa học của hợp chất X để lập công thức đơn giản nhất.
- Dựa vào phổ khối lượng và công thức đơn giản nhất để tìm ra công thức phân tử của hợp chất hữu cơ X.
Từ đó, nhận xét về nhận định ở các đáp án.
Lời giải:
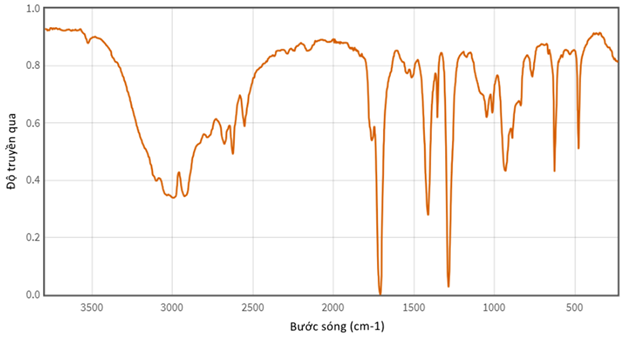
- Dựa vào kết quả phổ \(I R\) của hợp chất hữu cơ \(X\), ta thấy:
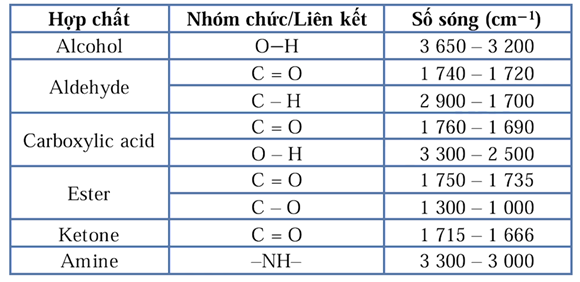
- Có một peak tù, vân rộng, cường độ tín hiệu trung bình ở bước sóng \(2900-3100 \mathrm{cm}^{-1} \Rightarrow\) tín hiệu của liên kết \(\mathrm{O}-\mathrm{H}\) của nhóm carboxyl.
- Có một peak nhọn, vân hẹp, cường độ tín hiệu mạnh ở bước sóng khoảng từ \(1600-1750 \mathrm{cm}^{-1} \Rightarrow\) tín hiệu của liên kết \(\mathrm{C}=\mathrm{O}\) của nhóm carboxyl
Vậy hợp chất hữu cơ X có nhóm - COOH.
- Dựa vào kết quả phổ MS của hợp chất hữu cơ X , ta thấy: Mảnh ion \(\left[\mathrm{M}^{+}\right]\)có giá trị \(\mathrm{m} / \mathrm{z}=60\) là lớn nhất đồng thời cũng có cường độ tương đối lớn nhất nên khối lượng phân tử của X là 60 amu.
- Phân tích kết quả đốt cháy hợp chất hữu cơ X ta có: \(\% \mathrm{mO}=100 \%-40 \%-6,67 \%=53,33 \%\)
- Gọi công thức đơn giản nhất của hợp chất X là \(\mathrm{C}_{\mathrm{x}} \mathrm{H}_{\mathrm{y}} \mathrm{O}_{\mathrm{z}}\), ta có:
\(x: y: z=\frac{\% m C}{12}: \frac{\% m H}{1}: \frac{\% m O}{16}=\frac{40}{12}: \frac{6,67}{1}: \frac{53,33}{15}=3,33: 6,67: 3,56 \approx 1: 2: 1\)
Vậy công thức đơn giản nhất của hợp chất hữu cơ X là \(\left(\mathrm{CH}_{2} \mathrm{O}\right)_{\mathrm{n}}\)
Dựa vào phổ khối lượng ta biết khối lượng phân tử của hợp chất hữu cơ X là 60 amu
\(\Rightarrow\left(\mathrm{CH}_{2} \mathrm{O}\right)_{\mathrm{n}}=60 \Rightarrow \mathrm{n}=2\)
Vậy công thức phân tử của X là \(\mathrm{C}_{2} \mathrm{H}_{4} \mathrm{O}_{2}\) mà \(X\) có nhóm -COOH trong phân tử \(\Rightarrow\) công thức hóa học của \(X\) là \(\mathrm{CH}_{3} \mathrm{COOH}\).
- Đáp án A : Đúng. Chất X là carboxylic acid nên có khả năng tham gia phản ứng ester hóa.
- Đáp án B: Đúng. \(\mathrm{CH}_{3} \mathrm{COOH}\) là acid hữu cơ có tính acid yếu nên khi tan trong nước chỉ phân li một phần ra ion.
- Đáp án C : Sai. Phản ứng xà phòng hóa là phản ứng thủy phân ester trong môi trường kiềm.
- Đáp án D : Đúng. \(\mathrm{CH}_{3} \mathrm{COOH}\) là carboxylic acid no, đơn chức, mạch hở nên có công thức chung là \(\mathrm{C}_{\mathrm{n}} \mathrm{H}_{2 \mathrm{n}} \mathrm{O}_{2}(\mathrm{n} \geq 1)\).
Đáp án đúng là \(\mathbf{C}\).
Phương pháp giải:
Khái niệm và cách viết phương trình nhiệt hóa học.
Lời giải:
- Phương trình hóa học của phản ứng nhiệt phân đá vôi là:
\(\mathrm{CaCO}_{3} \rightarrow \mathrm{CaO}+\mathrm{CO}_{2}\)
- Biến thiên enthalpy của phản ứng nhiệt phân đá vôi là:
Vì phương trình nhiệt hóa học phải có trạng thái của các chất và nhiệt kèm theo của phản ứng nên phương trình nhiệt hóa học của phản ứng nhiệt phân đá vôi là
\(\mathrm{CaCO}_{3}(\mathrm{s}) \rightarrow \mathrm{CaO}(\mathrm{s})+\mathrm{CO}_{2}(\mathrm{g}) \quad \Delta_{\mathrm{r}} \mathrm{H}_{298}^{\circ}=179,2 \mathrm{kJ}\).
Đáp án đúng là \(\mathbf{C}\).
Phương pháp giải:
Các yếu tố làm cân bằng hóa học chuyển dịch.
Lời giải:
Quá trình sản xuất vôi sống sẽ bị giảm hiệu suất nếu cân bằng chuyển dịch theo chiều nghịch.
Đáp án A : Nếu rút bớt khí \(\mathrm{CO}_{2}\) ra khỏi lò phản ứng, nồng độ khí \(\mathrm{CO}_{2}\) của hệ cân bằng sẽ giảm đi, cân bằng chuyển dịch theo chiều làm tăng thêm nồng độ \(\mathrm{CO}_{2} \Rightarrow\) cân bằng chuyển dịch theo chiều thuận \(\Rightarrow\) Loại.
Đáp án B: Nếu giảm áp suất trong lò nung thì cân bằng sẽ chuyển dịch theo chiều làm tăng áp suất của hệ phản ứng, tức tạo ra thêm phân tử cho nên cân bằng sẽ chuyển dịch theo chiều thuận \(\Rightarrow\) Loại.
Đáp án C : Bơm thêm khí \(\mathrm{CO}_{2}\) vào lò phản ứng thì cân bằng chuyển dịch theo chiều làm giảm khí \(\mathrm{CO}_{2}\), tức là cân bằng chuyển dịch theo chiều nghịch \(\Rightarrow\) Chọn.
Đáp án D : Khi tăng nhiệt độ của lò nung thì cân bằng chuyển dịch theo chiều thu nhiệt nên cân bằng sẽ chuyển dịch theo chiều thuận \(\Rightarrow\) Loại.
Đáp án đúng là \(C\).
Phương pháp giải:
- Tính lượng nhiệt cần cung cấp để tạo ra 420 tấn vôi sống.
- Tính lượng nhiệt thực tế mà than đá cần phải cung cấp (vì hiệu suất sử dụng nhiệt là \(60 \%\) ).
- Tính khối lượng than đá thực tế cần sử dụng.
Lời giải:
- Phản ứng nhiệt phân 1 mol đá vôi hay tạo ra 1 mol CaO cần được cung cấp lượng nhiệt là \(179,2 \mathrm{kJ}\).
- Để sản xuất 420 tấn vôi sống/ngày tương đương \(\frac{420.10^{6}}{56}=75.10^{5} \mathrm{mol} \mathrm{CaO}\) thì cần một lượng nhiệt là:
\(75.10^{5}.179,2=1344.10^{6} \mathrm{kJ}\)
- Lượng nhiệt trên được cung cấp bởi than đá, nhưng chỉ tương ứng với \(60 \%\) nhiệt mà than đá tỏa ra.
Vậy lượng nhiệt ban đầu mà than đá có thể cung cấp là: \(1344.10^{6}: 60 \%=224.10^{7} \mathrm{kJ}\)
- Khối lượng than đá cần đốt cháy là: \(224.10^{7}: 25000=896.10^{3} \mathrm{kg}\)

Trọn Bộ Giáo Án Word & PowerPoint Tiếng Anh 12 – I-Learn Smart World – Năm Học 2025-2026

Trọn Bộ Giáo Án Word & PowerPoint Tiếng Anh 12 – Global Success – Năm Học 2025-2026

Trọn Bộ Giáo Án Word & PowerPoint Hóa Học 12 – Kết Nối Tri Thức – Năm Học 2025-2026

Trọn Bộ Giáo Án Word & PowerPoint Hóa Học 12 – Chân Trời Sáng Tạo – Năm Học 2025-2026

Trọn Bộ Giáo Án Word & PowerPoint Công Nghệ 12 – Kết Nối Tri Thức – Năm Học 2025-2026

Trọn Bộ Giáo Án Word & PowerPoint Địa Lí 12 – Chân Trời Sáng Tạo – Năm Học 2025-2026
ĐĂNG KÝ GÓI THI VIP
- Truy cập hơn 100K đề thi thử và chính thức các năm
- 2M câu hỏi theo các mức độ: Nhận biết – Thông hiểu – Vận dụng
- Học nhanh với 10K Flashcard Tiếng Anh theo bộ sách và chủ đề
- Đầy đủ: Mầm non – Phổ thông (K12) – Đại học – Người đi làm
- Tải toàn bộ tài liệu trên TaiLieu.VN
- Loại bỏ quảng cáo để tăng khả năng tập trung ôn luyện
- Tặng 15 ngày khi đăng ký gói 3 tháng, 30 ngày với gói 6 tháng và 60 ngày với gói 12 tháng.
 - Thu thập kết quả của phép đo khối lượng của hợp chất X thông qua kết quả phép đo phổ khối lượng (MS):
- Thu thập kết quả của phép đo khối lượng của hợp chất X thông qua kết quả phép đo phổ khối lượng (MS):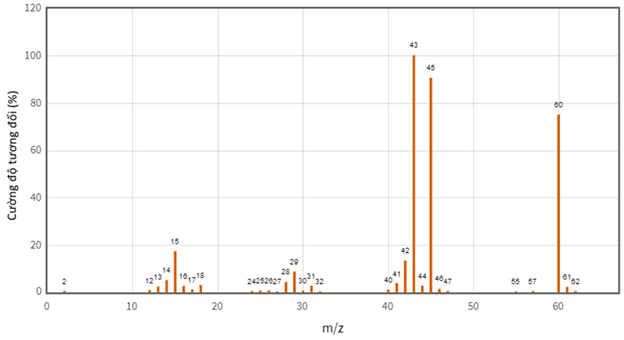 Đốt chất hợp chất hữu cơ X thấy thành phần phần trăm các nguyên tố về khối lượng: \(\% \mathrm{mC}=40 \%\); \(\% \mathrm{mH}=6,67 \%\), còn lại là của nguyên tố oxygen.
Đốt chất hợp chất hữu cơ X thấy thành phần phần trăm các nguyên tố về khối lượng: \(\% \mathrm{mC}=40 \%\); \(\% \mathrm{mH}=6,67 \%\), còn lại là của nguyên tố oxygen.
 Phát biểu nào sau đây không đúng?
Phát biểu nào sau đây không đúng? Thể tích \(\mathrm{KMnO}_{4}\) xác định được là (làm tròn đến chữ số thập phân thứ ba)
Thể tích \(\mathrm{KMnO}_{4}\) xác định được là (làm tròn đến chữ số thập phân thứ ba)