Đề thi thử Tốt nghiệp THPT năm 2025 môn Hóa học Sở GD&ĐT TP.Đà Nẵng - Đề 4
28 câu hỏi 60 phút
Đun nước cứng lâu ngày, trong ấm nước xuất hiện một lớp cặn. Thành phần chính của lớp cặn đó là

\(\mathrm{CaCl}_{2}\)
\(\mathrm{CaCO}_{3}\)
\(\mathrm{Na}_{2} \mathrm{CO}_{3}\)
CaO
Lớp cặn đó là \(\mathrm{CaCO}_{3}, \mathrm{MgCO}_{3}\) do trong nước tự nhiên có \(\mathrm{Ca}^{2+}, \mathrm{HCO}_{3}\) :
\(\mathrm{Ca}\left(\mathrm{HCO}_{3}\right)_{2} \xrightarrow{\mathrm{t}} \mathrm{CaCO}_{3}+\mathrm{CO}_{2}+\mathrm{H}_{2} \mathrm{O}\)
Danh sách câu hỏi:
Câu 1:
Đun nước cứng lâu ngày, trong ấm nước xuất hiện một lớp cặn. Thành phần chính của lớp cặn đó là

Lớp cặn đó là \(\mathrm{CaCO}_{3}, \mathrm{MgCO}_{3}\) do trong nước tự nhiên có \(\mathrm{Ca}^{2+}, \mathrm{HCO}_{3}\) :
\(\mathrm{Ca}\left(\mathrm{HCO}_{3}\right)_{2} \xrightarrow{\mathrm{t}} \mathrm{CaCO}_{3}+\mathrm{CO}_{2}+\mathrm{H}_{2} \mathrm{O}\)
Chọn B.
Oxide bị khử bởi H2 thì oxide kim loại sau Al => loại Al, Mg.
Kim loại tác dụng H2SO4 loãng nên loại Cu => chọn Fe.
Câu 4:
Chất X có công thức \(\mathrm{H}_{2} \mathrm{N}-\mathrm{CH}_{2}-\mathrm{COOH}\). Tên gọi của X là
Chọn A.
CTPT của X có dạng: (RCOO)2(R’COO)C3H5
Theo đề ta có:
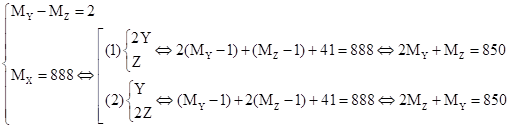
Như vậy ta có 2 hệ
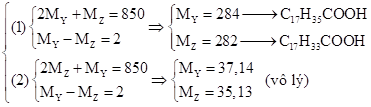
Câu 6:
Nhóm khí nào sau đây trong không khí khi vượt quá mức cho phép sẽ gây ra hiện tượng mưa acid?
Câu 11:
Phát biểu nào sau đây đúng?
Câu 13:
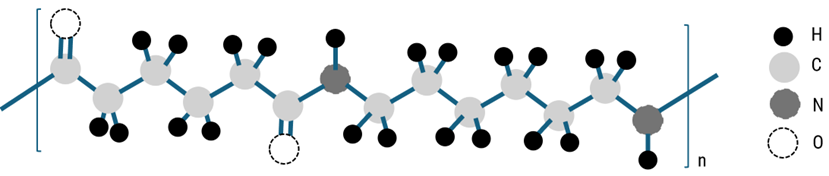
Polymer nào trong các polymer cho dưới đây được điều chế bằng phản ứng trùng hợp methyl acrylate?
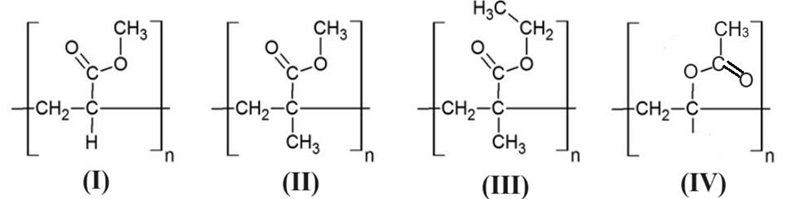
Câu 14:
Phát biểu nào sau đây sai?
Câu 16:
Phát biểu nào sau đây sai?
Câu 19:
Trong công nghiệp, methanol \(\left(\mathrm{CH}_{3} \mathrm{OH}\right.\), nhiệt độ sôi \(\left.65^{\circ} \mathrm{C}\right)\) được tổng hợp từ CO và \(\mathrm{H}_{2}\) theo sơ đồ sau:

Cho các phát biểu sau:
Phản ứng xảy khi đun nóng hỗn hợp A là : \(\mathrm{CH}_{4}+\mathrm{H}_{2} \mathrm{O} \xrightarrow{200^{\circ} \mathrm{C}, 10 \text { bar }} \mathrm{CO}_{2}+\mathrm{H}_{2}\)
Chất ngưng tụ thoát ra ở (4) là \(\mathrm{H}_{2} \mathrm{O}\) và \(\mathrm{CH}_{4}\) lỏng
Cho quá trình tổng hợp methanol là quá trình tỏa nhiệt, để tăng hiệu suất tổng hợp methanol thì cần tăng nhiệt độ và giảm áp suất của hệ
Nếu cho tốc độ lưu chuyển của \(\mathrm{CH}_{4}\) là \(86 \mathrm{L} / \mathrm{s}\) và \(\mathrm{H}_{2} \mathrm{O}\) là \(150 \mathrm{L} / \mathrm{s}\) thì tốc độ lưu chuyển của \(\mathrm{H}_{2} \mathrm{O}\) dưở 4 là \(56 \mathrm{L} / \mathrm{s}\)
Câu 20:
Acetylene thường được dùng làm nhiên liệu, ví dụ đèn xì oxygen - acetylene dùng để hàn cắt kim loại. Khí methane là thành phần chính của khí thiên nhiên cũng được sử dụng làm nhiên liệu. Methane và acetylene cháy theo phương trình hóa học sau:
CH4 (g) + 2 O2 (g) CO2 (g) + 2H2O (g) (1)
2C2H2 (g) + 5O2 (g) 4CO2 (g) + 2H2O (g) (2)
Cho biết nhiệt tạo thành chuẩn của một số chất như sau:
|
Chất |
CH4 (g) |
C2H2 (g) |
CO2 (g) |
H2O (g) |
|
|
- 74,6 |
227,4 |
- 393,5 |
- 241,8 |
Cho các phát biểu sau:
Biến thiên enthalpy chuẩn của phương trình (2) là - \(2512,4 \mathrm{kJ}\)
Biến thiên enthalpy chuẩn của phương trình (1) là - \(802,5 \mathrm{kJ}\)
Nếu xét cùng số mol thì lượng nhiệt tỏa ra từ \(\mathrm{C}_{2} \mathrm{H}_{2}\) gấp \(\mathrm{CH}_{4}\) xấp xỉ 3,1 lần (cho phép làm tròn đến hàng phần mười)
Theo giá quốc tế thì 1 bình methane 40 L dạng lỏng có giá \(1035000 \mathrm{VNĐ}\) và 1 bình acetylene 40 L dạng lỏng có giá \(1334000 \mathrm{VNĐ}\), tính về mặt kinh tế thì việc sử dụng khí methane làm khí đốt sẽ có ưu thế hơn. Cho khối lượng riêng của methane và acetylene lần lượt là \(0,657 \mathrm{kg} / \mathrm{m}^{3}\) và \(1,1 \mathrm{kg} / \mathrm{m}^{3}\)
Câu 21:
Cho sơ đồ phản ứng sau:
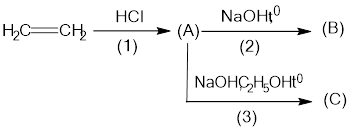
Cho các phát biểu sau:
Phản ứng (2) là phản ứng oxid hoá - khử
Hợp chất hữu cơ A là \(\mathrm{CH}_{3}-\mathrm{CH}_{2} \mathrm{Cl}\)
Phương trình hoá học (2) là \(\mathrm{CH}_{3}-\mathrm{CH}_{2} \mathrm{Cl}+\mathrm{NaOH} \longrightarrow \mathrm{CH}_{3}-\mathrm{CH}_{2} \mathrm{OH}+\mathrm{NaCl}\)
Nếu thay ethylene bằng but-1-ene thì sản phẩm chính thu được ở phản ứng (3) là \(\mathrm{CH}_{3} \mathrm{CH}=\mathrm{CHCH}_{3}\)
Câu 22:
Poly(ethylene terephthalate) (viết tắt là PET ) là một polymer được điều chế từ terephthalic acid và ethylene glycol. PET được ử dụng để sản xuất tơ, chai đựng nước uống, hộp đựng thực phẩm. Để thuận lợi cho việc nhận biết, sử dụng và tái chế thì các đồ nhựa làm từ vật liệu chứa PET thường được in kí hiệu là số 1 (như hình bên). Cho các phát biểu sau:
PET thuộc loại polyeste
Tơ được chế tạo từ PET thuộc loại tơ tổng hợp
Trong một mắt xích PET , phần trăm khối lượng carbon là \(62,5 \%\)
PET được điều chế bằng phản ứng trùng ngưng các monomer tương ứng
 (*)
(*)