Trắc nghiệm Kim loại kiềm thổ và hợp chất quan trọng của chúng Hóa Học Lớp 12
-
Câu 1:
Khi cho Mg tác dụng với dung dịch sắt(III)clorua dư. Phản ứng xảy ra là:
A. \({\;3Mg{\rm{ }} + {\rm{ }}2FeC{l_3}\; \to {\rm{ }}2Fe{\rm{ }} + {\rm{ }}3MgC{l_2}}\)
B. \({Mg{\rm{ }} + {\rm{ }}4FeC{l_3}\; \to {\rm{ }}MgC{l_2}\; + {\rm{ 4}}FeC{l_2}}\)
C. \({{\rm{ }}Mg{\rm{ }} + {\rm{ }}2FeC{l_3}\; \to {\rm{ }}MgC{l_2}\; + {\rm{ }}2FeC{l_2}}\)
D. Không xảy ra phản ứng
-
Câu 2:
Cho dãy các kim loại: Na, Ba, Al, K, Mg. Số kim loại trong dãy phản ứng với lượng dư dung dịch FeCl3 thu được kết tủa là
A. 5
B. 3
C. 2
D. 4
-
Câu 3:
Cho 2,4 g Mg tác dụng với nước đun nóng thu được khí X dẫn toàn bộ khí X qua CuO nung nóng, phản ứng xảy ra hoàn toàn. Khối lượng CuO tham gia phản ứng là:
A. 9g
B. 7g
C. 12g
D. 8g
-
Câu 4:
Chất X tác dụng với dung dịch HCl. Khi chất X tác dụng với dung dịch Ca(OH)2 sinh ra kết tủa. Chất X là
A. AlCl3
B. CaCO3
C. BaCl2
D. Ca(HCO3)2
-
Câu 5:
Phát biểu nào sau đây là sai?
A. Theo chiều tăng dần của điện tích hạt nhân, nhiệt độ nóng chảy của kim loại kiềm giảm dần.
B. Ở nhiệt độ thường, tất cả các kim loại kiềm thổ đếu tác dụng được với nước
C. Fe, Al, Cr thụ động trong axit sunfuric đặc nguội
D. Nhôm bền trong môi trường không khí và nước là do màng oxi Al2O3 bền vững bảo vệ
-
Câu 6:
Khi cho axit axetic tác dụng với kim loại magie có hiện tượng gi xảy ra?
A. Có khí H2 thoát ra
B. Có hiện tượng kết tủa đen
C. Tạo thành dung dịch màu xanh lam
D. Có khí mùi khai thoát ra.
-
Câu 7:
Cho Mg tác dụng với dung dịch axit axetic thu được 2,24 lít khí (đktc). Khối lượng của muối thu được là
A. 1,42 g
B. 0,71g
C. 14,2 g
D. 7,1 g
-
Câu 8:
Khi cho Mg tác dụng với axit sunfuric đặc nóng thu được muối X và khí không màu có mùi trứng thối. Cho dung dịch X tác dụng với dung dịch BaCl2 dư thu được 2,33 g kết tủa.Khối lượng Mg tham gia phản ứng là
A. 1,2 g
B. 0,12 g
C. 2,4 g
D. 0,24 g
-
Câu 9:
Cho kim loại Mg tác dụng với axit sunfuric đặc nóng thấy thoát ra khí không màu mùi trứng thối. Sản phẩm khử của axit sunfuric là
A. S
B. SO2
C. H2S
D. SO3
-
Câu 10:
Cho phản ứng sau: Mg + H2SO4 → MgSO4 + H2S + H2O
Hệ số tối giản của H2SO4 trong phương trình trên là:
A. 4
B. 5
C. 6
D. 7
-
Câu 11:
Khi cho Mg tác dụng với axit sunfuric đặc nóng, các sản phẩm khử có thể có là:
A. H2
B. SO2
C. S
D. Cả B và C
-
Câu 12:
Khi cho Mg tác dụng với axit sunfuric đặc nóng thu được 3,2 g kết tủa màu vàng. Khối lượng muối thu được sau phản ứng là:
A. 6g
B. 12g
C. 36 g
D. 12,8 g
-
Câu 13:
Cho phản ứng sau: Mg + H2SO4 → MgSO4 + S + H2O
Tổng hệ số tối giản của phản ứng trên là:
A. 12
B. 14
C. 15
D. 16
-
Câu 14:
Cho phương trình hóa học sau: \(Mg{\rm{ }} + {\rm{ }}{H_2}S{O_4}\; \to {\rm{ }}MgS{O_4}\; + {\rm{ }}S{O_2}\; + {\rm{ }}{H_2}O\)
Tổng hệ số tối giản của phương trình trên:
A. 6
B. 7
C. 8
D. 9
-
Câu 15:
Cho Mg tác dụng với dụng dịch axit nitric loãng thu được khí không màu hóa nâu ngoài không khí. Phương trình phản ứng xảy ra là:
A. \({Mg{\rm{ }} + {\rm{ }}4HN{O_3}\; \to {\rm{ }}Mg{{\left( {N{O_3}} \right)}_2}\; + {\rm{ }}2N{O_2}\; + {\rm{ }}2{H_2}O}\)
B. \({3Mg{\rm{ }} + {\rm{ }}8HN{O_3}\; \to {\rm{ }}3Mg{{\left( {N{O_3}} \right)}_2}\; + {\rm{ }}2NO{\rm{ }} + {\rm{ }}4{H_2}O}\)
C. \({5Mg{\rm{ }} + {\rm{ }}12HN{O_3}\; \to {\rm{ }}5Mg{{\left( {N{O_3}} \right)}_2}\; + {\rm{ }}N2{\rm{ }} + {\rm{ }}6{H_2}O}\)
D. \({4Mg{\rm{ }} + {\rm{ }}10HN{O_3}\; \to {\rm{ }}4Mg{{\left( {N{O_3}} \right)}_2}\; + {\rm{ }}N{H_4}N{O_3}\; + {\rm{ }}3{H_2}O}\)
-
Câu 16:
Hoà tan hoàn toàn m gam Mg trong dung dịch HNO3, thu được dung dịch Y và 4,48 lít hỗn hợp khí Z ở đktc gồm N2O và NO có tỉ khối so với hydro là 18,5. Giá trị của m là:
A. 2,4 g
B. 1,2 g
C. 13,2 g
D. 16,5 g
-
Câu 17:
Cho 2,4 g Mg tác dụng với dụng với HNO3 dư thu được V lít khí N2O sản phẩm khử duy nhất. Giá trị của V là
A. 2,24 lít
B. 0,56 lít
C. 1,12 lít
D. 0,336 lít
-
Câu 18:
Cho 250 ml dung dịch HCl 1M vào 100 ml dung dịch X chứa Na2CO3 1,0M và KHCO3 1,5M, sinh ra V lít khí (ở đktc) đồng thời thu được Y. Cho lượng dư Ca(OH)2 vào Y thu được bao nhiêu gam chất kết tủa.
A. 15,0.
B. 10,0.
C. 25,0.
D. 12,5.
-
Câu 19:
Cho Na – Ba tác dụng với nước được C và 3,36 lít H2 ( ở đktc). Thể tích H2SO4 2M cần dùng trung hòa X là bao nhiêu?
A. 150ml
B. 75ml
C. 60ml
D. 30ml
-
Câu 20:
Lấy 3,44g hỗn hợp 2 muối cacbonat kiềm cho vào HCl dư được 448 ml CO2 (đktc) thì lượng muối clorua ?
A. 4,26 g.
B. 3,66 g.
C. 5,12 g.
D. 6,72g.
-
Câu 21:
Lấy 4 g kim loại R hoá trị II cho vào HCl được 2,24 lít H2 (đktc) và dung dịch X. Cho Na2CO3 dư vào X thì nhận được bao nhiêu (g) kết tủa.
A. 8,12.
B. 10,0.
C. 11,12.
D. 12,0.
-
Câu 22:
Lấy 2 thanh kim loại M bên dưới đây biết chúng có hoá trị II với nồng độ bằng nhau. Thanh 1 nhúng vào 250 ml FeSO4; thanh 2 nhúng vào 250 ml CuSO4. Sau khi phản ứng, thanh 1 tăng 16g, thanh 2 tăng 20g.
A. Mg.
B. N.
C. Zn.
D. Be.
-
Câu 23:
1,26 gam một kim loại nào dưới đây sẽ tác dụng với H2SO4 loãng tạo ra 3,42 gam muối sunfat?
A. Mg.
B. Fe.
C. Ca.
D. Al.
-
Câu 24:
Cho 20,15 gam 2 axit no đơn chức vào Na2CO3 được bao nhiêu lít khí CO2 (đktc) và dung dịch muối, biết cô cạn dung dịch thì thu được 28,96 gam muối.
A. 2,24 lít
B. 4,48 lít
C. 3,36 lít
D. 1,12 lít
-
Câu 25:
Cho 14 gam hỗn hợp 2 muối MCO3 và N2(CO3)3 bằng HCl dư được A và 0,672 lít khí (đktc). Cô cạn A được bao nhiêu gam muối khan?
A. 16,33 g.
B. 14,33 g.
C. 9,265 g.
D. 12,65 g.
-
Câu 26:
Tìm tỉ lệ a : b biết cho CO2 vào a mol Ca(OH)2 và b mol NaOH thì kết qua như sau:
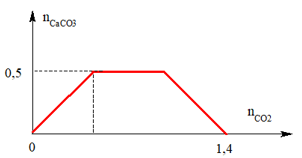
A. 4 : 5.
B. 5 : 4.
C. 2 : 3.
D. 4 : 3.
-
Câu 27:
Sục bao nhiêu mol CO2 vào Ba(OH)2 ta có kết quả theo đồ thị sau:
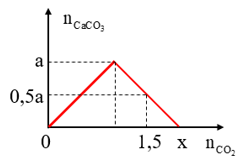
A. 1,8 mol.
B. 2,2 mol.
C. 2,0 mol.
D. 2,5 mol.
-
Câu 28:
Cho NaOH vào a mol HCl và b mol ZnSO4 thì được kết quả như sau:
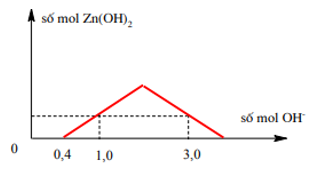
Tính tỉ lệ a : b?
A. 1 : 2.
B. 3 : 2.
C. 2 : 3.
D. 3 : 4.
-
Câu 29:
Cho KOH vào a mol HCl và x mol ZnSO4 thì được đồ thị hình bên, hãy tính giá trị của x (mol)?
A. 0,4.
B. 0,6.
C. 0,7.
D. 0,65.
-
Câu 30:
Sục bao nhiêu lít CO2 (đktc) vào 200 ml KOH 0,5M và Ba(OH)2 0,375M để ta thu được 11,82 gam kết tủa.
A. 1,344l lít.
B. 4,256 lít.
C. 8,512 lít.
D. 1,344l lít hoặc 4,256 lít.
-
Câu 31:
Sục CO2 vào Ca(OH)2 và KOH ta được đồ thi, em hãy tìm giá trị của x?
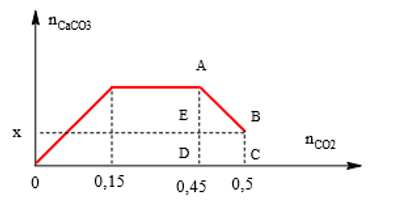
A. 0,12 mol.
B. 0,11 mol.
C. 0,13 mol.
D. 0,10 mol.
-
Câu 32:
Tìm x, y, z biết khi sục CO2 vào 0,1 mol NaOH; x mol KOH và y mol Ba(OH)2, thu được kết quả như sau:
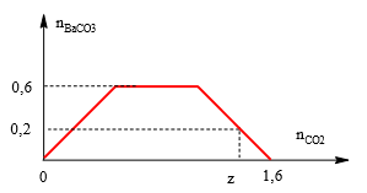
A. 0,60; 0,40 và 1,50.
B. 0,30; 0,60 và 1,40.
C. 0,30; 0,30 và 1,20.
D. 0,20; 0,60 và 1,25
-
Câu 33:
Cần cho bao nhiêu (lít) khí CO2 vào 200 ml Ba(OH)2 0,5M và NaOH 1,0M để kết tủa thu được là cực đại?
A. 2,24 lít ≤ V ≤ 8,96 lít.
B. 2,24 lít ≤ V ≤ 5,6 lít.
C. 2,24 lít ≤ V ≤ 4,48 lít.
D. 2,24 lít ≤ V≤ 6,72 lít.
-
Câu 34:
Hãy tính a : b biết khi sục từ từ đến dư CO2 vào dung dịch hỗn hợp gồm a mol NaOH và b mol Ca(OH)2, thì thu được kết quả như bên dưới:
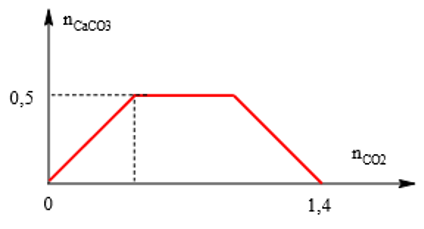
A. 4 : 5.
B. 5 : 4.
C. 2 : 3.
D. 4 : 3.
-
Câu 35:
Cho 270ml dung dịch Ba(OH)2 0,2M vào dung dịch X chứa 0,025 mol CO32-; 0,1 mol Na+; 0,25 mol NH4+ và 0,3 mol Cl-. Tổng khối lượng X và dung dịch Ba(OH)2 giảm đi bao nhiêu?
A. 4,215g
B. 5,296g
C. 6,761g
D. 7,015g
-
Câu 36:
Khi cô cạn dung dịch Y chứa Ca2+ 0,1 mol, Mg2+ 0,3 mol, Cl- 0,4 mol, HCO3- y mol thì lượng muối khan thu được là mấy?
A. 37,4g
B. 49,8g
C. 25,4g
D. 30,5g
-
Câu 37:
Hòa tan 10g hỗn hợp X gồm Mg và Fe vào HCl 2M thu được Y và 5,6l khí H2 (đktc). Để kết tủa Y cần vừa đủ 300ml NaOH 2M.Thể tích dung dịch HCl đã dùng là mấy?
A. 0,2 lít
B. 0,24 lít
C. 0,3 lít
D. 0,4 lít
-
Câu 38:
Trộn Ba2+; OH- 0,0 6mol và Na+ 0,02 mol vào HCO3- 0,04 mol; CO32- 0,03 mol và Na+. Khối lượng kết tủa thu được là mấy?
A. 3,94g
B. 5,91g
C. 7,88g
D. 1,71g
-
Câu 39:
Hấp thụ 2,688 lít CO2 (đktc) vào 2,5 lít dung dịch Ba(OH)2 có nồng độ là bao nhiêu để ta thu được 15,76 gam kết tủa?
A. 0,032
B. 0,048
C. 0,06
D. 0,04
-
Câu 40:
Hấp thụ 0,672lit khí CO2 (đktc) vào 1 lít dd gồm NaOH 0,025M và Ca(OH)2 0,0125M, thu được mấy gam kết tủa.
A. 2,00
B. 0,75
C. 1,25
D. 1,00
-
Câu 41:
Cho a mol Ca(HCO3)2 tác dụng với a mol chất tan X., hãy tìm X để thu được lượng kết tủa lớn nhất thì X?
A. Ba(OH)2.
B. Ca(OH)2.
C. NaOH.
D. Na2CO3.
-
Câu 42:
Cho 150 cm3 dung dịch NaOH 7M tác dụng với 100cm3 dung dịch Al2(SO4)3 1M. Xác định nồng độ mol của NaOH?
A. 0,8M
B. 1,2M
C. 1M
D. 0,75M
-
Câu 43:
Cho Na và Al có tỉ lệ mol tương ứng là 1: 2 vào nước dư thu được 8,96 lít khí H2 (đktc) và bao nhiêu gam chất rắn không tan.
A. 3,6 (g)
B. 2,7 (g)
C. 1,2 (g)
D. 5,4 (g)
-
Câu 44:
Đốt 16,1 gam Na trong bình chứa đầy khí O2 thu được bao nhiêu gam hỗn hợp chất rắn Y gồm Na2O, Na2O2 và Na dư. Hòa tan hết toàn bộ lượng Y trên vào nước nóng, sinh ra 5,04 lít (đktc) hỗn hợp khí Z, có tỉ khối so với He là 3?
A. 18,8
B. 21,7
C. 18,5
D. 21,4
-
Câu 45:
Tìm biểu thức liên hệ giữa V với a, b biết chúng thõa mãn điều kiện cho a mol HCl vào b mol Na2CO3 đồng thời khuấy đều, thu được V lít khí (ở đktc) và dung dịch X. Khi cho dư nước vôi trong vào dung dịch X thấy có xuất hiện kết tủa. B
A. V = 22,4(a - b).
B. V = 11,2(a - b).
C. V = 11,2(a + b).
D. V = 22,4(a + b).
-
Câu 46:
Cho 0,96 gam bột Cu và HNO3 đặc, nóng (dư) sau đó hấp thụ hết khí thoát ra vào 0,4 lít dung dịch KOH 0,1M thu được 0,4 lít X. Dung dịch X có giá trị pH là bao nhiêu?
A. 12,4
B. 13,4
C. 1,6
D. 2,6
-
Câu 47:
Sau khi thực hiện phản ứng nhiệt nhôm với Fe3O4 thu được chất rắn A và nhận thấy khối lượng nhiệt nhôm tăng 0,96(g). Cho A tác dụng với dung dịch NaOH dư thu được 0,672 lít khí (đktc), (giả sử các phản ứng đều xảy ra với hiệu suất 100%). Khối lượng của A là:
A. 1,08g
B. 1,62g
C. 2,1g
D. 5,1g
-
Câu 48:
Cần cho mấy gam Mg vào 0,12 mol FeCl3 để thu được 3,36 gam chất rắn?
A. 2,88
B. 4,32
C. 5,04
D. 2,16
-
Câu 49:
Cho tối đa bao nhiêu lít dung dịch NaOH 0,4M tác dụng với 58,14g Al2(SO4)3 để thu được 23,4g kết tủa.
A. 2,65 l
B. 2,24 l
C. 1,12 l
D. 3,2 l
-
Câu 50:
Nung 13,4 gam hỗn hợp 2 muối cacbonat của 2 kim loại hóa trị 2, thu được 6,8 gam chất rắn và khí X sinh ra cho hấp thụ vào 75ml dung dịch NaOH 1M thì sẽ được bao nhiêu gam muối?
A. 5,8 g
B. 6,5 g
C. 4,2 g
D. 6,3 g














