Thực hiện thí nghiệm sau: lấy 5,2 gam một mẫu bột oxide sắt và cho đủ lượng carbon monoxide, thực hiện phản ứng ở nhiệt độ cao, đến khi thu được kim loại Fe và khí X. Cho khí X sinh ra qua nước vôi trong dư thì thu được 8,00 gam kết tủa trắng. Tỷ lệ mol của Fe và O trong mẫu oxide Fe là
Hãy suy nghĩ và trả lời câu hỏi trước khi xem đáp án
Sơ đồ hóa: 5, 2gam oxide \(\mathrm{Fe}\left\{\begin{array}{l}\mathrm{Fe} \\ \mathrm{O}\end{array} \xrightarrow{+\mathrm{CO}}\left(\begin{array}{l}\mathrm{Fe} \\ \mathrm{CO}_{2} \xrightarrow{\mathrm{Ca}(\mathrm{OH})_{2}} 8 \mathrm{gam} \mathrm{CaCO}_{3} \downarrow\end{array}\right.\right.\)
Theo đề ta có :
\(\mathrm{n}_{\mathrm{CaCO}_{3}}=\frac{8}{100}=0,08 \mathrm{mol} \xrightarrow{\text { BTNTC }} \mathrm{n}_{\mathrm{CO}_{2}}=0,08 \mathrm{mol} \Rightarrow \mathrm{n}_{\text {Otrongoxide }}=0,08 \mathrm{mol} \Rightarrow \mathrm{m}_{\text {Otrongoxide }}=0,08.16=1,28 \mathrm{gam}\)
Khối lượng Fe trong oxide là \(\mathrm{m}_{\text {Fetrongoxide }}=5,2-1,28=3,92 \mathrm{gam} \Rightarrow \mathrm{n}_{\text {Fetrongoxide }}=\frac{3,92}{56}=0,07 \mathrm{mol}\)
Ta có: \(\frac{\mathrm{n}_{\text {Fetrongoxide }}}{\mathrm{n}_{\text {Otrong oxide }}}=\frac{0,07}{0,08}=\frac{7}{8}\)
Tuyển Tập Đề Thi Tham Khảo Tốt Nghiệp THPT Năm 2025 - Hóa Học - Bộ Đề 06 giúp học sinh lớp 12 ôn tập hiệu quả và tự tin bước vào kỳ thi Tốt nghiệp THPT năm 2025. Mỗi đề thi trong tài liệu được xây dựng theo đúng cấu trúc chuẩn của Bộ Giáo dục và Đào tạo, bao gồm ba phần: trắc nghiệm nhiều lựa chọn, trắc nghiệm đúng – sai và trắc nghiệm trả lời ngắn. Các câu hỏi được chọn lọc kỹ lưỡng, bám sát nội dung chương trình, tích hợp kiến thức liên môn và có độ phân hóa phù hợp, giúp học sinh không chỉ ôn tập lý thuyết mà còn rèn luyện kỹ năng giải đề thực tiễn. Đặc biệt, phần đáp án và hướng dẫn giải chi tiết đi kèm giúp học sinh dễ dàng tự đánh giá kết quả và nhận diện các dạng bài quan trọng.
Câu hỏi liên quan
Khi xảy ra phản ứng hóa học, lượng chất đầu biến đổi như thế nào?
Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai. Câu 1. Nhúng thanh Cu tinh khiết có khối lượng là \(\mathrm{m}_{1}(\mathrm{gam})\) vào dung dịch iron(III) chloride, sau một thời gian, lấy thanh Cu ra cân lại thấy khối lượng là \(\mathrm{m}_{2}(\mathrm{gam})\). Cho các phát biểu sau:
Cho phản ứng hóa học: \(\mathrm{Zn}+\mathrm{Cu}\left(\mathrm{NO}_{3}\right)_{2} \longrightarrow \mathrm{Zn}\left(\mathrm{NO}_{3}\right)_{2}+\mathrm{Cu}\). Trong phản ứng trên xảy ra các quá trình là
Ammonium sulfate \(\left(\mathrm{NH}_{4}\right)_{2} \mathrm{SO}_{4}\) là một loại phân bón quan trọng giúp cung cấp nguyên tố N và S , thúc đẩy sự phát triển và tăng năng suất cây trồng. Số oxi hóa của nitrogen trong \(\left(\mathrm{NH}_{4}\right)_{2} \mathrm{SO}_{4}\) là bao nhiêu?
Vỏ trứng có chứa calcium ở dạng \(\mathrm{CaCO}_{3}\). Để xác định hàm lượng \(\mathrm{CaCO}_{3}\) trong vỏ trứng, các bước thí nghiệm được tiến hành như sau:
Bước 1: Cân 2,0 gam vỏ trứng khô, đã làm sạch, hoà tan hoàn toàn trong 50 mL dung dịch \(\mathrm{HCl} 0,1 \mathrm{M}\). Lọc dung dịch sau phản ứng thu được 50 mL dung dịch X .
Bước 2; Chuẩn độ \(10,0 \mathrm{~mL}\) dung dịch X bằng dung dịch NaOH chuẩn với chỉ thị phenolphthalein thì tại điểm kết thúc chuẩn độ, dung dịch xuất hiện màu hồng.
Kết quả chuẩn độ \(10,0 \mathrm{~mL}\) dung dịch X khi sử dụng dung dịch chuẩn \(\mathrm{NaOH} \ 0,01 \mathrm{M}\) được ghi trong bảng sau:
Giả thiết các tạp chất khác trong vỏ trứng không phản ứng với HCl , chấp nhận sai số chuẩn độ không đáng kể, các thành phần khác trong vỏ trứng không ảnh hưởng đến kết quả chuẩn độ. Tính hàm lượng \(\mathrm{CaCO}_{3}\) trong vỏ trứng.
Potassium dichromate \(\left(\mathrm{K}_{2} \mathrm{Cr}_{2} \mathrm{O}_{7}\right)\) có thể được sử dụng để phát hiện nồng độ còn trong hơi thở. Phương trình phản ứng của alcohol và \(\mathrm{K}_{2} \mathrm{Cr}_{2} \mathrm{O}_{7}\) như sau:
\(3 \mathrm{CH}_{3} \mathrm{CH}_{2} \mathrm{OH}+2 \mathrm{Cr}_{2} \mathrm{O}_{7}{ }^{2-}+16 \mathrm{H}^{+} \longrightarrow 3 \mathrm{CH}_{3} \mathrm{COOH}+4 \mathrm{Cr}^{3+}+11 \mathrm{H}_{2} \mathrm{O}\)
Sau phản ứng, màu sắc chuyển từ cam sang xanh lục, dữ liệu đo được bằng thiết bị có thể chuyển đổi thành nồng độ cồn. Ở nhiệt độ và áp suất bình thường, tỷ lệ nồng độ cồn trong máu ( \(\mathrm{mg} / \mathrm{L}\) ) so với nồng độ cồn trong hơi thở \((\mathrm{mg} / \mathrm{L})\) hiện đang là 2100 : 1. Theo luật quy định, nồng độ cồn trong mỗi lít hơi thở không được vượt quá \(0,25 \mathrm{mg}\). Cho đồ thị thể hiện mối quan hệ giữa nồng độ cồn trong hơi thở và chỉ số đo bằng thiết bị như sau:
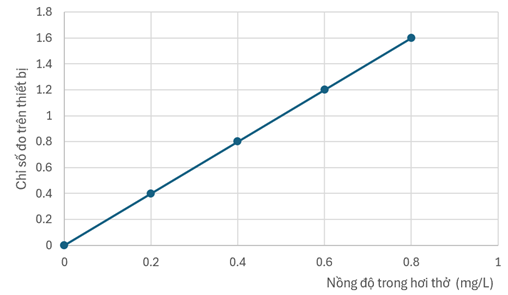
Khi chỉ số của thiết bị đo hơi thở của một người là 0,80 thì nồng độ cồn trong máu ( \(\mathrm{mmol} / \mathrm{L}\) ) của người đó là bao nhiêu? (làm tròn đáp án đến hàng đơn vị).
Trong ăn mòn hóa học, loại phản ứng hóa học xảy ra là phản ứng nào sau đây?
Để xác định hàm lượng muối \(\mathrm{Fe}(\mathrm{II})\) trong 1 mẫu dung dịch A có thể dùng dung dịch thuốc tím \(\mathrm{KMnO}_{4}\), phương trình ion như sau:
\( \mathrm{MnO}_{4}^{-}+5 \mathrm{Fe}^{2+}+8 \mathrm{H}^{+} \longrightarrow \mathrm{Mn}^{2+}+5 \mathrm{Fe}^{3+}+4 \mathrm{H}_{2} \mathrm{O} \)
+ Người ta lấy \(25,00 \mathrm{mL}\) dung dịch A cho vào bình định mức, thêm nước cất cho đủ 100 mL , dung dịch thu được gọi là dung dịch X .
+ Lấy \(10,00 \mathrm{mL}\) từ dung dịch X chuyển vào bình tam giác. Thêm khoảng 5 mL dung dịch \(\mathrm{H}_{2} \mathrm{SO}_{4} 2 \mathrm{M}\).
+ Tiến hành chuẩn độ 3 lần bằng dung dịch \(\mathrm{KMnO}_{4} 0,02 \mathrm{M}\).
Kết quả thể tích \(\mathrm{KMnO}_{4}\) sau 3 lần chuẩn độ lần lượt là \(20,50 \mathrm{mL} ; 20,55 \mathrm{mL} ; 20,55 \mathrm{mL}\). Tính hàm lượng muối \(\mathrm{Fe}^{2+}(\mathrm{g} / \mathrm{L})\) trong dung dịch A (làm tròn đáp án đến hàng phần mười)
Quá trình nào sau đây xảy hiện tượng hóa học?
Xét phản ứng sau:
\(\mathrm{Fe}_{2} \mathrm{O}_{3}+3 \mathrm{CO} \rightarrow 2 \mathrm{Fe}+3 \mathrm{CO}_{2}\)
Phương trình biểu diễn quá trình khử của phản ứng trên là
Trong hợp chất \(\mathrm{Na}_{2} \mathrm{SO}_{4}\), số oxi hóa của sulfur là
Cho biết giá trị thế điện cực chuẩn của các cặp oxi hoá – khử sau:
Số kim loại trong dãy các kim loại Zn, Ni, Fe, Cu phản ứng được với dung dịch HCl ở điều kiện chuẩn là
Nồng độ ion \(\mathrm{NO}_{3}{ }^{-}\)trong nước uống tối đa cho phép là 9 ppm (part per million - phần triệu). Nếu thừa ion này sẽ gây ra một loại bệnh thiếu máu hoặc tạo thành nitrosamin (một hợp chất gây ung thư đường tiêu hóa). Để xác định hàm lượng ion \(\mathrm{NO}_{3}{ }^{-}\)trong 200 mL nước người ta dùng các hoá chất ( \(\mathrm{Cu}+\mathrm{H}_{2} \mathrm{SO}_{4}\) loãng) thấy cần dùng đến \(1,92 \mathrm{mg} \mathrm{Cu}\). Hàm lượng \(\mathrm{NO}_{3}{ }^{-}\)trong mẫu nước trên là bao nhiêu?
Cho phản ứng chuẩn độ muối Mohr \(\left(\mathrm{FeSO}_{4} \cdot\left(\mathrm{NH}_{4}\right)_{2} \mathrm{SO}_{4} \cdot 6 \mathrm{H}_{2} \mathrm{O}\right)\) trong môi trường acid:
\(\mathrm{Cr}_{2} \mathrm{O}_{7}{ }^{2-}+14 \mathrm{H}^{+}+6 \mathrm{Fe}^{2+} \rightarrow 2 \mathrm{Cr}^{3+}+6 \mathrm{Fe}^{3+}+7 \mathrm{H}_{2} \mathrm{O}\)
Cần bao nhiêu milimol potassium dichromate để oxi hóa \(24 \mathrm{cm}^{3}\) dung dịch muối Mohr \(0,5 \mathrm{M}\) trong môi trường acid (làm tròn kết quả đến chữ số hàng đơn vị)?
Xét phản ứng sau:
\(\mathrm{aKMnO}_{4}+\mathrm{bKI}+\mathrm{H}_{2} \mathrm{O} \rightarrow \mathrm{xI}_{2}+\mathrm{yMnO}_{2}+\mathrm{zKOH}\)
Giá trị của \(\mathrm{x}, \mathrm{y}\) và z trong phản ứng này lần lượt là
Hòa tan 4,875 gam kim loại M (có hóa trị 2) trong HNO3 loãng, dư thì thu được 0,05 mol NO (sản phẩm khử duy nhất). Kim loại M là
Muối Mohr có công thức \(\left(\mathrm{NH}_{4}\right)_{2} \mathrm{Fe}\left(\mathrm{SO}_{4}\right)_{2} \cdot 6 \mathrm{H}_{2} \mathrm{O}\). Để xác định độ tinh khiết của một loại muối Mohr (cho rằng trong muối Mohr chỉ có muối kép ngậm nước nêu trên và tạp chất trơ), một học sinh tiến hành các thí nghiệm sau: Cân chính xác 7,237 gam muối Mohr, pha thành 100 mL dung dịch X. Lấy chính xác 10 mL dung dịch X , thêm 10 mL dung dịch \(\mathrm{H}_{2} \mathrm{SO}_{4} 10 \%\), được dung dịch Y. Chuẩn độ dung dịch Y bằng dung dịch chuẩn \(\mathrm{KMnO}_{4} 0,023 \mathrm{M}\). Thực hiện chuẩn độ 3 lần.
Kết quả đạt được như sau:
Lần chuẩn độ
1
2
3
Thể tích dung dịch KMnO4 (mL)
16,0
16,1
16,0
Cho các phát biểu sau:
Nối dung dịch sodium chloride với nguồn điện và một bóng đèn nhỏ. Quan sát thấy bóng đèn
Nhiệt luyện thép chính là quá trình điều chế sắt từ quặng hematite bằng cách khử oxide của sắt ở nhiệt độ cao trong lò luyện kim.
Phản ứng xảy ra như sau: \(\mathrm{Fe}_{2} \mathrm{O}_{3}+\mathrm{xCO} \rightarrow \mathrm{yFe}+\mathrm{zCO}_{2}\)
Trong phòng thí nghiệm, một học sinh nhúng thanh Cu có khối lượng 12,340 gam vào 256 mL dung dịch \(\mathrm{AgNO}_{3} 0,125 \mathrm{M}\). Sau một thời gian, lấy thanh Cu đem sấy khô và cân lại có khối lượng 12,492 gam. Khối lượng Ag sinh ra là bao nhiêu, nếu giả thiết rằng toàn bộ lượng Ag giải phóng đều bám vào thanh đồng.















