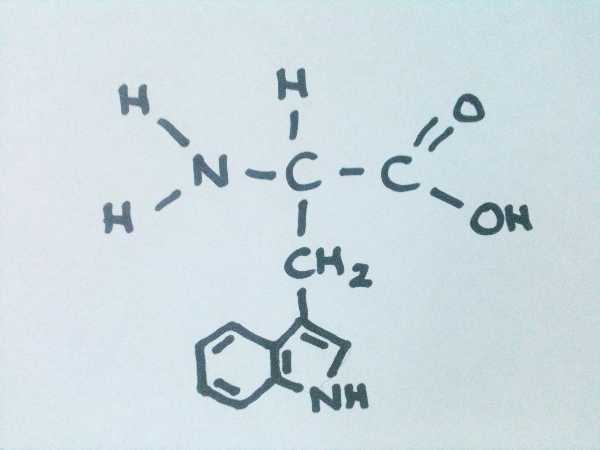
Histidine là một trong những axit amin độc đáo hơn về tính chất hóa học của nó. Nó cũng (cho đến nay) là axit amin phổ biến nhất tại các vị trí hoạt động của các protein đáng chú ý nhất đó là các enzym. Tại sao thế này?
Hãy suy nghĩ và trả lời câu hỏi trước khi xem đáp án
Lời giải:
Báo saiĐịnh nghĩa Bronsted-Lowry về một axit là một chất cho proton. Định nghĩa tương đương của một cơ sở là một chất nhận proton. Histidine có thể hoạt động như cả hai. Nhưng không phải axit và bazơ có cực không? Câu trả lời mơ hồ và có lẽ đáng thất vọng là tất cả chỉ là tương đối. Cụ thể hơn, tất cả đều liên quan đến pH sinh lý (khoảng 7). Chuỗi bên của axit amin có thể được gán một giá trị được gọi là pKa, cho chúng ta biết liệu chúng hoạt động như một axit hay như một bazơ. Nếu pKa của chuỗi bên axit amin cao hơn pH sinh lý thì đó là một bazơ. Nếu pKa của chuỗi bên axit amin thấp hơn pH sinh lý thì đó là axit. Chuỗi bên của Histidine có giá trị pKa gần với pH sinh lý, có nghĩa là nó được cung cấp linh hoạt trong việc cung cấp và chấp nhận proton.
Một tính năng thú vị thứ hai của histidine (và một đặc điểm vô giá đối với nghiên cứu sinh học) là khả năng liên kết với kim loại, đặc biệt là kẽm. Các nhóm nghiên cứu khác nhau chỉ quan tâm đến một loại protein và vì vậy họ có thể muốn phân lập protein vật nuôi của họ để nghiên cứu kỹ hơn. Một cách để làm điều này là thay đổi gen mã hóa protein với mục đích kết hợp một số gốc histidine ở đầu cuối của protein. Vì những lý do có thể tự giải thích, đây được gọi là đuôi poly-histidine. Tế bào sản xuất ra loại protein này cũng sẽ sản xuất ra nhiều loại protein khác. Các tế bào này có thể bị phá vỡ mở ra và chất ly giải đi qua cột mà kẽm được gắn vào. Do ái lực của kẽm với histidine, protein mục tiêu sẽ vẫn ở trong cột trong khi các protein khác bị rửa trôi.