“Năng lượng liên kết là năng lượng cần thiết để ..(1)... một liên kết hóa học trong phân tử ở thể ..(2)... thành nguyên tử ở thể khí.” Từ/cụm từ thích hợp để điền vào (1) và (2) lần lượt là
Bộ Đề Kiểm Tra Tham Khảo Học Kì 1 - Môn Hoá 10 - Kết Nối Tri Thức Với Cuộc Sống là một tài liệu ôn tập được xây dựng nhằm đánh giá kiến thức và kỹ năng của học sinh theo chương trình "Kết nối tri thức với cuộc sống". Đề thi bao gồm các dạng bài tập đa dạng như: trắc nghiệm, tự luận tập trung vào các chủ đề đã học trong học kỳ 1. Đề thi giúp học sinh rèn luyện tư duy logic, kỹ năng tính toán và củng cố kiến thức để chuẩn bị tốt cho bài kiểm tra chính thức.
Câu hỏi liên quan
Freon-12 \(\left(\mathrm{CCl}_{2} \mathrm{F}_{2}\right)\) là một hợp chất thuộc nhóm CFC , được sử dụng rộng rãi làm chất làm lạnh. Tuy nhiên, việc sử dụng Freon-12 ngày càng bị hạn chế do khi thoát ra khí quyển, nó gây phá hủy tầng ozone. Phản ứng tổng hợp Freon-12 diễn ra theo phương trình:
\(\mathrm{CH}_{4}(\mathrm{g})+2 \mathrm{Cl}_{2}(\mathrm{g})+2 \mathrm{F}_{2}(\mathrm{g}) \rightarrow \mathrm{CF}_{2} \mathrm{Cl}_{2}(\mathrm{g})+2 \mathrm{HF}(\mathrm{g})+2 \mathrm{HCl}(\mathrm{g})(*)\)
Cho biết:
Liên kết
C-H
Cl-Cl
F-F
C-F
C-Cl
H-F
H-Cl
Eb (kJ/mol)
413
239
154
485
339
565
427
\(\Delta_{\mathrm{r}} \mathrm{H}_{298}{ }^{0}\) của phản ứng \((*)\) đã cho là
Cho phản ứng hóa học: \(\mathrm{CO}_{2}(\mathrm{~g}) \longrightarrow \mathrm{CO}(\mathrm{g})+\frac{1}{2} \mathrm{O}_{2}\) và các dữ kiện:
Biến thiên năng lượng tự do Gibbs chuẩn của phản ứng trên ở \(25^{\circ} \mathrm{C}\) là bao nhiêu?. (làm tròn đến hàng đơn vị)
Quá trình nào sau đây là phản ứng thu nhiệt?
Năm 2024, các nhà khoa học Trung Quốc đã thiết kế hệ thống để thu giữ khí \(\mathrm{CO}_{2}\) và sản xuất khí \(\mathrm{H}_{2}\), hệ thống này được minh họa trong hình dưới đây:
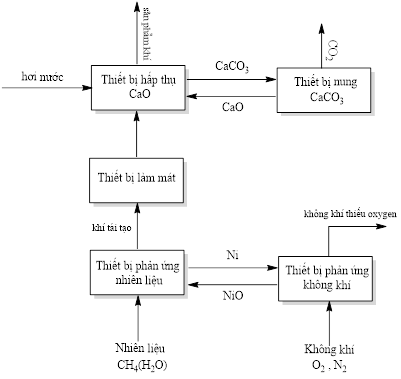
Cho các phát biểu sau:
Xét phản ứng sau:
\(\mathrm{SO}_{2}(\mathrm{g})+\mathrm{O}_{2}(\mathrm{g}) \rightarrow \mathrm{SO}_{3}(\mathrm{l})\)
Biết nhiệt tạo thành của \(\mathrm{SO}_{2}(\mathrm{g})\) là \(-296,8 \mathrm{kJ} / \mathrm{mol}^{2}\) và \(\mathrm{SO}_{3}(\mathrm{l})\) là \(-441,0 \mathrm{kJ} / \mathrm{mol}\). Tính biến thiên enthalpy của phản ứng ở điều kiện chuẩn (theo \(\mathrm{kJ} / \mathrm{mol}\), làm tròn kết quả đến chũ số hàng đơn vị).
Nhiệt nhôm là phản ứng giữa nhôm và oxide sắt \(\left(\mathrm{Fe}_{2} \mathrm{O}_{3}\right)\) nhằm tách sắt nguyên chất ra khỏi quặng. Phản ứng này tạo ra một lượng nhiệt rất lớn.
\(2 \mathrm{Al}(\mathrm{s})+\mathrm{Fe}_{2} \mathrm{O}_{3}(\mathrm{s}) \rightarrow \mathrm{Al}_{2} \mathrm{O}_{3}(\mathrm{s})+2 \mathrm{Fe}(\mathrm{s})\)
Biết nhiệt tạo thành của \(\mathrm{Fe}_{2} \mathrm{O}_{3}\) và \(\mathrm{Al}_{2} \mathrm{O}_{3}\) lần lượt là \(-824,2 \mathrm{kJ} / \mathrm{mol}\) và \(-1675,7 \mathrm{kJ} / \mathrm{mol}\). Giá trị biến thiên enthalpy của phản ứng nhiệt nhôm là
Cho quá trình phản ứng dưới dạng hình ảnh như sau:
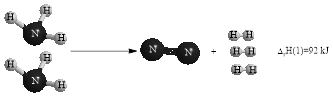
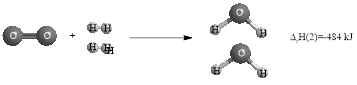
Các chất trong hình đều ở trạng thái khí.
Hãy tính biến thiên enthalpy của phản ứng sau đây: \(2 \mathrm{N}_{2(\mathrm{g})}+6 \mathrm{H}_{2} \mathrm{O}_{(\mathrm{g})} \longrightarrow 3 \mathrm{O}_{2(\mathrm{g})}+4 \mathrm{NH}_{3(\mathrm{g})} \Delta_{\mathrm{r}} \mathrm{H}(3)\)
Cho sơ đồ mô tả enthalpy sau:
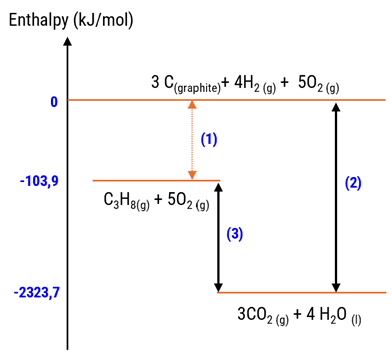
Cho các phát biểu sau:
Ethanol \(\left(\mathrm{C}_{2} \mathrm{H}_{5} \mathrm{OH}\right)\) là một loại nhiên liệu sinh học được sử dụng phổ biến. Khi cháy hoàn toàn, ethanol tạo ra \(\mathrm{CO}_{2}\) và \(\mathrm{H}_{2} \mathrm{O}\). Ngoài ra, trong một số quá trình công nghiệp, CO có thể bị oxi hóa thành \(\mathrm{CO}_{2}\). Cho hai phản ứng sau:
(1) \(\mathrm{C}_{2} \mathrm{H}_{5} \mathrm{OH}(\mathrm{l})+3 \mathrm{O}_{2}(\mathrm{g}) \rightarrow 2 \mathrm{CO}_{2}(\mathrm{g})+3 \mathrm{H}_{2} \mathrm{O}(\mathrm{l})\)
(2) \(\mathrm{CO}(\mathrm{g})+1 / 2 \mathrm{O}_{2}(\mathrm{g}) \rightarrow \mathrm{CO}_{2}(\mathrm{g})\)
Cho bảng số liệu nhiệt động học chuẩn ở 298K:
Hợp chất
C₂H₅OH(l)
CO(g)
CO₂(g)
H₂O(l)
(kJ/mol)
-277,0
-110,5
-393,5
-285,8
S° (J/mol·K)
160,7
197,6
213,6
69,9
Tổng giá trị \(\Delta \mathrm{G}_{1}+\Delta \mathrm{G}_{2}\) của hai phản ứng trên là bao nhiêu ? Biết công thức tính \(\Delta \mathrm{G}=\Delta \mathrm{H}-\mathrm{T} \Delta \mathrm{S}(\mathrm{kJ} / \mathrm{mol})\) (làm tròn đến số nguyên )
Cho vòng tròn năng lượng như sau:
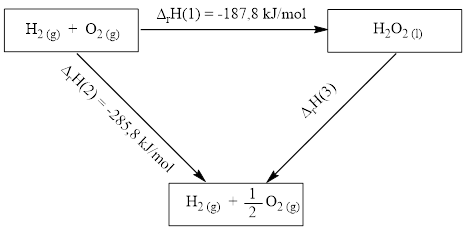
Tính giá trị của \(\Delta_{\mathrm{r}} \mathrm{H}(3)\)?
Cho giản đồ năng lượng của phản ứng \(\mathrm{C}_{2} \mathrm{H}_{5} \mathrm{Cl} \longrightarrow \mathrm{C}_{2} \mathrm{H}_{4}+\mathrm{HCl}\) như sau:
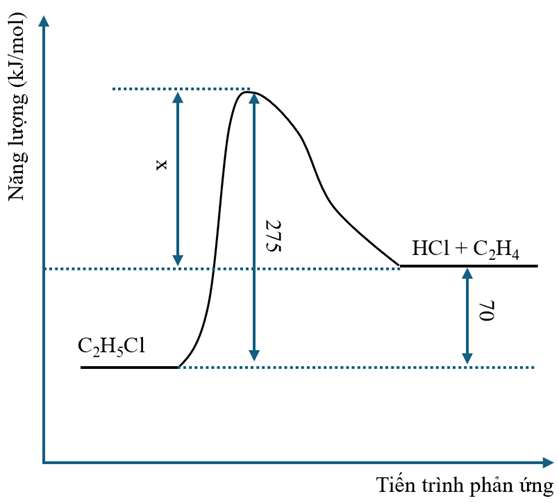
Phản ứng giữa ethane và chlorine tạo ra ethyl chloride và khí hydrogen chloride là phản ứng tỏa nhiệt. Phương trình phản ứng:
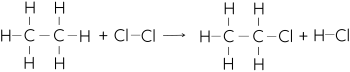
Cho biết năng lượng của một số liên kết như sau:
Liên kết
Năng lượng liên kết (kJ/mol)
C-Cl
+340
C-C
+350
C-H
+410
Cl-Cl
+240
H-Cl
+430
Biến thiên enthalpy chuẩn của phản ứng trên là bao nhiêu \(\mathrm{kJ} / \mathrm{mol}\) (làm tròn kết quả đến chư số hàng đơn vị)?
Phương trình phản ứng giữa hydrogen và chlorine tạo ra hydrogen chloride được biểu diễn như sau:
\(Cl_2+ H_2\ \rightarrow 2HCl\) với \(\Delta_{r} H_{298}^{o}=-184 \mathrm{kJ} / \mathrm{mol}\)
Bảng dưới đây cho biết năng lượng của một số liên kết tham gia trong phản ứng.
Liên kết
Năng lượng liên kết (kJ/mol)
H-Cl
+430
H-H
+436
Cl-Cl
?
Năng lượng của liên kết \(\mathrm{Cl}-\mathrm{Cl}\) là
Cho sơ đồ:
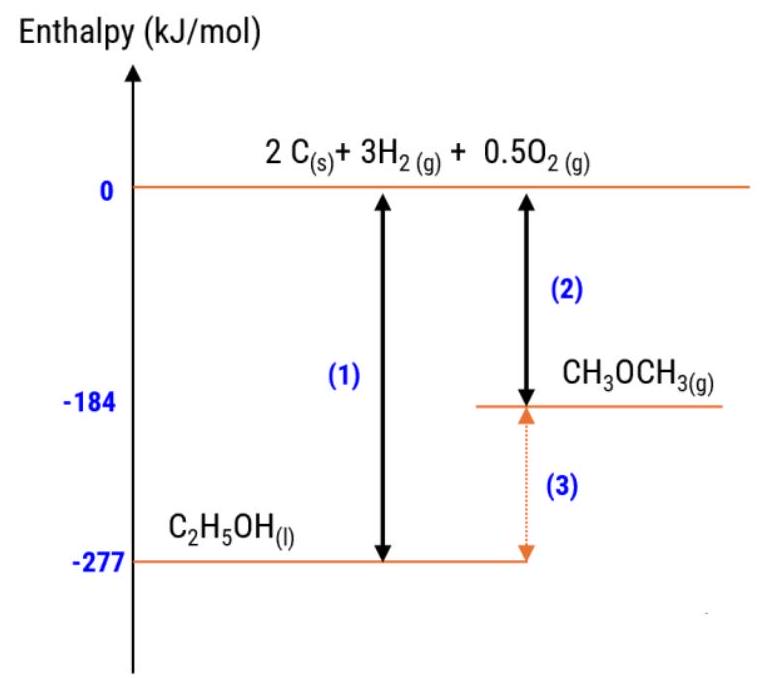
Sự tạo thành \(1,5 \mathrm{mol}\) nước lỏng tỏa ra nhiệt lượng là \(428,76 \mathrm{kJ}\).
\(H_2\left(g\right)+\frac12O_2\left(g\right)\rightarrow H_2O\left(l\right)\)
Biến thiên enthalpy của phản ứng trên là bao nhiêu?
Tính entanpy tạo thành \(\left(\Delta_{\mathrm{f}} \mathrm{H}_{298}^{\rho}\right)\) của acetaldehyde \(\left(\mathrm{CH}_{3} \mathrm{CHO}\right)\) : Cho các dữ kiện như sau:
\(\mathrm{H}_{2(\mathrm{~g})}+\frac{1}{2} \mathrm{O}_{2(\mathrm{~g})} \longrightarrow \mathrm{H}_{2} \mathrm{O}_{(\mathrm{l})} \quad \Delta_{\mathrm{f}} \mathrm{H}_{298}^{\rho}=-286 \mathrm{~kJ} / \mathrm{mol} \tag{1}\)
\(\mathrm{C}(\mathrm{s})+\mathrm{O}_{2(\mathrm{~g})} \longrightarrow \mathrm{CO}_{2}(\mathrm{~g}) \quad \Delta_{\mathrm{f}} \mathrm{H}_{298}^{\rho}=-394 \mathrm{~kJ} / \mathrm{mol} \tag{2}\)
\(2 \mathrm{CH}_{3} \mathrm{CHO}_{(\mathrm{g})}+5 \mathrm{O}_{2(\mathrm{~g})} \longrightarrow 4 \mathrm{H}_{2} \mathrm{O}_{(\mathrm{l})}+4 \mathrm{CO}_{2(\mathrm{~g})} \quad \Delta_{\mathrm{r}} \mathrm{H}_{298}^{\rho_{2}}=-2388 \mathrm{~kJ} / \mathrm{mol} \tag{3}\)
Trong các quá trình sau, quá trình nào hấp thụ nhiệt từ môi trường?
Quá trình hình thành nitrogen dioxide gồm 2 bước:
Bước 1: \(\mathrm{N}_{2}+\mathrm{O}_{2} \rightarrow 2 \mathrm{NO}\)
Bước 2: \(2 \mathrm{NO}+\mathrm{O}_{2} \rightarrow 2 \mathrm{NO}_{2}\)
Phản ứng tổng thể: \(\mathrm{N}_{2}+2 \mathrm{O}_{2} \rightarrow 2 \mathrm{NO}_{2}\)
Biết biến thiên enthalpy của phản ứng tổng thể là \(+68 \mathrm{kJ} / \mathrm{mol}\).
Biến thiên enthalpy \((\Delta \mathrm{H})\) có giá trị âm đối với loại phản ứng nào sau đây?
Cho chu trình enthalpy sau:
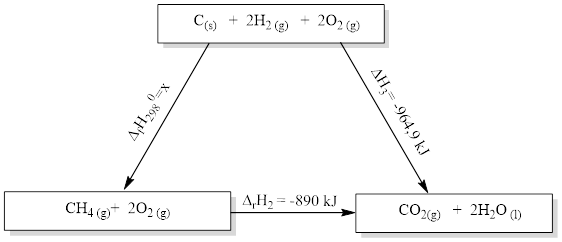
Giá trị của x là















