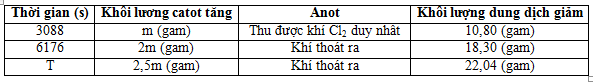
Tiến hành điện phân dung dịch CuSO4 và NaCl bằng điện cực trơ, màng ngăn xốp với cường độ dòng điện không đổi, ta có kết quả ghi theo bảng sau:
Giá trị của t là :
Hãy suy nghĩ và trả lời câu hỏi trước khi xem đáp án
Lời giải:
Báo sai- Gọi a là số mol của NaCl. Quá trình điện phân xảy ra như sau:
|
Thời gian (s) |
Tại catot |
Tại anot |
|
t = 3088 ne = 2x |
Cu2+ + 2e → Cu x 2x x |
2Cl- → 2e + Cl2 2x 2x x |
|
t = 6176 ne = 4x = 0,32 |
Cu2+ + 2e → Cu 0,16 0,32 0,16
|
2Cl- → 2e + Cl2 a → 0,5a 2H2O → 4e + 4H+ + O2 0,32 - a → 0,08 - 0,25a |
|
t = ? |
Cu2+ + 2e → Cu 0,2 0,4 0,2 2H2O + 2e → 2OH- + H2 2y y |
2Cl- → 2e + Cl2 0,2 0,2 0,1 2H2O → 4e + 4H+ + O2 2a (0,4 + 2y) - 0,2 → 0,5y + 0,05 |
- Tại thời điểm t = 3088 có: \({m_{dd{\rm{ giam}}}} = 64{n_{Cu}} + 71{n_{C{l_2}}} \Rightarrow 135x = 10,8 \Rightarrow x = 0,06\;mol\)
- Tại thời điểm t = 6176 (s) có: \({m_{dd{\rm{ giam}}}} = 64{n_{Cu}} + 71{n_{C{l_2}}} + 32{n_{{O_2}}} = 18,3 \Rightarrow a = 0,2\;mol\)
- Tại thời điểm t (s) có:\({m_{dd{\rm{ giam}}}} = 64{n_{Cu}} + 71{n_{C{l_2}}} + 32{n_{{O_2}}} + 2{n_{{H_2}}} = 22,04 \Rightarrow y = 0,03\;mol\)
\(\Rightarrow {n_{e{\rm{(trao doi)}}}} = 2{n_{Cu}} + 2{n_{{H_2}}} = 2.0,2 + 2.0,03 = 0,46\;mol \Rightarrow t = \frac{{0,46}}{{0,16}}.3088 = 8878s\)
Đề thi thử THPT QG môn Hóa học năm 2018
Trường THPT Nguyễn Đình Chiểu - Bến Tre