Ion nào sau đây có tính oxi hoá mạnh nhất ở điều kiện chuẩn?
Tuyển Tập Đề Thi Tham Khảo Tốt Nghiệp THPT Năm 2025 - Hóa Học - Bộ Đề 05 được biên soạn theo định hướng mới nhất của kỳ thi tốt nghiệp THPT. Mỗi đề đều có cấu trúc ba phần: trắc nghiệm nhiều lựa chọn, trắc nghiệm đúng – sai, và trắc nghiệm trả lời ngắn, kết hợp cùng hệ thống câu hỏi đa dạng, phân hóa rõ rệt theo các mức độ nhận thức từ cơ bản đến nâng cao. Điểm nổi bật của bộ đề là các câu hỏi bám sát thực tế giảng dạy, đề cập đến nhiều chủ đề quen thuộc như hợp chất hữu cơ, amino acid – protein, ester, polymer, ăn mòn kim loại, phản ứng điện hóa, cân bằng hóa học, chất điện li và môi trường. Mỗi đề đều có đáp án và hướng dẫn giải chi tiết, giúp học sinh tự ôn tập, rèn kỹ năng giải nhanh và nắm vững bản chất kiến thức. Đây là tài liệu ôn luyện lý tưởng giúp học sinh lớp 12 hệ thống hóa kiến thức toàn diện và sẵn sàng bước vào kỳ thi quan trọng với sự tự tin cao nhất.
Câu hỏi liên quan
Chromium có số oxi hóa là +3 trong hợp chất nào sau đây?
Cho biết giá trị thế điện cực chuẩn của các cặp oxi hoá – khử sau:
Số kim loại trong dãy các kim loại Zn, Ni, Fe, Cu phản ứng được với dung dịch HCl ở điều kiện chuẩn là
Xét phản ứng sau:
\(\mathrm{Fe}_{2} \mathrm{O}_{3}+3 \mathrm{CO} \rightarrow 2 \mathrm{Fe}+3 \mathrm{CO}_{2}\)
Phương trình biểu diễn quá trình khử của phản ứng trên là
Muối Mohr có công thức \(\left(\mathrm{NH}_{4}\right)_{2} \mathrm{Fe}\left(\mathrm{SO}_{4}\right)_{2} \cdot 6 \mathrm{H}_{2} \mathrm{O}\). Để xác định độ tinh khiết của một loại muối Mohr (cho rằng trong muối Mohr chỉ có muối kép ngậm nước nêu trên và tạp chất trơ), một học sinh tiến hành các thí nghiệm sau: Cân chính xác 7,237 gam muối Mohr, pha thành 100 mL dung dịch X. Lấy chính xác 10 mL dung dịch X , thêm 10 mL dung dịch \(\mathrm{H}_{2} \mathrm{SO}_{4} 10 \%\), được dung dịch Y. Chuẩn độ dung dịch Y bằng dung dịch chuẩn \(\mathrm{KMnO}_{4} 0,023 \mathrm{M}\). Thực hiện chuẩn độ 3 lần.
Kết quả đạt được như sau:
Lần chuẩn độ
1
2
3
Thể tích dung dịch KMnO4 (mL)
16,0
16,1
16,0
Cho các phát biểu sau:
Nối dung dịch sodium chloride với nguồn điện và một bóng đèn nhỏ. Quan sát thấy bóng đèn
Xét phản ứng sau: \(3 \mathrm{HCl}+\mathrm{HNO}_{3} \rightarrow \mathrm{Cl}_{2}+\mathrm{NOCl}+2 \mathrm{H}_{2} \mathrm{O}\) Chất khử trong phản ứng trên là
Theo QCVN 01-1:2018/BYT, hàm lượng manganese (Mn) tối đa cho phép trong nước sinh hoạt không được vượt quá \(0,3 \mathrm{mg} / \mathrm{L}\). Một mẫu nước chứa \(\mathrm{Mn}^{2+}\) với nồng độ chưa xác định. Để đánh giá hàm lượng manganese trong \(5 \mathrm{m}^{3}\) mẫu nước trên, người ta tiến hành tách loại manganese bằng cách sử dụng 50 gam \(\mathrm{KMnO}_{4}\) để oxy hóa toàn bộ \(\mathrm{Mn}^{2+}\) thành \(\mathrm{MnO}_{2}\) kết tủa theo phản ứng:
\(3 \mathrm{Mn}^{2+}+2 \mathrm{MnO}_{4}^{-}+2 \mathrm{H}_{2} \mathrm{O} \rightarrow 5 \mathrm{MnO}_{2}+4 \mathrm{H}^{+}\)
Biết rằng phản ứng xảy ra hoàn toàn và toàn bộ \(\mathrm{MnO}_{2}\) được loại bỏ. Hàm lượng manganese trong mẫu nước này cao gấp bao nhiêu lần so với ngưỡng cho phép? (Làm tròn kết quả đến hàng đơn vị)
Nồng độ ion \(\mathrm{NO}_{3}{ }^{-}\)trong nước uống tối đa cho phép là 9 ppm (part per million - phần triệu). Nếu thừa ion này sẽ gây ra một loại bệnh thiếu máu hoặc tạo thành nitrosamin (một hợp chất gây ung thư đường tiêu hóa). Để xác định hàm lượng ion \(\mathrm{NO}_{3}{ }^{-}\)trong 200 mL nước người ta dùng các hoá chất ( \(\mathrm{Cu}+\mathrm{H}_{2} \mathrm{SO}_{4}\) loãng) thấy cần dùng đến \(1,92 \mathrm{mg} \mathrm{Cu}\). Hàm lượng \(\mathrm{NO}_{3}{ }^{-}\)trong mẫu nước trên là bao nhiêu?
Theo lý thuyết công thức của quặng pyrite là \(\mathrm{FeS}_{2}\). Thực tế một phân ion disulfide \(\mathrm{S}_{2}{ }^{-}\)bị thay thế bởi ion sulfide \(\left(\mathrm{S}^{2-}\right)\) nên coi pyrite như một hỗn hợp của \(\mathrm{FeS}_{2}\) và FeS. Như vậy, công thức tổng quát của pyrite có thể biểu diễn là \(\mathrm{FeS}_{\mathrm{x}}\) ). Khi xử lí m gam một mẫu pyrite (chỉ gồm \(\mathrm{FeS}_{2}\) và FeS ) bằng bromine trong dung dịch KOH dư người ta thu được kết tủa nâu đỏ A và dung dịch B. Nung kết tủa A đến khối lượng không đổi thu được 0,4 gam chất rắn. Thêm lượng dư dung dịch \(\mathrm{BaCl}_{2}\) vào dung dịch B thì thu được 2,2174 gam kết tủa trắng không tan trong acid. Xác định giá trị x trong công thức tổng quát \(\mathrm{FeS}_{\mathrm{x}}\) của quặng pyrite.
Nhiệt luyện thép chính là quá trình điều chế sắt từ quặng hematite bằng cách khử oxide của sắt ở nhiệt độ cao trong lò luyện kim.
Phản ứng xảy ra như sau: \(\mathrm{Fe}_{2} \mathrm{O}_{3}+\mathrm{xCO} \rightarrow \mathrm{yFe}+\mathrm{zCO}_{2}\)
Các vụ hỏa hoạn ở các chung cư và nhà cao tầng hiện đang xảy ra liên tục với quy mô và mức độ tổn thất ngày càng cao. Các nạn nhân bị tử vong trong các vụ hỏa hoạn có thể do ngạt khí, bỏng nhiệt, nhảy từ trên cao xuống đất, bị vật nặng đè, giẫm đạp,... và số người chết thường không tập trung nhiều ở tâm đám cháy mà thường tập trung nhiều ở những nơi tích tụ khói hoặc có luồng khói đi qua. Khói từ đám cháy chứa các khí độc như carbon monoxide \((\mathrm{CO})\), hydrogen cyanide \((\mathrm{HCN})\) và các khí gây kích ứng khác.
Cho các phát biểu sau :
Potassium dichromate \(\left(\mathrm{K}_{2} \mathrm{Cr}_{2} \mathrm{O}_{7}\right)\) có thể được sử dụng để phát hiện nồng độ còn trong hơi thở. Phương trình phản ứng của alcohol và \(\mathrm{K}_{2} \mathrm{Cr}_{2} \mathrm{O}_{7}\) như sau:
\(3 \mathrm{CH}_{3} \mathrm{CH}_{2} \mathrm{OH}+2 \mathrm{Cr}_{2} \mathrm{O}_{7}{ }^{2-}+16 \mathrm{H}^{+} \longrightarrow 3 \mathrm{CH}_{3} \mathrm{COOH}+4 \mathrm{Cr}^{3+}+11 \mathrm{H}_{2} \mathrm{O}\)
Sau phản ứng, màu sắc chuyển từ cam sang xanh lục, dữ liệu đo được bằng thiết bị có thể chuyển đổi thành nồng độ cồn. Ở nhiệt độ và áp suất bình thường, tỷ lệ nồng độ cồn trong máu ( \(\mathrm{mg} / \mathrm{L}\) ) so với nồng độ cồn trong hơi thở \((\mathrm{mg} / \mathrm{L})\) hiện đang là 2100 : 1. Theo luật quy định, nồng độ cồn trong mỗi lít hơi thở không được vượt quá \(0,25 \mathrm{mg}\). Cho đồ thị thể hiện mối quan hệ giữa nồng độ cồn trong hơi thở và chỉ số đo bằng thiết bị như sau:
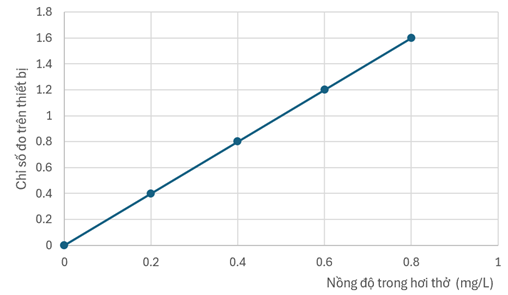
Khi chỉ số của thiết bị đo hơi thở của một người là 0,80 thì nồng độ cồn trong máu ( \(\mathrm{mmol} / \mathrm{L}\) ) của người đó là bao nhiêu? (làm tròn đáp án đến hàng đơn vị).
Trong phương pháp phân tích nhiệt, một chất rắn khối lượng \(\mathrm{m}_{1}\) được gia nhiệt, thu được chất rắn mới khối lượng \(\mathrm{m}_{2}\) (khối lượng \(\mathrm{m}_{2}\) thay đổi theo từng giai đoạn phản ứng) và chất khí hoặc hơi. Giản đồ phân tích nhiệt hình bên cho biết sự biến đổi khối lượng của calcium oxalate ngậm nước \(\mathrm{CaC}_{2} \mathrm{O}_{4} . \mathrm{H}_{2} \mathrm{O}\) trong môi trường khí trơ theo nhiệt độ: trục tung biểu thị phần trăm khối lượng chất rắn còn lại so với khối lượng ban đầu (\%); trục hoành biểu thị nhiệt độ nung.
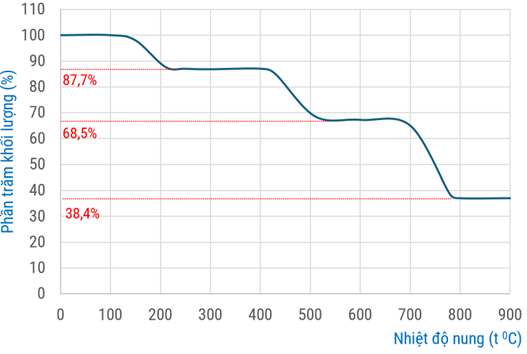
Cho các phương trình hóa học (theo đúng tỷ lệ mol) ứng với ba giai đoạn phản ứng có kèm theo thay đổi khối lượng của các chất rắn như sau:
(1) \(\mathrm{CaC}_{2} \mathrm{O}_{4} . \mathrm{H}_{2} \mathrm{O} \xrightarrow{\text { nung } 200^{\circ} \mathrm{C}} \mathrm{X}_{1(\mathrm{s})}+\mathrm{Y}_{1(\mathrm{g})}\)
(2) \(X_{1(\mathrm{s})} \xrightarrow{\text { nung } 510^{\circ} \mathrm{C}} X_{2(\mathrm{s})}+Y_{2(\mathrm{g})}\)
(3) \(\mathrm{X}_{2(\mathrm{s})} \xrightarrow{\text { nung } 780^{\circ} \mathrm{C}} \mathrm{X}_{3(\mathrm{s})}+\mathrm{Y}_{3(\mathrm{g})}\)
Phân tử khối của \(Y_{3}\) bằng bao nhiêu?
Có nhiều vụ tai nạn giao thông xảy ra do người lái xe uống rượu. Người ta có thể xác định hàm lượng ethanol bằng xét nghiệm máu hoặc đo hơi thở bằng máy đo (có chứa hỗn hợp \(\mathrm{K}_{2} \mathrm{Cr}_{2} \mathrm{O}_{7}\) và \(\mathrm{H}_{2} \mathrm{SO}_{4}\) ) theo phương trình như sau:
\(\mathrm{CH}_{3} \mathrm{CH}_{2} \mathrm{OH}+\mathrm{K}_{2} \mathrm{Cr}_{2} \mathrm{O}_{7}+\mathrm{H}_{2} \mathrm{SO}_{4} \rightarrow \mathrm{CH}_{3} \mathrm{COOH}+\mathrm{Cr}_{2}\left(\mathrm{SO}_{4}\right)_{3}+\mathrm{K}_{2} \mathrm{SO}_{4}+\mathrm{H}_{2} \mathrm{O}\)
Khi chuẩn độ 25,0 gam huyết tương máu của một người lái xe cần dùng \(20,0 \mathrm{~mL}\) dung dịch \(\mathrm{K}_{2} \mathrm{Cr}_{2} \mathrm{O}_{7} 0,010 \mathrm{M}\). Nồng độ phần trăm ethanol trong 25 gam huyết tương máu của một người lái xe là
Cho sơ đồ phản ứng sau (biết \(\mathrm{A}),(\mathrm{Z})\) là kim loại, muối \(\mathrm{C})\) có màu xanh, \(\mathrm{G})\) là phi kim):
(1) \(\mathrm{A})+(\mathrm{B}) \longrightarrow(\mathrm{C})+(\mathrm{D}) \uparrow+(\mathrm{E})\)
(2) \(\mathrm{D})+(\mathrm{E})+(\mathrm{G}) \longrightarrow(\mathrm{B})+(\mathrm{X})\)
(3) \(\mathrm{BaCl}_{2}+(\mathrm{C}) \longrightarrow(\mathrm{Y})+\mathrm{BaSO}_{4}\)
(4) \(\mathrm{Z})+(\mathrm{Y}) \longrightarrow(\mathrm{T})+(\mathrm{A})\)
(5) \(\mathrm{T})+(\mathrm{G}) \longrightarrow \mathrm{FeCl}_{3}\)
Tỉ lệ số nguyên tử trong \(\mathrm{D})\) và số nguyên tử trong \((\mathrm{Y})\) là
Trong danh mục tiêu chuẩn chất lượng sản phẩm có chỉ tiêu về dư lượng chlorine không vượt quá 1 \(\mathrm{mg} / \mathrm{L}\) (chlorine sử dụng trong quá trình sơ chế nguyên liệu để diệt vi sinh vật).
Phương pháp chuẩn độ iodine-thiosulfate được dùng để xác định dư lượng chlorine trong thực phẩm theo phương trình: \(\mathrm{Cl}_{2}+2 \mathrm{KI} \longrightarrow \mathrm{KCl}+\mathrm{I}_{2}\).
Lượng \(\mathrm{I}_{2}\) sau đó được được nhận biết bằng hồ tinh bột, \(\mathrm{I}_{2}\) bị khử bởi dung dịch chuẩn sodium thiosul \(\mathfrak{f}\) ate theo phương trình: \(\mathrm{I}_{2}+2 \mathrm{Na}_{2} \mathrm{~S}_{2} \mathrm{O}_{3} \longrightarrow 2 \mathrm{NaI}+\mathrm{Na}_{2} \mathrm{~S}_{4} \mathrm{O}_{6}\).
Dựa vào thể tích dung dịch \(\mathrm{Na}_{2} \mathrm{~S}_{2} \mathrm{O}_{3}\) đã phản ứng, tính được dư lượng chlorine trong dung dịch mẫu. Tiến hành chuẩn độ 100 mL dung dịch mẫu bằng dung dịch \(\mathrm{Na}_{2} \mathrm{~S}_{2} \mathrm{O}_{3}\) 0,01 M thì thể tích \(\mathrm{Na}_{2} \mathrm{~S}_{2} \mathrm{O}_{3}\) đã dùng trong lần chuẩn độ lần lượt như sau:
(dụng cụ chứa dung dịch chuẩn \(\mathrm{Na}_{2} \mathrm{~S}_{2} \mathrm{O}_{3}\) là loại buret 25 mL , vạch chia \(0,1 \mathrm{~mL}\) ). Tính lượng \(\mathrm{Cl}_{2}\) trong mẫu sản phẩm trên.
Tiến hành thí nghiệm theo các bước sau:
Bước 1: Lấy vào ống nghiệm (1) \(0,5 \mathrm{mL}\) dung dịch \(\mathrm{HNO}_{3}\) đặc (68%)
ống nghiệm (2) \(0,5 \mathrm{mL}\) dung dịch HCl đặc.
Bước 2: Cho vào mỗi ống nghiệm một mảnh nhỏ đồng kim loại. Nút các ống nghiệm bằng bông tẩm dung dịch NaOH. Đun nhệ ống nghiệm thứ hai.
Cho các phát biểu sau:
(a) Ở ống nghiệm (1), mảnh đồng tan dần, dung dịch chuyển sang màu xanh.
(b) Ở ống nghiệm thứ hai, thấy có khí không màu, không hóa nâu thoát ra khỏi dung dịch.
(c) Bông tẩm dung dịch NaOH có tác dụng hạn chế khí độc thoát ra khỏi ống nghiệm.
(d) Có thể thay bông tẩm dung dịch NaOH bằng bông tẩm dung dịch NaCl.
Số phát biểu đúng là
Để dập tắt các đám cháy do xăng dầu gây ra, người ta dùng cát hoặc bột chữa cháy \(\mathrm{MAP}\left(\mathrm{NH}_{4} \mathrm{H}_{2} \mathrm{PO}_{4}\right)\) mà không dùng nước. Cho các phát biểu sau:
(a) Xăng dầu nhẹ hơn nước và không tan trong nước nên nếu dùng nước xăng dầu sẽ nổi lên trên làm cho càng dễ cháy hơn.
(b) Cát hoặc bột chữa cháy MAP có tác dụng tạo lớp phủ bề mặt ngăn xăng dầu tiếp xúc với oxygen trong không khí.
(c) Quá trình nước bay hơi là quá trình tỏa nhiệt nên đám cháy xảy ra càng mạnh.
(d) Cát hoặc bột chữa cháy MAP hấp thụ nhiệt nên làm giảm nhiệt độ ngăn cản đám cháy.
Có bao nhiêu phát biểu sai?
Sự cố tràn dầu thường xảy ra trong các hoạt động tìm kiếm, thăm dò, khai thác, vận chuyển, chế biến, phân phối và tàng trữ dầu khí và các sản phẩm của chúng. Ví dụ: các hiện tượng rò rỉ, phụt dầu, vỡ đường ống, vỡ bể chứa, tai nạn đâm và gây thủng tàu, sự cố tại các khoan dầu khí, nhà máy lọc hóa dầu ….
Ở Hình 9.6, Hình 9.7 và Hình 9.8 là các cách xử lý do sự cố tràn dầu. Hiện nay các nước sử dụng giải pháp nào có hiệu quả để hạn chế sự lan ra xung quanh của dầu khi xảy ra sự cố tràn dầu trên mặt biển?
Khi xảy ra phản ứng hóa học, lượng chất đầu biến đổi như thế nào?















