Trong quá trình điện phân, \(1 \mathrm{mol} \ \mathrm{Cr}^{3+}\) được điện phân cần bao nhiêu mol electron?
Tuyển Tập Đề Thi Tham Khảo Tốt Nghiệp THPT Năm 2025 - Hóa Học - Bộ Đề 06 giúp học sinh lớp 12 ôn tập hiệu quả và tự tin bước vào kỳ thi Tốt nghiệp THPT năm 2025. Mỗi đề thi trong tài liệu được xây dựng theo đúng cấu trúc chuẩn của Bộ Giáo dục và Đào tạo, bao gồm ba phần: trắc nghiệm nhiều lựa chọn, trắc nghiệm đúng – sai và trắc nghiệm trả lời ngắn. Các câu hỏi được chọn lọc kỹ lưỡng, bám sát nội dung chương trình, tích hợp kiến thức liên môn và có độ phân hóa phù hợp, giúp học sinh không chỉ ôn tập lý thuyết mà còn rèn luyện kỹ năng giải đề thực tiễn. Đặc biệt, phần đáp án và hướng dẫn giải chi tiết đi kèm giúp học sinh dễ dàng tự đánh giá kết quả và nhận diện các dạng bài quan trọng.
Câu hỏi liên quan
Một chiếc khuyên tai dạng đĩa tròn mỏng có đường kính \(5,00 \mathrm{cm}\) được mạ với lớp phủ Au dày 0,02 mm từ dung dịch \(\mathrm{Au}^{3+}\).
Cho:
- Khối lượng riêng của Au là \(\mathrm{D}=19,7 \mathrm{g} / \mathrm{cm}^{3}, \pi=3,14\).
- \(\mathrm{F}=96500 \mathrm{C} / \mathrm{mol} ; \mathrm{I}=0,10 \mathrm{A}\).
Thời gian để mạ vàng cho chiếc khuyên tai là bao nhiêu giờ? (làm tròn đến hàng phần trăm)
Trong quá trình mạ điện, một kỹ thuật viên nhúng một tấm zinc (Zn) có khối lượng 15,625 gam vào 300 mL dung dịch \(\mathrm{CuSO}_{4} 0,2 \mathrm{M}\). Sau một thời gian, lấy tấm Zn ra, rửa sạch, sấy khô và cân lại thấy khối lượng là 15,615 gam. Khối lượng Cu bám vào tấm Zn là bao nhiêu gam? (Giả sử toàn tộ lượng Cu sinh ra đều bám hết vào thanh Zn ).
Trong công nghiệp, kim loại Mg được sản xuất từ quặng Carnallite \(\mathrm{KCl} . \mathrm{MgCl}_{2} . 6 \mathrm{H}_{2} \mathrm{O}\) bằng phương pháp điện phân nóng chảy \(\mathrm{MgCl}_{2}\) (đã được tách từ quặng). Quá trình điện phân diễn ra trong điều kiện không có không khí, với điện cực than chì. Ở cathode thu được kim loại Mg , còn ở anode chỉ sinh ra khí \(\mathrm{Cl}_{2}\). Giả sử khí \(\mathrm{Cl}_{2}\) thu được có thể tích là \(49,58 \mathrm{m}^{3}\) (ở đkc). Biết hiệu suất toàn bộ quá trình (từ quặng đến kim loại) là \(75 \%\). Tính khối lượng (kg) quặng đã dùng để sản xuất lượng Mg trên?
Tiến hành thí nghiệm như hình vẽ dưới đây:
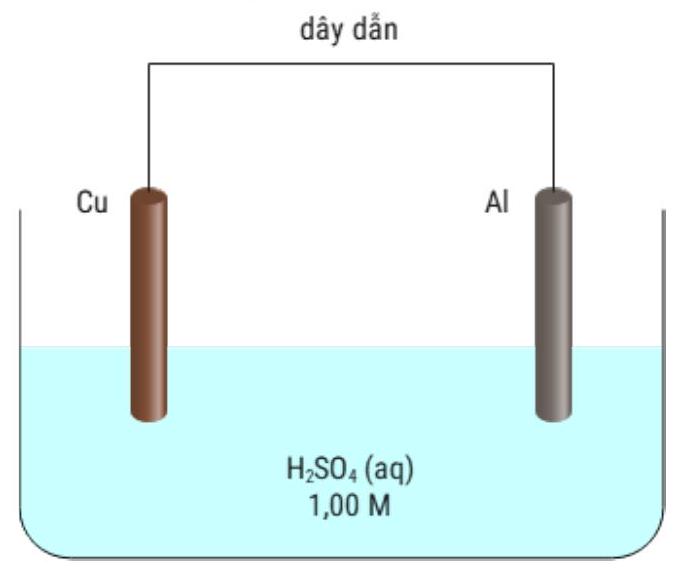 Phát biểu nào sau đây là SAI?
Phát biểu nào sau đây là SAI?Điện phân dung dịch NaCl bão hòa, không có màng ngăn để sản xuất hóa chất nào dưới đây?
Khi điện phân NaCl nóng chảy (điện cực trơ), ở cathode thu được chất nào sau đây?
Khi điện phân dung dịch nào dưới đây tại cathode xảy ra quá trình khử nước?
Cho các cặp oxi hoá - khử và thế điện cực chuẩn tương ứng:
Cặp oxi hóa – khử
2H+/H2
Cu2+/Cu
Fe2+/Fe
Ag+/Ag
Thế điện cực chuẩn (V)
0,00
+0,34
-0,44
+0,799
Khi điện phân dung dịch chứa đồng thời bốn loại cation trên với nồng độ mol bằng nhau, cation bị điện phân đầu tiên ở cathode là
Một sinh viên thực hiện điện phân theo sơ đồ như hình bên.
- Bình (1) chứa 100 ml dung dịch \(\mathrm{CuSO}_{4} 1 \mathrm{M}\).
- Bình (2) chứa 100 ml dung dịch \(\mathrm{AgNO}_{3} 1 \mathrm{M}\).
Sau thời gian \(t\) giây, sinh viên quan sát thấy ở cathode bình (2) bắt đầu xuất hiện khí. Biết trong hệ điện phân nối tiếp, số điện tử truyền dẫn trong các bình là như nhau. Nguyên tử khối của Cu và Ag lần lượt là 64 và 108 đvC.
Coi như nhiệt độ ở 2 bình là không thay đổi và bỏ qua các quá trình phụ.Tính số gam Cu bám lên điện cực trong bình (1) tại thời điểm t giây.
Điện phân có nhiều ứng dụng trong thực tiễn sản xuất và đời sống như luyện kim, tinh chế kim loại, mạ điện, ...
Điện phân dung dịch \(\mathrm{Cu}\left(\mathrm{NO}_{3}\right)_{2}\) với điện cực trơ, ở anode xảy ra quá trình nào?
Điện phân \(\mathrm{CaCl}_{2}\) nóng chảy, ở cathode xảy ra quá trình nào?
Cryolite (còn gọi là băng thạch) có công thức phân tử \(\mathrm{Na}_{3} \mathrm{AlF}_{6}\), được thêm vào \(\mathrm{Al}_{2} \mathrm{O}_{3}\) trong quá trình điện phân \(\mathrm{Al}_{2} \mathrm{O}_{3}\) nóng chảy để sản xuất aluminium. Cryolite không có tác dụng nào sau đây?
Cho các phát biểu sau:
(a) Tráng Sn lên Fe là phương pháp bảo vệ kim loại bằng phương pháp điện hóa.
(b) Trong quá trình điện phân, tại anode xảy ra quá trình oxi hóa.
(c) Cho mẫu nhỏ Na vào dung dịch \(\mathrm{CuSO}_{4}\), thấy xuất hiện kết tủa màu đỏ.
(d) Vỏ các loài ốc, sò, hến có chứa \(\mathrm{CaCO}_{3}\).
(e) Để phân biệt khí \(\mathrm{CO}_{2}\) và \(\mathrm{SO}_{2}\) có thể dùng dung dịch nước vôi trong
Số phát biểu đúng là
Một học sinh muốn xác định hàm lượng Cu có trong hợp \(\operatorname{kim} \mathrm{Cu}-\mathrm{Zn}\), học sinh đã tiến hành làm thí nghiệm như sau:
- Bước 1: Tiến hành cân thanh hợp kim Cu-Zn (2,25 gam) và thanh đồng nguyên chất (2,58 gam).
- Bước 2: Nối thanh hợp kim với cực dương, thanh đồng nguyên chất với cực âm của nguồn điện một chiều có hiệu điện thế phù hợp, rồi nhúng vào bình điện phân chứa dung dịch copper(II) sulfate.
Sau một thời gian điện phân, làm khô, rồi cân lại khối lượng thanh đồng nguyên chất (2,99 gam). Giả thuyết trong quá trình điện phân không chịu sự ảnh hưởng của các yếu tố khác như: hoạt độ của ion và quá thế, \(\ldots\). Học sinh đã phát biểu như sau:
Thí nghiệm điện phân dung dịch copper (II) sulfate với các điện cực trơ (graphite) được mô phỏng như hình vẽ sau đây:
Mạ điện là một trong những ứng dụng của điện phân dựa trên định luật Faraday. Sơ đồ bên dưới minh họa một bình điện phân được sử dụng để mạ bạc cho muỗng bằng đồng. Tính khối lượng kim loại bạc tạo thành phủ lên muỗng bằng đồng khi dùng dòng điện 2,1A trong 45 phút để mạ điện thìa đồng với hiệu suất là 80% (làm tròn đáp án đến hàng phần mười).
Nước Javel là một hóa chất quen thuộc, thường dùng làm chất tẩy rửa và khử trùng. Quá trình sản xuất nước Javel ( NaClO ) trong công nghiệp bằng phương pháp điện phân dung dịch NaCl loãng không có màng ngăn để tạo ra hỗn hợp chứa NaClO.
Cho các phát biểu sau:
Điện phân dung dịch copper(II) sulfate, nhóm học sinh đã tiến hành như sau: Nhúng hai điện cực vào cốc đựng khoảng 60 mL dung dịch \(\mathrm{CuSO}_{4} 0,5 \mathrm{M}\) rồi nối hai điện cực với nguồn điện để tiến hành điện phân (Chú ý không để hai điện cực đã nối nguồn điện chạm vào nhau). Thời gian điện phân là 5 phút với cường độ dòng điện 10A. Quan sát hiện tượng thí nghiệm xảy ra, một học sinh phát biểu như sau:
\(\mathrm{Al}_{2} \mathrm{O}_{3}\) có nhiệt độ nóng chảy rất cao \(\left(2050^{\circ} \mathrm{C}\right)\) nên việc điện phân nóng chảy \(\mathrm{Al}_{2} \mathrm{O}_{3}\) nguyên chất sẽ khó thực hiện. Hiện nay, theo công nghệ Hall-Héroult, người ta hoà tan \(\mathrm{Al}_{2} \mathrm{O}_{3}\) trong cryolite \(\left(\mathrm{Na}_{3} \mathrm{AlF}_{6}\right)\) nóng chảy được hỗn hợp chất điện phân có nhiệt độ nóng chảy thấp hơn (khoảng gần \(1000^{\circ} \mathrm{C}\) ). Giải pháp này giúp tiết kiệm năng lượng, đồng thời tạo ra chất lỏng có tính dẫn điện tốt, nhẹ hơn Al và nổi lên phía trên lớp A 1 lỏng, bảo vệ Al không bị oxi hoá bởi không khí. Sơ đồ thùng điện phân được biểu diễn như hình dưới:
Quá trình điện phân được tiến hành với dòng điện có hiệu điện thể thấp (khoảng 5 V ) và cường độ dòng điện \(100-300 \mathrm{~km}\). Để sản xuất được 1 tấn Al cần tiêu tốn khoảng 2 tấn \(\mathrm{Al}_{2} \mathrm{O}_{3} 50 \mathrm{~kg}\) cryolite, 400 kg than côc.
Cho biết: Năng lượng điện tiêu thụ theo lí thuyết, \(\mathrm{A}_{\mathrm{lt}}=\frac{\mathrm{U}_{\mathrm{m}} \cdot \mathrm{m} \cdot \mathrm{F}}{9 \cdot 3,6 \cdot 10^{6}}(\mathrm{kWh})\). Với \(\mathrm{m}_{\mathrm{Al}}\) là khối lượng Al được điều chế ( gam ); F là hằng số Faraday, \(\mathrm{F}=96485 \mathrm{C} \mathrm{mol}^{-1}, \mathrm{U}(\mathrm{V})\) là hiệu điện thế áp đặt vào hai cực của bình điện phân.















