Trả lời:
Đáp án đúng: B
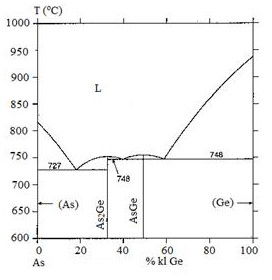
Điểm ơtecti là điểm mà tại đó xảy ra chuyển biến ơtecti, tức là một pha lỏng chuyển thành hai pha rắn đồng thời ở một nhiệt độ xác định. Trên giản đồ pha đã cho, ta thấy có hai điểm mà tại đó một đường nằm ngang (biểu diễn nhiệt độ không đổi) cắt qua vùng có ba pha (một pha lỏng và hai pha rắn). Do đó, có hai điểm ơtecti trên giản đồ này.
Sưu tầm và chia sẻ hơn 850 câu trắc nghiệm môn Hóa học đại cương (kèm đáp án) dành cho các bạn sinh viên, sẽ giúp bạn hệ thống kiến thức chuẩn bị cho kì thi sắp diễn ra. Mời các bạn tham khảo!
50 câu hỏi 60 phút