Tuyển Tập Đề Thi Tham Khảo Tốt Nghiệp THPT Năm 2025 - Hóa Học - Bộ Đề 03 - Đề Số 04
Câu 1
Hình vẽ dưới đây minh hoạ cho thí nghiệm về ăn mòn kim loại mà một học sinh thực hiện:
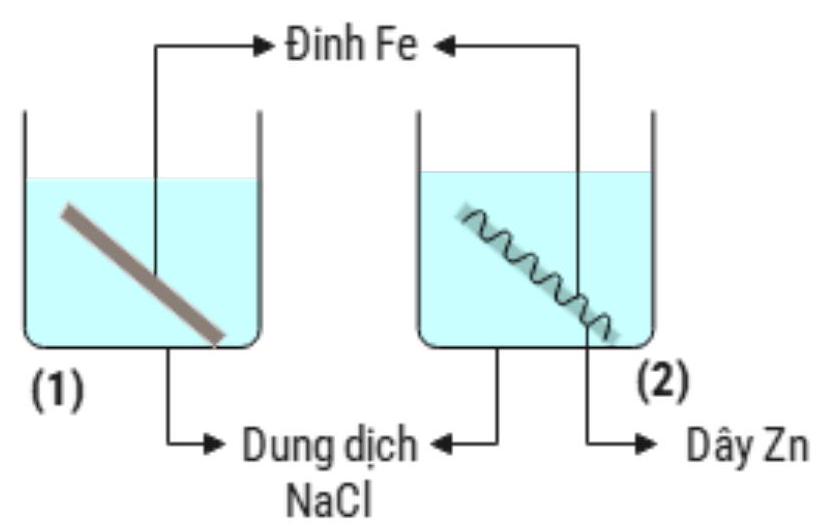 Để yên hai cốc sau một thời gian (cho biết là đinh Fe làm bằng thép). Nhận định nào sau đây đúng?A.
Để yên hai cốc sau một thời gian (cho biết là đinh Fe làm bằng thép). Nhận định nào sau đây đúng?A.Ở cốc (1) nếu thay đinh sắt bằng hợp kim\(\mathrm{Fe}-\mathrm{Cu}\) thì Cu sẽ bị ăn mòn trước.
B.Ở cốc (2) Zn và Fe đều không bị ăn mòn.
C.Ở cốc (1) Fe không bị ăn mòn.
D.Ở cốc (2) Zn bị ăn mòn trước, khi Zn bị ăn mòn hết thì Fe sẽ bị ăn mòn.
Câu 2
Loại đá và khoáng chất nào sau đây không chứa thành phần calcium carbonate?
A.Đá vôi.
B.Thạch cao.
C.Đá hoa.
D.Đá phấn.
Câu 3
Khí nào nhẹ hơn không khí, thường được nạp vào khinh khí cầu (càng nhẹ càng tốt). Trong thực tế người ta thường nạp vào khí cầu khí nào sau đây?
A.He.
B.CO.
C.\(\mathrm{H}_{2}\).
D.\(\mathrm{N}_{2}\).
Câu 4
Phát biểu nào sau đây sai?
A.Glucose thuộc loại monosaccharide.
B.Nicotin là một amine độc, có trong thuốc lá.
C.Trong y học, glutamic acid là thuốc hỗ trợ thần kinh.
D.Cho cellulose vào dung dịch \(\mathrm{I}_{2}\) thấy xuất hiện màu xanh tím.
Câu 5
Tiến hành các thí nghiệm và ghi lại như sau:
Thí nghiệm 1. Nhỏ từ từ đến dư dung dịch methylamine vào ống nghiệm đựng dung dịch \(\mathrm{CuSO}_{4}\) thu được dung dịch màu xanh tím.
Thí nghiệm 2 . Nhỏ nước bromine vào ống nghiệm đựng dung dịch aniline thấy có kết tủa màu trắng xuất hiện.
Thí nghiệm 3. Cho từ từ dung dịch ethylamine vào ống nghiệm đựng dung dịch hỗn hợp acid \(\mathrm{HCl}+\mathrm{NaNO}_{2}\) ở nhiệt độ thường thấy có khí không màu bay lên.
Thí nghiệm 4 . Nhỏ vài giọt dung dịch aniline vào mẩu giấy quỳ tím, thấy màu quỳ tím chuyển sang màu xanh.
Hiện tượng ở thí nghiệm nào được ghi lại không đúng?
A.Thí nghiệm 1.
B.Thí nghiệm 2.
C.Thí nghiệm 3.
D.Thí nghiệm 4.
Câu 7
Chất nào sau đây có thể làm thuốc trừ sâu, thường dùng để phun trị bệnh nấm mốc sương cho nho?
A.\(\mathrm{SO}_{2} \mathrm{Cl}_{2}\).
B.\(\mathrm{CuSO}_{4}\)
C.\(\mathrm{Zn}_{3} \mathrm{P}_{2}\).
D.\(\mathrm{SO}_{2}\).
Câu 8
Cho các chất có công thức cấu tạo như sau:
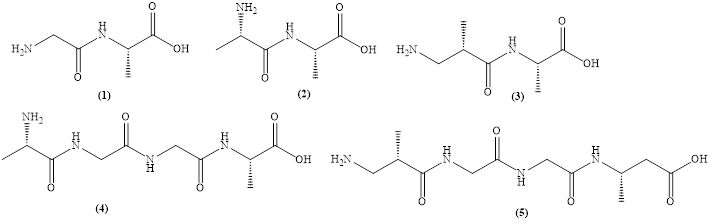
Có bao nhiêu chất tham gia phản ứng màu biuret cho màu tím đặc trưng?
A.2 chất.
B.3chất.
C.1 chất.
D.4 chất.
Câu 9
Phần trăm khối lượng của nguyên tố carbon trong trong phân tử aniline?
A.\(83,72 \%\)
B.\(75,00 \%\)
C.\(78,26\%\)
D.\(77,42\%\)
Câu 10
Ở điều kiện chuẩn, những kim loại tan trong hydrochloric acid hoặc sulfuric acid loãng thường có thế điện cực chuẩn như thế nào?
A.Thế điện cực chuẩn lớn hơn 0V.
B.Thế điện cực chuẩn lớn hơn \(-0,413 \mathrm{~V}\).
C.Thế điện cực chuẩn nhỏ hơn \(0,413 \mathrm{~V}\).
D.Thế điện cực chuẩn nhỏ hơn 0V.
Câu 11
Cho các nguyên tố có vị trí trong bảng tuần hoàn như hình dưới đây?
Phát biểu nào sau đây là ĐÚNG?
A.Trong ba nguyên tố thì P có tính phi kim mạnh nhất.
B.Bán kinh nguyên tử tăng dần theo thứ tự \(\mathrm{F}<\mathrm{P}<\mathrm{Cl}\).
C.Xét sự phân bố electron vào các orbital thì P có số electron độc thân nhiều nhất.
D.Trong 3 nguyên tố, \(F\) có độ âm điện nhỏ nhất.
Câu 12
Một chiếc khuyên tai dạng đĩa tròn mỏng có đường kính \(5,00 \mathrm{~cm}\) được mạ với lớp phủ vàng dày \(0,02 \mathrm{~mm}\) từ dung dịch \(\mathrm{Au}^{3+}\). Cho khối lượng riêng của vàng là \(19,3 \mathrm{~g} / \mathrm{cm}^{3}\).
\(\mathrm{Q}=\mathrm{It}=\mathrm{nF}\) với \(\mathrm{F}=96500 \mathrm{C} / \mathrm{mol}\) và \(\mathrm{I}=0,10 \mathrm{~A}\).
Giá vàng 9999 là 85 triệu đồng/lượng (1 lượng vàng nặng \(37,5 \mathrm{~g}\) ).
Phát biểu nào sau đây là đúng?
A.Khối lượng vàng cần mạ lên hai mặt của chiếc khuyên tai là \(6,60 \mathrm{~g}\).
B.Thời gian để mạ vàng cho chiếc khuyên tai là 24,7 giờ.
C.Chi phí mua vàng để mạ chiếc khuyên tai là 13.736.000 đồng.
D.Trong quá trình mạ, chiếc khuyên tai đóng vai trò là cathode.
Câu 14
Một số loại thực vật chỉ phát triển tốt ở môi quan trọng trong nông nghiệp. Một số loại cây trồng trường có pH phù hợp, việc nghiên cứu pH của đất rất phù hợp với đất có giá trị pH cho trong bảng sau:
Cây trồng
pH thích hợp
Cây trồng
pH thích hợp
Bắp (ngô)
5.7-7.5
Cây chè
4.5-5.5
Cà chua
6.0-7.0
Thanh Long
4.0-6.0
Cải thảo
6.5-7.0
Lúa
5.5-6.5
Hành tây
6.4-7.9
Mía
5.0-8.0
Dùng máy đo pH xác định được giá trị pH của một loại đất là 4,52 . Phát biểu nào sau đây đúng?
A.A. Loại đất trên không phù hợp trồng cây chè và thanh long.
B.B. Nồng độ Ion \(\left[\mathrm{H}^{+}\right]\) của loại đất trên lớn hơn \(1 \cdot 10^{-7} \mathrm{M}\).
C.C. Loại đất trên bị chua, để trồng hành tây, cà chua, mía phát triển tốt ta cần khử chua cho đất bằng urea.
D.D. Để cây cải thảo và hành tây phát triển tốt trên loại đất trên, ta cần bón nhiều đạm hai lá \(\left(\mathrm{NH}_{4} \mathrm{NO}_{3}\right)\) qua nhiều vụ liên tiếp để tăng pH của đất.
Câu 15
Dạng carbocation được hình thành trong một thời gian ngắn khi một nguyên tử carbon trong một hợp chất chỉ có 3 liên kết thay vì là 4 . Do vậy, nguyên từ carbon mang điện dương. Có bốn loại carbocation khác nhau được gọi là methyl, primary (bậc một), secondary (bậc hai), và tertiary (bậc ba), phụ thuộc vào sự sắp xếp của các nhóm alkyl trong phân tử.Cho các carbocation như sau:
Loại carbocation nào được biểu diễn ở hình (i)?
A.Methyl.
B.Primary.
C.Secondary.
D.Tertiary.
Câu 16
Dạng carbocation được hình thành trong một thời gian ngắn khi một nguyên tử carbon trong một hợp chất chỉ có 3 liên kết thay vì là 4 . Do vậy, nguyên từ carbon mang điện dương. Có bốn loại carbocation khác nhau được gọi là methyl, primary (bậc một), secondary (bậc hai), và tertiary (bậc ba), phụ thuộc vào sự sắp xếp của các nhóm alkyl trong phân tử.Cho các carbocation như sau:
Càng nhiều nhóm alkyl liên kết với carbon mang điện dương thì carbocation càng bền. Thứ tự độ bền tăng dần của bốn carbocation trên là
A.(ii), (iv), (iii), (i).
B.(i), (iii), (iv), (ii).
C.(ii), (iii), (iv), (i).
D.(i), (iv), (iii), (ii).
Câu 17
Chất nào sau đây không tạo được liên kết hydrogen giữa các phân tử?
A.\(\mathrm{NH}_{3}\).
B.\(\mathrm{H}_{2} \mathrm{O}\).
C.HF.
D.\(\mathrm{CH}_{4}\).
Câu 19
Giải Nobel Hóa học năm 2022 được trao cho các nhà khoa học nghiên cứu về hóa học click". Hợp chất \(\mathrm{DBCO}-\mathrm{Acid}\) dưới đây là phân tử được sử dụng trong nghiên cứu này.
Cho các phát biểu sau:
a. DBCO-acid có thể tham gia phản ứng cộng.
b. DBCO-acid có thể phản ứng với NaOH vời tỷ lệ tối đa là \(1: 1\).
c. DBCO -acid có thể làm mất màu dung dịch nước bromine và dung dịch \(\mathrm{KMnO}_{4}\) trong môi trường acid.
d. DBCO-acid có thể phản ứng với amino acid và nhóm amine trong protein ở điều kiện thích hợp.
Câu 20
Cho phản ứng như sau: \(\mathrm{aA} \longrightarrow \mathrm{bB}\). Kết quả sự thay đổi số mol theo thời gian được mô tả bằng hình vẽ sau:
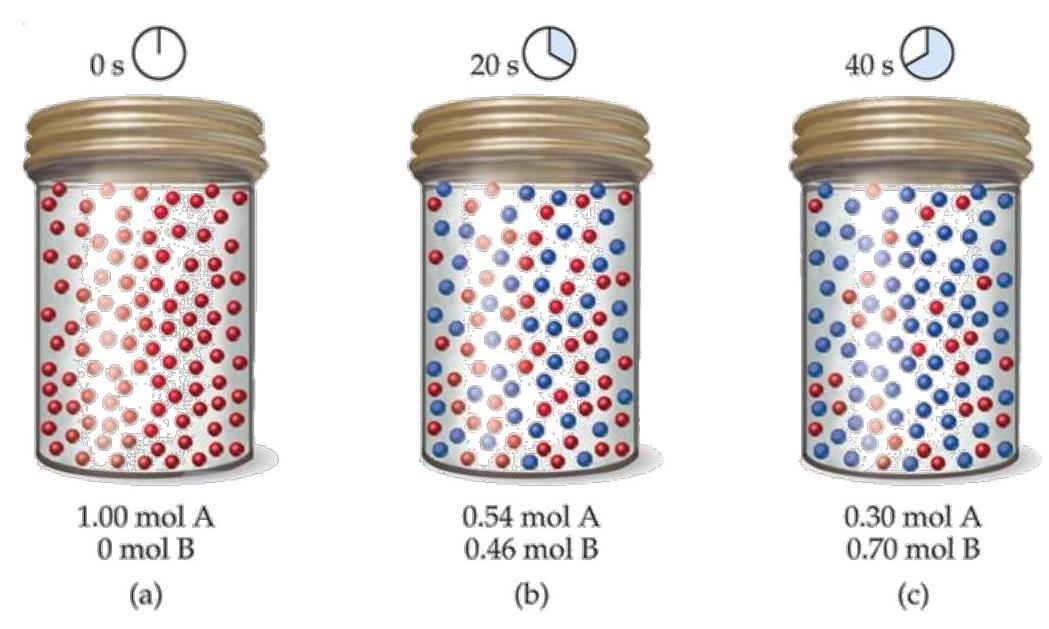 Cho các phát biểu sau:
Cho các phát biểu sau:a. Tỷ lệ hệ số cân bằng \(a\) và \(b\) là \(1: 1\).
b. Tốc độ phản ứng trong 20 s đầu là \(0,023 \mathrm{~mol} / \mathrm{s}\).
c. Tốc độ tiêu hao chất A và tốc độ hình thành chất B là bằng nhau trong 40 s đầu của phản ứng.
d. Tốc độ hình thành chất B trong 40 s là \(0,0175 \mathrm{~mol} / \mathrm{s}\).
Câu 21
Người ta thường dùng ethyl acohol để lên men tạo acetic acid. Để xác định hàm lượng acetic acid trong giấm, người ta cho các cách dưới đây:
Cách 1: Xác định khối lượng riêng của giấm rồi so với khối lượng riêng của dung dịch mẫu pha từ \(\mathrm{CH}_{3} \mathrm{COOH}\) và nước.
Cách 2: Cô cạn nước, còn lại là \(\mathrm{CH}_{3} \mathrm{COOH}\).
Cách 3: Chuẩn độ bằng dung dịch NaOH đã biết nồng độ tới khi làm dung dịch phenolphthalein hóa hồng.
Cho các phát biểu sau:
a. Phản ứng lên men tạo acetic acid từ ethyl alcohol là \(\mathrm{C}_{2} \mathrm{H}_{5} \mathrm{OH}+\mathrm{O}_{2} \xrightarrow{\text { men }} \mathrm{CH}_{3} \mathrm{COOH}+\mathrm{H}_{2} \mathrm{O}\)
b. Cách (1), (3) đều có thể dùng để xác định hàm lượng acetic acid trong giấm.
c. Cách (2) sai vì khi cô cạn thì \(\mathrm{CH}_{3} \mathrm{COOH}\) kết tinh ở chất rắn dạng ngậm nước.
d. Nếu \(\mathrm{H} \%=50 \%\) thì từ 46 gam \(\mathrm{C}_{2} \mathrm{H}_{5} \mathrm{OH}\) điều chế được dung dịch có chứa 23,0 gam \(\mathrm{CH}_{3} \mathrm{COOH}\).
Câu 22
Trước đây, tinh thể copper(II) sulfate được "nuôi" như sau:
Bước 1: Cho dung dịch sulfuric acid loãng vào cốc thuỷ tinh.
Bước 2: Đun nóng dung dịch acid.
Bước 3: Thêm copper (II) oxide vào đến dư.
Bước 4: Đợi phản ứng xảy ra hoàn toàn rồi lọc hỗn hợp thu được.
Bước 5: Làm bay hơi nước lọc cho đến khi tinh thể xuất hiện trong cốc.
Bước 6: Làm mát cốc nước lọc.
Cho các phát biểu sau:
a. Mục đích của bước 3 là để chắc chắn sulfuric acid phản ứng hết.
b. Mục đích của bước 4 là để thu copper(II) sulfate rắn.
c. Tinh thế copper(II) sulfate là dạng rắn kết tinh màu xanh.
d. Cho 50 gam tinh thể \(\mathrm{CuSO}_{4} \cdot \mathrm{nH}_{2} \mathrm{O}\) vào 450 ml nước, thu được dung dịch A . Sau đó cho vừa đủ dung dịch NaOH vào dung dịch A , sau khi phản ứng kết thúc thu được 19,6 gam kết tủa. Công thức của tinh thể xác định được là \(\mathrm{CuSO}_{4} .3 \mathrm{H}_{2} \mathrm{O}\).
Top 10/0 lượt thi
| Tên | Điểm | Thời gian |
|---|















