Câu hỏi:
Phát biểu nào sau đây sai?
Đáp án đúng: B
Chọn B.
Câu hỏi này thuộc đề thi trắc nghiệm dưới đây, bấm vào Bắt đầu thi để làm toàn bài
Tuyển Tập Đề Thi Tham Khảo Tốt Nghiệp THPT Năm 2025 - Hóa Học - Bộ Đề 06 giúp học sinh lớp 12 ôn tập hiệu quả và tự tin bước vào kỳ thi Tốt nghiệp THPT năm 2025. Mỗi đề thi trong tài liệu được xây dựng theo đúng cấu trúc chuẩn của Bộ Giáo dục và Đào tạo, bao gồm ba phần: trắc nghiệm nhiều lựa chọn, trắc nghiệm đúng – sai và trắc nghiệm trả lời ngắn. Các câu hỏi được chọn lọc kỹ lưỡng, bám sát nội dung chương trình, tích hợp kiến thức liên môn và có độ phân hóa phù hợp, giúp học sinh không chỉ ôn tập lý thuyết mà còn rèn luyện kỹ năng giải đề thực tiễn. Đặc biệt, phần đáp án và hướng dẫn giải chi tiết đi kèm giúp học sinh dễ dàng tự đánh giá kết quả và nhận diện các dạng bài quan trọng.
Câu hỏi liên quan
Theo đề ta có: \(\mathrm{n}_{\left(\mathrm{NH}_{4}\right)_{2} \mathrm{SO}_{4}}=\frac{2,64 . 10^{6}}{132}=0,02 . 10^{6} \mathrm{mol}\).
Từ phương trình (2) ta có:
\(\left\{\begin{array}{l}\mathrm{n}_{\mathrm{CaSO}_{4} . 2 \mathrm{H}_{2} \mathrm{O}}=0,02 . 10^{6} \\ \mathrm{n}_{\left(\mathrm{NH}_{4}\right)_{2} \mathrm{O}_{3}}=0,02 . 10^{6} \xrightarrow{\text { thay yào(1) }}\left\{\begin{array}{l}\mathrm{n}_{\mathrm{NH}_{3}}=0,02 . 10^{6} . 2=0,04 . 10^{6} \\ \mathrm{n}_{\mathrm{OO}_{2}}=0,02 . 10^{6}\end{array} \Rightarrow\left\{\begin{array}{l}\mathrm{m}_{\mathrm{CaSO}_{4} . 2 \mathrm{H}_{2} \mathrm{O}}=0,02 . 10^{6} . 172=3,44 . 10^{6} \text { gam } \\ \mathrm{n}_{\mathrm{NH}_{3}}=0,04 . 10^{6} . 17=0,68 . 10^{6} \mathrm{gam} \\ \mathrm{n}_{\mathrm{OO}_{2}}=0,02 . 10^{6} . 44=0,88 . 10^{6} \mathrm{gam}\end{array}\right.\right.\end{array}\right.\)
Đưa hiệu suất vào: \(\left\{\begin{array}{l}\mathrm{m}_{\mathrm{CaSO}_{4} . 2 \mathrm{H}_{2} \mathrm{O}}=3,44 . 10^{6} . \frac{100}{90}=3,82 . 10^{6} \mathrm{gam}=3,82 \mathrm{tấn} \\ \mathrm{m}_{\mathrm{NH}_{3}}=0,68 . 10^{6} . \frac{100}{90} . \frac{100}{80}=0,94 . 10^{6} \mathrm{gam}=0,94 \mathrm{tan} \\ \mathrm{m}_{\mathrm{OO}_{2}}=0,88 . 10^{6} . \frac{100}{90} . \frac{100}{80}=1,22 . 10^{6} \mathrm{gam}=1,22\mathrm{tan}\end{array}\right.\)
Chọn C.
Lidocaine (công thức phân tử \(\mathrm{C}_{14} \mathrm{H}_{22} \mathrm{N}_{2} \mathrm{O}\) ) là một hợp chất hữu cơ được sử dụng phổ biến làm thuốc gây tê cục bộ trong y học, đặc biệt trong nha khoa và tiểu phẫu. Lidocaine là một amine bậc hai thuộc nhóm amide. Khi cho tác dụng với NaOH , có thể xảy ra phản ứng thủy phân liên kết amide trong môi trường base.
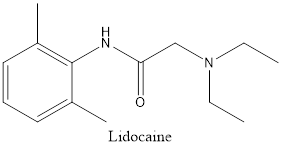
Cho các phát biểu sau:
Khi đun nóng Lidocaine với dung dịch NaOH dư, phản ứng xảy ra ở nhóm amide và thu được muối sodium và amine
Phản ứng giữa lidocaine (một base hữu cơ) và acid hydrochloric \((\mathrm{HCl})\) là phản ứng acid-base, trong đó nhóm amine bậc ba \(\left(-\mathrm{N}\left(\mathrm{CH}_{2} \mathrm{CH}_{3}\right)_{2}\right)\) trong phân tử lidocaine nhận một proton từ HCl để tạo thành muối lidocaine hydroclorid, tan tốt hơn trong nước và dễ hấp thu trong y học
Nếu cho \(0,5 \mathrm{mol}\) Lidocaine tác dụng với acid HCl thì khối lượng muối thu được là hơn 137 gam
Tổng số liên kết \(\pi\) trong phân tử Lidocaine là 6 , bao gồm 3 liên kết \(\pi\) vòng benzene và 1 liên kết \(\pi\) từ nhóm \(\mathrm{C}=\mathrm{O}, 2\) liên kiết \(\pi\) trong nhóm amine
a. Đúng
vì khi đun nóng lidocaine với dung dịch NaOH dư, phản ứng sẽ xảy ra ở nhóm amide (-NH-CO-) trong phân tử lidocaine, gây ra sự thủy phân amide. Sản phẩm của phản ứng này sẽ là một muối của acid cacboxylic và một amine.
b. Đúng
c. Sai
vì sản phẩm thu được là \(\mathrm{C}_{14} \mathrm{H}_{23} \mathrm{N}_{2} \mathrm{OCl}\)
\(\mathrm{m}_{\text {muối }}=135,25 \mathrm{gam}\)
d. Sai
vì tổng số liên kết \(\pi\) là 4 liên kết \(\pi\), trng đó 3 liên kết \(\pi\) tại vòng benzene, 1 liên kết \(\pi\) từ nhóm \(\mathrm{C}=\mathrm{O}\)
Khi bị ợ nóng, bệnh nhận thường được khuyên dùng thuốc kháng acid chứa aluminum hydroxide \(\mathrm{Al}(\mathrm{OH})_{3}\) như thuốc Maalox, Giviscon. Tuy nhiên, nếu dùng lâu dài thuốc này có thể gây tác dụng phụ như táo bón, nên thường được phối hợp với \(\mathrm{Mg}(\mathrm{OH})_{2}\) (có tác dụng nhuận tràng nhẹ) để cân bằng. So với sử dụng thuốc có chứa \(\mathrm{NaHCO}_{3}\) thì phản ứng của thuốc có \(\mathrm{Al}(\mathrm{OH})_{3}\) không sinh khí. Cơ chế của thuốc là trung hòa lượng acid dư trong dạ dày.
Phản ứng trung hòa được biểu diễn như sau: \(\mathrm{Al}(\mathrm{OH})_{3}+3 \mathrm{HCl} \rightarrow \mathrm{AlCl}_{3}+3 \mathrm{H}_{2} \mathrm{O}\)
Cho các phát biểu sau:
So với \(\mathrm{NaHCO}_{3}, \mathrm{Al}(\mathrm{OH})_{3}\) phản ứng chậm và không gây ra hiện tượng sủi bọt
Dùng quá nhiều thuốc có chứa \(\mathrm{Al}(\mathrm{OH})_{3}\) có thể gây táo bón
\(\mathrm{Mg}(\mathrm{OH})_{2}, \mathrm{Al}(\mathrm{OH})_{3}\) đều là base yếu, có thể trung hòa acid trong dạ dày
Thuốc kháng acid "sữa magie" chứa thành phần \(\mathrm{Mg}(\mathrm{OH})_{2}\). Khi tác dụng với acid HCl trong dịch dạ dày thì xảy ra phương trình hóa học (dạng ion thu gọn) như sau: \(\mathrm{H}^{+}+\mathrm{OH}^{-} \rightarrow \mathrm{H}_{2} \mathrm{O}\)
a. Đúng
b. Đúng
c. Đúng
d. Sai.
Phương trình ion rút gọn như sau: \(\mathrm{Mg}(\mathrm{OH})_{2}+2 \mathrm{H}^{+} \rightarrow \mathrm{Mg}^{2+}+2 \mathrm{H}_{2} \mathrm{O}\)
Một hộ gia đình sử dụng hệ thống lọc nước RO tại vòi để loại bỏ tạp chất và làm mềm nước trước khi sử dụng. Để bảo vệ màng lọc RO khỏi bị đóng cặn bởi các ion \(\mathrm{Ca}^{2+}\) và \(\mathrm{Mg}^{2+}\) trong nước cứng, một cột chứa hạt nhựa trao đổi ion cationite dạng \(\mathrm{R}-\mathrm{SO}_{3} \mathrm{Na}\) được lắp đặt phía trước màng lọc.
PTHH xảy ra như sau:
\(2 \mathrm{R}-\mathrm{SO}_{3} \mathrm{Na}+\mathrm{Ca}^{2+} \rightarrow\left(\mathrm{R}-\mathrm{SO}_{3}\right)_{2} \mathrm{Ca}+2 \mathrm{Na}^{+}\)
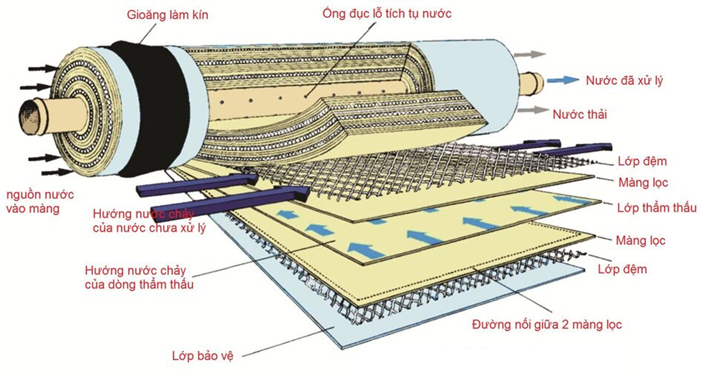
Cho các phát biểu sau:
Một cột lọc nước chứa 250 g hạt cationite \(\mathrm{R}-\mathrm{SO}_{3} \mathrm{Na}\) có khả năng trao đổi tối đa \(0,04 \mathrm{mol}\) ion \(\mathrm{Ca}^{2+}\) cho mỗi 1 g hạt. Nếu nguồn nước chứa \(160 \mathrm{mg} / \mathrm{L}\) ion \(\mathrm{Ca}^{2+}\), thể tích nước tối đa (L) mà cột có thể làm mềm hoàn toàn là 625 L
Phản ứng trao đổi ion giữa cationite \(\mathrm{R}-\mathrm{SO}_{3} \mathrm{Na}\) và ion \(\mathrm{Ca}^{2+}\) trong nước có phương trình:
\(2 \mathrm{R}-\mathrm{SO}_{3} \mathrm{Na}+\mathrm{Ca}^{2+} \rightarrow\left(\mathrm{R}-\mathrm{SO}_{3}\right)_{2} \mathrm{Ca}+2 \mathrm{Na}^{+}\)
Cho thấy \(1 \mathrm{mol} \mathrm{Ca}^{2+}\) trao đổi với \(2 \mathrm{mol} \mathrm{Na}^{+}\)và giải phóng \(\mathrm{Na}^{+}\)vào nước, góp phần làm tăng độ dẫn điện của nước đầu ra
Khi sử dụng cationite dạng \(\mathrm{R}-\mathrm{H}\) thay vì \(\mathrm{R}-\mathrm{SO}_{3} \mathrm{Na}\) để làm mềm nước, pH nước đầu ra có xu hướng giảm do ion \(\mathrm{H}^{+}\)được giải phóng vào nước trong quá trình trao đổi
Một gia đình dùng 600 L nước/ngày, chứa trung bình \(120 \mathrm{mg} / \mathrm{L} \mathrm{Ca}^{2+}\) và \(24 \mathrm{mg} / \mathrm{L} \mathrm{Mg}^{2+}\). Cột lọc chứa 360 g R- \(\mathrm{SO}_{3} \mathrm{Na}\), có khả năng trao đổi tổng cộng \(0,05 \mathrm{mol}\) ion hóa trị II trên mỗi 1 g hạt. Cột lọc này có thể sử dụng tối đa trong 10 ngày trước khi bão hòa
a. Sai
-Tổng số \(\mathrm{mol} \mathrm{CO}_{2}\) trao đổi là:
PTHH
\(\mathrm{C}_{2} \mathrm{H}_{5} \mathrm{OH}+\frac{1}{2} \mathrm{O}_{2} \rightarrow \mathrm{CH}_{3} \mathrm{OOH} \quad \sum \mathrm{n}_{\mathrm{CO}_{2} \mathrm{td}}=250.0,04=10 \mathrm{mol}\)
\(\mathrm{CH}_{3} \mathrm{OOH}+\mathrm{Zn} \rightarrow\left(\mathrm{CH}_{3} \mathrm{COO}\right)_{2} \mathrm{Zn}+\mathrm{H}_{2} \uparrow\)
Tổng khối lượng \(\mathrm{Ca}^{2+}=10.40=400 \mathrm{g}=4.10^{5} \mathrm{mg}\)
Thể tích nước \(=\frac{4.10^{5}}{160}=2500\) (lit)
b. Đúng
c. Đúng.
d. Sai
\(\mathrm{m}_{\mathrm{Ca}^{2+}}=600.120=72 \mathrm{g} \rightarrow \mathrm{n}_{\mathrm{Ca}^{2+}}=1,8 \mathrm{mol}\)
\(\mathrm{m}_{\mathrm{Mg}^{2+}}=600.24=14,4 \mathrm{g} \rightarrow \mathrm{n}_{\mathrm{Mg}^{2+}}=0,6 \mathrm{mol}\)
\(\sum \mathrm{n}_{\text {ion }}=2,4 \mathrm{mol}\)
Sức chứa trao đổi \(=360 . 0,05=18 \mathrm{mol}\)
Số ngày dùng \(\frac{18}{24}=7,5\)
Trong quá trình sản xuất sulfuric acid, sulfur dioxide được chuyển thành sulfur trioxide ở nhiệt độ \(400-500{ }^{\circ} \mathrm{C}\) theo phản ứng: \(2 \mathrm{SO}_{2}(\mathrm{g})+\mathrm{O}_{2}(\mathrm{g}) \stackrel{\mathrm{V}_{2} \mathrm{O}_{5}, \mathrm{t}^{\circ}}{\Longleftrightarrow} 2 \mathrm{SO}_{3}(\mathrm{g}), \Delta_{\mathrm{r}} \mathrm{H}_{298}^{\rho}<0\)
Sau khi hệ đạt trạng thái cân bằng, một số yếu tố được thay đổi, kể cả thêm chất xúc tác, dẫn đến sự chuyển dịch trạng thái cân bằng như đồ thị sau:
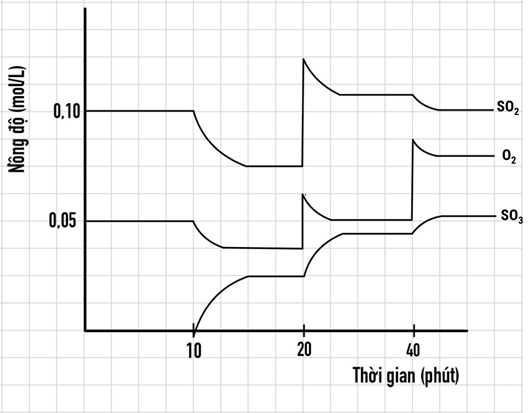
Cho các phát biểu sau:
Biểu thức hằng số Kc của phản ứng \(\mathrm{K}_{\mathrm{C}}=\frac{\mathrm{p}_{\mathrm{SO}_{3}}{ }^{2}}{\mathrm{p}_{\mathrm{SO}_{2}}{ }^{2} . \mathrm{p}_{\mathrm{O}_{2}}}\)
Hệ đạt trạng thái cân bằng trong các khoảng thời gian: 15-20 phút, 25-30 phút, 35-40 phút
Tại thời điểm 18 phút, hệ đạt trạng thái cân bằng, có \(\mathrm{K}_{\mathrm{C}}=1,5625 \mathrm{M} / \mathrm{s}\)
Tại thời điểm 20 phút đã thực hiện tăng áp suất bằng cách giảm thể tích của hệ đi 1,67 lần, nên cân bằng chuyển dịch về phía thuận

Bộ 50 Đề Thi Thử Tốt Nghiệp THPT Giáo Dục Kinh Tế Và Pháp Luật Năm 2026 – Theo Cấu Trúc Đề Minh Họa Bộ GD&ĐT

Bộ 50 Đề Thi Thử Tốt Nghiệp THPT Lịch Sử Học Năm 2026 – Theo Cấu Trúc Đề Minh Họa Bộ GD&ĐT

Bộ 50 Đề Thi Thử Tốt Nghiệp THPT Công Nghệ Năm 2026 – Theo Cấu Trúc Đề Minh Họa Bộ GD&ĐT

Bộ 50 Đề Thi Thử Tốt Nghiệp THPT Môn Hóa Học Năm 2026 – Theo Cấu Trúc Đề Minh Họa Bộ GD&ĐT

Bộ 50 Đề Thi Thử Tốt Nghiệp THPT Môn Sinh Học Năm 2026 – Theo Cấu Trúc Đề Minh Họa Bộ GD&ĐT

Bộ 50 Đề Thi Thử Tốt Nghiệp THPT Môn Vật Lí Năm 2026 – Theo Cấu Trúc Đề Minh Họa Bộ GD&ĐT
ĐĂNG KÝ GÓI THI VIP
- Truy cập hơn 100K đề thi thử và chính thức các năm
- 2M câu hỏi theo các mức độ: Nhận biết – Thông hiểu – Vận dụng
- Học nhanh với 10K Flashcard Tiếng Anh theo bộ sách và chủ đề
- Đầy đủ: Mầm non – Phổ thông (K12) – Đại học – Người đi làm
- Tải toàn bộ tài liệu trên TaiLieu.VN
- Loại bỏ quảng cáo để tăng khả năng tập trung ôn luyện
- Tặng 15 ngày khi đăng ký gói 3 tháng, 30 ngày với gói 6 tháng và 60 ngày với gói 12 tháng.