Câu hỏi:
Cho biết CTCT của 1 một số amino acid sau:
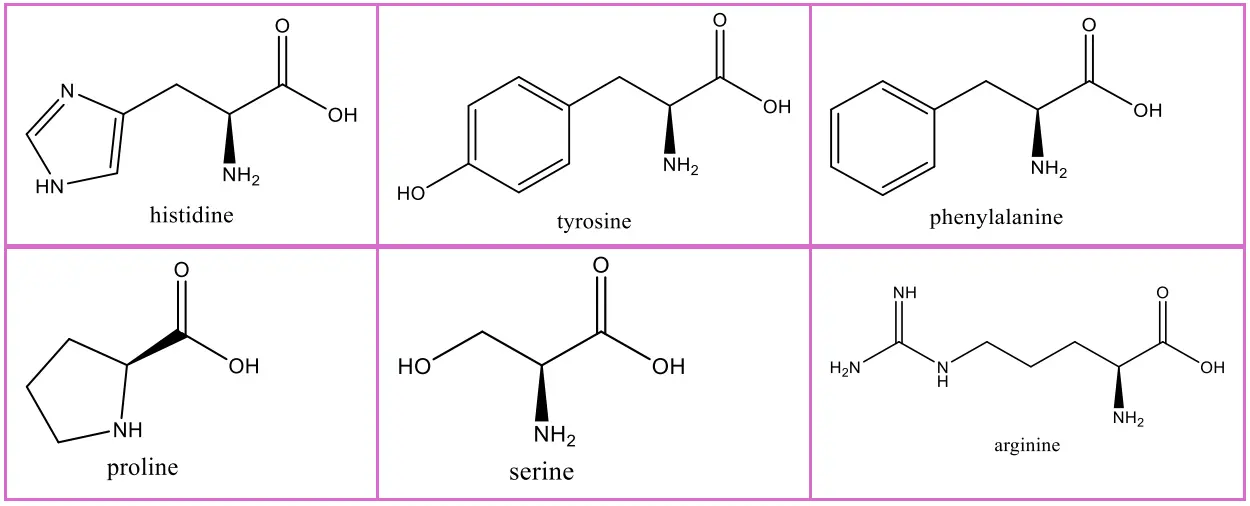
Trật tự các amino acid trong CTCT của peptide dưới đây là
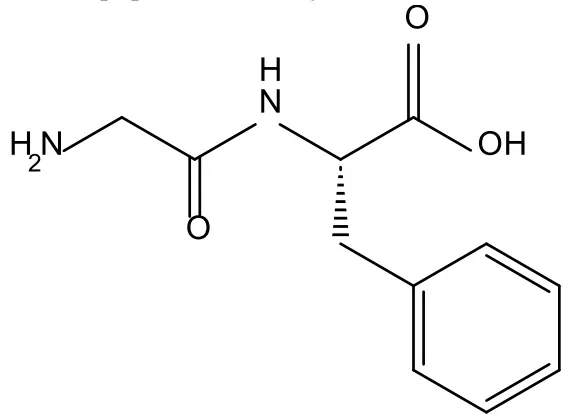
Đáp án đúng: B
Trật tự các amino acid trong CTCT của peptide đề cho là Gly-Phe.
Đáp án đúng là B.
Câu hỏi này thuộc đề thi trắc nghiệm dưới đây, bấm vào Bắt đầu thi để làm toàn bài
“Tuyển Tập Đề Thi Tham Khảo Tốt Nghiệp THPT Năm 2026 – Hoá Học – Bộ Đề 03” được biên soạn bám sát cấu trúc đề thi mới nhất.Các câu hỏi phủ rộng kiến thức Hoá học THPT, từ cơ bản đến vận dụng.Đề thi giúp học sinh rèn luyện kỹ năng làm bài và phân bổ thời gian hợp lý.Phù hợp cho ôn tập giai đoạn nước rút trước kỳ thi tốt nghiệp.Là tài liệu tham khảo hữu ích cho học sinh và giáo viên trong quá trình luyện thi.
Câu hỏi liên quan
Bromomethane được sử dụng làm chất để tiêu diệt côn trùng gây hại trong hạt. Bromomethane có thể được tạo ra bằng cách cho methanol phản ứng với hydrogen bromide theo phương trình sau:
\(\mathrm{CH}_3 \mathrm{OH}_{(\mathrm{l})}+\mathrm{HBr}_{(\mathrm{g})} \longrightarrow \mathrm{CH}_3 \mathrm{Br}_{(\mathrm{g})}+\mathrm{H}_2 \mathrm{O}_{(\mathrm{l})}\)
Cho nhiệt tạo thành chuẩn của các chất tương ứng trong phương trình như sau:
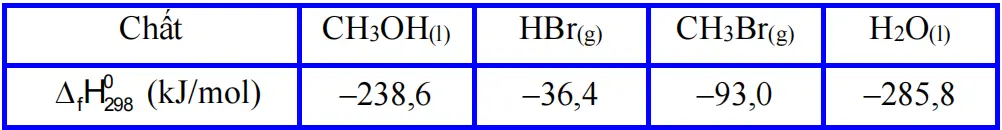
Cho các phát biểu sau:
Phản ứng (1) thuộc loại phản ứng thế nucleophile
Biến thiên enthalpy chuẩn của phản ứng (1) là \( - 103,8{\rm{\;kJ}}\)
Sản phẩm chính của phản ứng (1) có thể tác dụng với dung dịch NaOH và thể hiện tính khử
Nếu cho 2 tấn bromomethane thì phản ứng (1) toả ra môi trường lượng nhiệt bằng \(2185,3\ {\rm{MJ}}\)
a. Phản ứng (1) thuộc loại phản ứng thế nucleophile.
Đáp án đúng là Đúng.
b. CT tính enthalpy:
\(\begin{array}{*{20}{r}}{{{\rm{\Delta }}_{\rm{r}}}{\rm{H}}_{298}^\rho }&{\; = {{\rm{\Delta }}_{\rm{f}}}{\rm{H}}_{298}^\rho \left( {{{\rm{H}}_2}{\rm{O}}} \right) + {{\rm{\Delta }}_{\rm{f}}}{\rm{H}}_{298}^\rho \left( {{\rm{C}}{{\rm{H}}_3}{\rm{Br}}} \right) - \left[ {{{\rm{\Delta }}_{\rm{f}}}{\rm{H}}_{298}^\rho \left( {{\rm{HBr}}} \right) + {{\rm{\Delta }}_{\rm{f}}}{\rm{H}}_{298}^\rho \left( {{\rm{C}}{{\rm{H}}_3}{\rm{OH}}} \right)} \right]}\\{}&{\; = \left( { - 285,8} \right) + \left( { - 93} \right) - [\left( { - 36,4} \right) + \left( { - 238,6} \right) = - 103,8{\rm{\;kJ}}}\end{array}\).
Đáp án đúng là Đúng.
c. khi \({\rm{C}}{{\rm{H}}_3}{\rm{Br}}\) tác dụng NaOH thì phản ứng như sau: \(\mathrm{CH}_3 \mathrm{Br}+\mathrm{NaOH} \xrightarrow{\mathrm{t}^0} \mathrm{CH}_3 \mathrm{CH}+\mathrm{NaBr}\)
\(\Rightarrow\)Không có sự thay đổi oxi hoá.
Đáp án đúng là Sai.
d. Phương trình (1) và ý (b) thì 1 mol bromoethane tham gia sẽ toả ra \(103,8{\rm{\;kJ}}\).
Ta có: \({{\rm{n}}_{{\rm{bromomethane\;}}}} = \frac{{{{2.10}^6}}}{{95}}{\rm{\;mol}} \Rightarrow \) Nhiệt toả ra là \(\frac{{{{2.10}^6}}}{{95}} \cdot 103,8 = 2185263,158{\rm{\;kJ}} \approx 2185,3\ {\rm{MJ}}\).
Đáp án đúng là Đúng.
Chất tạo ngọt E951 (Aspartame (APM)) là một chất làm ngọt nhân tạo không chứa đường saccharide được sử dụng như một chất thay thế đường trong một số thực phẩm và đồ uống. Aspartame tạo ra năng lượng tương đương saccharide (khoảng \(17{\rm{\;kJ}}/{\rm{gam}}\)) nhưng có độ ngọt gấp 200 lần sucrose (đường ăn). Do đó chỉ cần 1 lượng aspartam rất nhỏ đã đủ tạo độ ngọt mà sự đóng góp calor của nó là không đáng kể. AOM được đánh giá là an toàn đối với người, tổ chức WHO xác định liều lượng an toàn là \(40\ {\rm{mg}}/{\rm{kg}}\) trọng lượng. Công thức cấu tạo APM như sau:
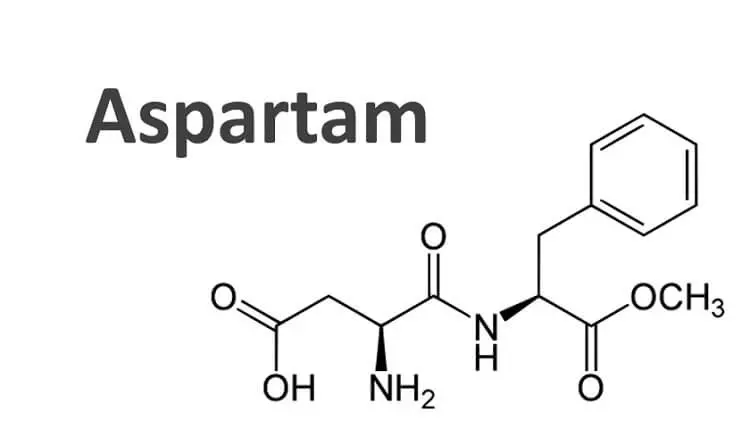
Cho các phát biểu:
Trong aspartame có 1 liên kết peptide và 1 chức ester của methanol
Khi thủy phân APM trong NaOH thì tỷ lệ phản ứng là \(1:3\)
Phần trăm khối lượng nitrogen trong APM là 9,523%
APM được coi là ester của dipeptide
a. Trong aspartame có 1 liên kết amide (chứ không phải liên kết peptide của 2 gốc \(\alpha \)-amino acid).
b. Khi thủy phân APM trong NaOH thì tỷ lệ phản ứng là \(1:3\).
Đáp án đúng là Đúng.
c. CTPT của APM là \({{\rm{C}}_{14}}{{\rm{H}}_{18}}{\rm{\;}}{{\rm{N}}_2}{{\rm{O}}_5}\) có \({\rm{\% }}{\bf{N}} = \frac{{14.2}}{{235}} \cdot 100 \approx 11,91\% \).
Đáp án đúng là Sai.
d. APM được coi là ester của dipeptide.
Đáp án đúng là Đúng.
A là tinh thể muối ngậm nước của kim loại M . Trong A, phần trăm khối lượng các nguyên tố \({\rm{O}},{\rm{S}}\), H lần lượt là \(57,399{\rm{\% }};\ 14,349{\rm{\% }};\ 3,587{\rm{\% }}\); còn lại là của M. Trong dung dịch nước, A phản ứng với \({\rm{BaC}}{{\rm{l}}_2}\) tạo kết tủa trắng không tan trong dung dịch HCl.
Theo dõi sự biến đổi khối lượng của A khi nung nóng dần lên nhiệt độ cao theo sơ đồ sau (biểu diễn sự giảm khối lượng của chất rắn còn lại so với ban đầu):
\(\underset{100 \%}{\mathrm{~A}} \xrightarrow{600^{\circ} \mathrm{C}} \underset{32,287 \%}{\mathrm{X}} \xrightarrow{900^{\circ} \mathrm{C}} \mathrm{M}_3 \mathrm{O}_4\)
Biết M không thuộc họ Lantan và không phóng xạ.
Cho các phát biểu sau:
Tinh thể A là tinh thế muối carbonate của kim loại M
Chất X là muối sulfate khan của kim loại M
Công thức tinh thể A là \({\rm{MnS}}{{\rm{O}}_4} \cdot 4{{\rm{H}}_2}{\rm{O}}\)
Hòa tan oxide \({{\rm{M}}_3}{{\rm{O}}_4}\) vào 100 mL dung dịch \({\rm{FeS}}{{\rm{O}}_4}\ 0,1\ {\rm{M}}\) trong \({{\rm{H}}_2}{\rm{S}}{{\rm{O}}_4}\). Sau khi phản ứng kết thúc, tiến hành chuẩn độ lượng \({\rm{F}}{{\rm{e}}^{2 + }}\) còn lại trong dung dịch bằng dung dịch \({\rm{KMn}}{{\rm{O}}_4}\ 0,05\ {\rm{M}}\) thì cần dùng vừa đủ 25 mL . Khối lượng muối tinh thể A đã đem nung là 1,26 gam. (cho biết \({{\rm{M}}_3}{{\rm{O}}_4}\) sẽ bị \({\rm{F}}{{\rm{e}}^{2 + }}\) khử thành \({{\rm{M}}^{2 + }}\) và làm tròn đáp án đến hàng phần trăm)
a. Nếu A là tinh thể muối carbonate thì khi tác dụng \({\rm{BaC}}{{\rm{l}}_2}\) thu kết tủa là \({\rm{BaC}}{{\rm{O}}_3}\) sẽ tan trong dung dịch HCl.
Đáp án đúng là Sai.
b. Chất X là muối sulfate khan của kim loại M.
Đáp án đúng là Đúng.
c. CTTQ của A là \({{\rm{H}}_{\rm{x}}}{{\rm{S}}_{\rm{y}}}{{\rm{O}}_{\rm{z}}}{{\rm{M}}_{\rm{t}}}\)
Ta có :
\(\begin{array}{*{20}{r}}{x:y:z:t}&{\; = \frac{{3,587{\rm{\% }}}}{1}:\frac{{14,349}}{{32}}:\frac{{57,399}}{{16}}:\frac{{24,665}}{{{M_M}}}}\\{}&{\; = 3,587:0,448:3,587:\frac{{24,665}}{{{M_M}}}}\\{}&{\; = 8:1:8:\frac{{55}}{{{M_M}}}}\end{array}\)
Vậy để là số nguyên thì \({{\rm{M}}_{\rm{M}}}\) là bội của \(55 \Rightarrow {{\rm{M}}_{\rm{M}}} = 55 \Rightarrow {\rm{M}}\) là Mn .
CTTQ của A là \({{\rm{H}}_8}{\rm{S}}{{\rm{O}}_8}{\rm{Mn}}\) mà trong dung dịch A tác dụng \({\rm{BaC}}{{\rm{l}}_2}\) tạo kết tủa trắng.
\( \Rightarrow {\rm{A}}\) chứa gốc \({\rm{S}}{{\rm{O}}_4}{\;^{2 - }}\) nên CTTQ của A có dạng \({\rm{MnS}}{{\rm{O}}_4} \cdot 4{{\rm{H}}_2}{\rm{O}}\).
Đáp án đúng là Đúng.
d. Theo đề ta có : \(\left\{\begin{array}{l}n_{\mathrm{KMnO}_4}=0,025 \cdot 0,05=0,00125 \mathrm{~mol} \\ n_{\mathrm{Fe}^{2+} \mathrm{bd}}=0,1 \cdot 0,1=0,01 \mathrm{~mol}\end{array}\right.\)
Phương trình phản ứng : \(\mathrm{Mn}_3 \mathrm{O}_4+2 \mathrm{FeSO}_4+4 \mathrm{H}_2 \mathrm{SO}_4 \longrightarrow 3 \mathrm{MnSO}_4+\mathrm{Fe}_2\left(\mathrm{SO}_4\right)_3+4 \mathrm{H}_2 \mathrm{O}\)
Phương trình chuẩn độ \(\mathrm{Fe}^{2+}\) còn dư:
\(\left\{\begin{array}{l}\mathrm{MnO}_4^{-}+5 \mathrm{Fe}^{2+}+8 \mathrm{H}^{+} \longrightarrow \mathrm{Mn}^{2+}+5 \mathrm{Fe}^{3+}+4 \mathrm{H}_2 \mathrm{O} \\ 0,00125 \mathrm{~mol}\end{array}\right.\)
Ta có : \({{\rm{n}}_{{\rm{F}}{{\rm{e}}^{2 + }}{\text{còn}}}} = 0,00125.5 = 0,00625{\rm{\;mol}}\)
Số \({\text{mol F}}{{\rm{e}}^{2 + }}\) tham gia khử \({\rm{M}}{{\rm{n}}_3}{{\rm{O}}_4}\) là: \({{\rm{n}}_{{\rm{F}}{{\rm{e}}^{2 + }}{\rm{\;thamgia\;}}}} = 0,01 - 0,00625 = 0,00375{\rm{\;mol}}\)
Thay vào pt ta có : \({{\rm{n}}_{{\rm{M}}{{\rm{n}}_3}{{\rm{O}}_4}}} = \frac{{0,00375}}{2} = 0,001875{\rm{\;mol}}\)
Phương trình nung A: \(\begin{aligned} \mathrm{MnSO}_4 \cdot 4 \mathrm{H}_2 \mathrm{O} \xrightarrow{900^{\circ} \mathrm{C}} & \mathrm{Mn}_3 \mathrm{O}_4 \\ & \leftarrow 0,001875 \mathrm{~mol}\end{aligned}\)
BTNT Mn : \({{\rm{n}}_{{\rm{MnS}}{{\rm{O}}_4}.4{{\rm{H}}_2}{\rm{O}}}} = 0,001875.3 = 0,005625{\rm{\;mol}} \Rightarrow {\rm{\;}}{{\rm{m}}_{{\rm{MnS}}{{\rm{O}}_4}.4{{\rm{H}}_2}{\rm{O}}}}\approx 1,25\ {\rm{gam}}\).
Đáp án đúng là Sai.
Tiến hành thí nghiệm thú vị như sau: trộn \(30{\rm{\% }} - 35{\rm{\% }}\) hydrogen peoxide với chất tẩy rửa. Oxygen được tạo ra sự phân hủy hydrogen peoxide được bao bọc bởi dung dịch chất tẩy rửa sẽ tạo ra bọt bong bóng và chất bọt này sẽ phun ra như một đài phun nước.
Cho phản ứng hóa học như sau: \(2 \mathrm{H}_2 \mathrm{O}_2(\mathrm{l}) \longrightarrow 2 \mathrm{H}_2 \mathrm{O}+\mathrm{O}_2{ }_{(\mathrm{g})}\ \Delta_{\mathrm{r}} \mathrm{H}(\mathrm{l})=-196 \mathrm{~kJ} / \mathrm{mol}\)
Năng lượng hoạt hóa của phản ứng (1) là \({{\rm{E}}_1} = 76{\rm{\;kJ}}/{\rm{mol}}\)
Nếu thêm một lượng nhỏ dung dịch potassium iodide vào dung dịch này, hiệu ứng tạo bọt sẽ rõ ràng hơn. Sau khi thêm dung dịch potassium iodide thì người ta đo được năng lượng hoạt hóa \({{\rm{E}}_2} = 57{\rm{\;kJ}}/{\rm{mol}}\) và nhiệt phản ứng \({{\rm{\Delta }}_{\rm{r}}}{{\rm{H}}_2} = - {\rm{QkJ}}/{\rm{mol}}\). Mặt khác, người ta còn phát hiện rằng các ion iodide sẽ tham gia các phản ứng sau:
(2) \(\mathrm{H}_2 \mathrm{O}_{2(\mathrm{l})}+\mathrm{I}_{(\mathrm{aq})}^{-} \longrightarrow \mathrm{Y}_{(\mathrm{aq})}^{-}+\mathrm{H}_2 \mathrm{O}_{(\mathrm{l})}\)
(3) \(\mathrm{H}_2 \mathrm{O}_{2(\mathrm{l})}+\mathrm{Y}_{(\mathrm{aq})}^{-} \longrightarrow \mathrm{I}_{(\mathrm{aq})}^{-}+\mathrm{H}_2 \mathrm{O}_{(\mathrm{l})}+\mathrm{O}_{2(\mathrm{~g})}\)
Cho biết các phương trình phản ứng theo đúng tỷ lệ mol và coi như thể tích dung dịch thay đổi không đáng kể.
Cho các phát biểu sau:
Giá trị của Q sẽ lớn hơn \(196{\rm{\;kJ}}/{\rm{mol}}\)
Ion \({{\rm{Y}}^ - }\)có công thức là \({\rm{I}}{{\rm{O}}_3}{\;^ - }\)
Trong phản ứng (1) thì \({{\rm{H}}_2}{{\rm{O}}_2}\) đóng vai trò chất oxi hóa và chất khử
Nồng độ \({I^ - }\)sau phản ứng (3) sẽ tăng lên
a. KI chỉ đóng vai trò xúc tác, làm giảm năng lượng hoạt hóa nhưng không làm thay đổi nhiệt phản ứng nên Q = 196.
Đáp án đúng là Sai.
b. theo phương trình thì \({{\rm{Y}}^ - }\)sẽ là \({\rm{I}}{{\rm{O}}^ - }\).
Đáp án đúng là Sai.
c. Trong phản ứng (1) thì \({{\rm{H}}_2}{{\rm{O}}_2}\) đóng vai trò chất oxi hóa và chất khử.
Đáp án đúng là Đúng.
d. \({{\rm{I}}^ - }\)tham gia phản ứng (2) và được trả lại ở phản ứng (3), nên nồng độ không thay đổi.
Đáp án đúng là Sai.
Có 2 chất là: polybuta-1,3-diene và polychloroprene.
Đáp án đúng là 2.

Bộ 50 Đề Thi Thử Tốt Nghiệp THPT Giáo Dục Kinh Tế Và Pháp Luật Năm 2026 – Theo Cấu Trúc Đề Minh Họa Bộ GD&ĐT

Bộ 50 Đề Thi Thử Tốt Nghiệp THPT Lịch Sử Học Năm 2026 – Theo Cấu Trúc Đề Minh Họa Bộ GD&ĐT

Bộ 50 Đề Thi Thử Tốt Nghiệp THPT Công Nghệ Năm 2026 – Theo Cấu Trúc Đề Minh Họa Bộ GD&ĐT

Bộ 50 Đề Thi Thử Tốt Nghiệp THPT Môn Hóa Học Năm 2026 – Theo Cấu Trúc Đề Minh Họa Bộ GD&ĐT

Bộ 50 Đề Thi Thử Tốt Nghiệp THPT Môn Sinh Học Năm 2026 – Theo Cấu Trúc Đề Minh Họa Bộ GD&ĐT

Bộ 50 Đề Thi Thử Tốt Nghiệp THPT Môn Vật Lí Năm 2026 – Theo Cấu Trúc Đề Minh Họa Bộ GD&ĐT
ĐĂNG KÝ GÓI THI VIP
- Truy cập hơn 100K đề thi thử và chính thức các năm
- 2M câu hỏi theo các mức độ: Nhận biết – Thông hiểu – Vận dụng
- Học nhanh với 10K Flashcard Tiếng Anh theo bộ sách và chủ đề
- Đầy đủ: Mầm non – Phổ thông (K12) – Đại học – Người đi làm
- Tải toàn bộ tài liệu trên TaiLieu.VN
- Loại bỏ quảng cáo để tăng khả năng tập trung ôn luyện
- Tặng 15 ngày khi đăng ký gói 3 tháng, 30 ngày với gói 6 tháng và 60 ngày với gói 12 tháng.