Câu hỏi:
Resveratrol có tác dụng chống khối u và công thức cấu tạo của nó như sau:
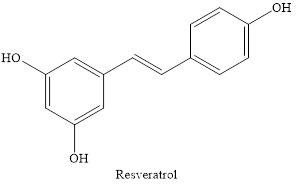
Phát biểu nào sau đây là sai?
Đáp án đúng: C
C. Sai vì resveratrol là hợp chất có nhóm chức phenol (tính acid chỉ mạnh hơn nấc thứ 2 của acid carbonic nên tác dụng được \(\mathrm{Na}_{2} \mathrm{CO}_{3}\) chứ không tác dụng được \(\mathrm{NaHCO}_{3}\) ).
Câu hỏi này thuộc đề thi trắc nghiệm dưới đây, bấm vào Bắt đầu thi để làm toàn bài
Tuyển Tập Đề Thi Tham Khảo Tốt Nghiệp THPT Năm 2025 - Hóa Học - Bộ Đề 06 giúp học sinh lớp 12 ôn tập hiệu quả và tự tin bước vào kỳ thi Tốt nghiệp THPT năm 2025. Mỗi đề thi trong tài liệu được xây dựng theo đúng cấu trúc chuẩn của Bộ Giáo dục và Đào tạo, bao gồm ba phần: trắc nghiệm nhiều lựa chọn, trắc nghiệm đúng – sai và trắc nghiệm trả lời ngắn. Các câu hỏi được chọn lọc kỹ lưỡng, bám sát nội dung chương trình, tích hợp kiến thức liên môn và có độ phân hóa phù hợp, giúp học sinh không chỉ ôn tập lý thuyết mà còn rèn luyện kỹ năng giải đề thực tiễn. Đặc biệt, phần đáp án và hướng dẫn giải chi tiết đi kèm giúp học sinh dễ dàng tự đánh giá kết quả và nhận diện các dạng bài quan trọng.
Câu hỏi liên quan
A. Sai vì theo bảng thông thì nhiệt lượng tỏa ra khi đốt cháy 1 mol các chất là \(373+337+317=1027\) kcal.
B. Sai vì độ dài liên kết \(\mathrm{C}-\mathrm{C}\) càng ngắn thì năng lượng để phá vỡ càng cao.
C. Đúng vì ta có phương trình cháy các chất như sau:
\(\mathrm{C}_{2} \mathrm{H}_{6}+\frac{7}{2} \mathrm{O}_{2} \longrightarrow 2 \mathrm{CO}_{2}+3 \mathrm{H}_{2} \mathrm{O}\)
\(\mathrm{C}_{2} \mathrm{H}_{4}+3 \mathrm{O}_{2} \longrightarrow 2 \mathrm{CO}_{2}+2 \mathrm{H}_{2} \mathrm{O}\)
\(\mathrm{C}_{2} \mathrm{H}_{2}+2 \mathrm{O}_{2} \longrightarrow 2 \mathrm{CO}_{2}+\mathrm{H}_{2} \mathrm{O}\)
Nhiệt lượng trung bình tính trên 1 mol sản phẩm lần lượt là: \(\left\{\begin{array}{l}\text { ethane : } \frac{373}{5}=74,6 \\ \text { ethylene : } \frac{337}{4}=84,25 \\ \text { acetylene : } \frac{317}{3}=105,6\end{array}\right.\)
D. Sai vì theo bảng thông tin thì \(\frac{\mathrm{E}_{\mathrm{b}(\mathrm{C}=\mathrm{C})}}{\mathrm{E}_{\mathrm{b}(\mathrm{C}-\mathrm{C})}}=\frac{231}{90}=2,56\) lần.
Methyl benzoate là một chất lỏng, không màu, có mùi dễ chịu và được sử dụng trong nước hoa) Nhóm học sinh A tiến hành điều chế methyl benzoate trong phòng thí nghiệm như sau:
Cho 12,2 gam benzoic acid và 20 mL methanol (khỏi lượng riêng \(0,79 \mathrm{g} / \mathrm{mL}\) ) vào bình cầu đáy tròn, lắc đều hỗn hợp.
Thêm \(3,0 \mathrm{mL}\) sulfuric acid đậm đặc vào, lắc nhẹ để các chất trộn đều với nhau.
Cho cá từ vào bình cầu, gắn bình cầu vào ống sinh hàn rồi tiền hành đun nóng trên máy khuấy từ gia nhiệt trong 1 giờ.
Để tách được methyl benzoate khỏi hỗn hợp, nhóm học sinh tiến hành theo sơ đồ sau:
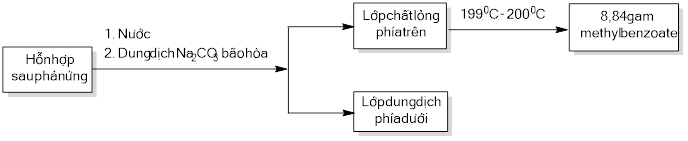
Phương trình xảy ra là \(\mathrm{C}_{6} \mathrm{H}_{5} \mathrm{COOH}+\mathrm{CH}_{3} \mathrm{OH} \stackrel{\mathrm{H}_{2} \mathrm{SO}_{4 \mathrm{d}}, \mathrm{t}^{\circ} \mathrm{C}}{\Longleftrightarrow} \mathrm{C}_{6} \mathrm{H}_{5} \mathrm{COOCH}_{3}+\mathrm{H}_{2} \mathrm{O}\)
Vai trò của sulfuric acid trong thí nghiệm là xúc tác và hút nước làm cân băng chuyến dịch sang phải
Việc thêm dung dịch \(\mathrm{Na}_{2} \mathrm{CO}_{3}\) vào là để pha loãng sulfuric acid còn dư
Hiệu suất của phản ứng ester hóa là \(70 \%\)
a. Đúng.
b. Đúng.
c. Sai
vì thêm \(\mathrm{Na}_{2} \mathrm{CO}_{3}\) bão hoà để trung hoà sulfuric acid và benzoic acid dư.
d. Sai
vì theo sơ đồ tách thì ta có \(\left\{\begin{array}{l}\mathrm{n}_{\mathrm{CH}_{3} \mathrm{OH}}=\frac{20.0,79}{32}=0,494 \mathrm{mol} \\ \mathrm{n}_{\mathrm{C}_{6} \mathrm{H}_{5} \mathrm{COOH}}=\frac{12,2}{123}=0,1 \mathrm{mol} \\ \mathrm{n}_{\text {esterthu }}=\frac{8,84}{136}=0,065 \mathrm{mol}\end{array}\right.\)
Vì \(\mathrm{n}_{\mathrm{CH}_{3} \mathrm{OH}}>\mathrm{n}_{\mathrm{C}_{6} \mathrm{H}_{5} \mathrm{COOH}}\) mà tỷ lệ phản ứng là \(1: 1\) nên hiệu suất tính theo benzoic acid.
Ta có: \(\mathrm{H} \%=\frac{0,065}{0,1} . 100=65 \%\).
Remdesivir (kí hiệu: R) là thuốc chống virus được dùng rất thành công để khống chế dịch MERSCoV năm 2012. Remdesivir đã được cấp phép sử dụng điều trị SARS-CoV-2 ở người và vẫn đang tiếp tục được cải tiến để tạo ra thuốc đặc trị. Phân tử \(\mathbf{R}\) có công thức cấu tạo như sau:
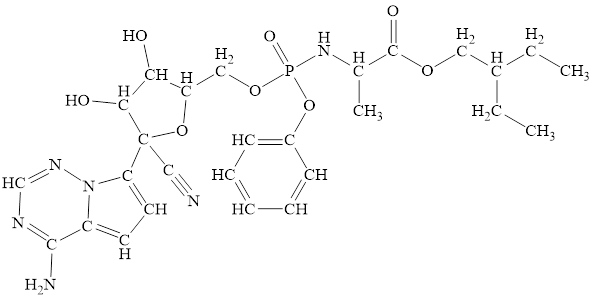
Công thức phân tử của \(\mathbf{R}\) là \(\mathrm{C}_{27} \mathrm{H}_{\mathrm{x}} \mathrm{N}_{\mathrm{y}} \mathrm{O}_{\mathrm{z}} \mathrm{P}\). Giá trị của \(\mathrm{x}, \mathrm{y}, \mathrm{z}\) lần lượt là \(35 ; 8 ; 6\)
Biết khối lượng mol phân tử của \(\mathbf{R}\) là \(\mathrm{M}_{\mathbf{R}}=602 \mathrm{g} / \mathrm{mol}\). Phần trăm khối lượng các nguyên tố carbon trong \(\mathbf{R}\) là \(56 \%\)
Tổng số liên kết \(\pi\) của \(R\) là 10
Đun nóng \(\mathbf{R}\) trong môi trường kiềm thu được hỗn hợp sản phẩm trong đó có chứa chất \(\mathbf{Y}\). Biết \(\mathbf{Y}\) có tính chất hóa học rất giống với ethyl alcohol. Công thức cấu tạo của \(\mathbf{Y}\) là \(\left(\mathrm{CH}_{3} \mathrm{CH}_{2}\right)_{2} \mathrm{CHCH}_{2} \mathrm{OH}\)
a. Sai
vì công thức phân tử của R là \(\mathrm{C}_{27} \mathrm{H}_{35} \mathrm{N}_{6} \mathrm{O}_{8} \mathrm{P}\) nên giá trị \(\mathrm{x}, \mathrm{y}, \mathrm{z}\) lần lượt là \(36 ; 6 ; 8\).
b. Sai
vì phần trăm nguyên tố carbon là \(\% \mathrm{C}=\frac{27 . 12}{602} . 100=53,8 \%\)
c. Sai
vì tổng số liên kết \(\pi\) trong \(R\) là 11.
d. Đúng
vì khi đun nóng với kiềm thì R bị thủy phân cho alcohol có CTCT là \(\left(\mathrm{CH}_{3} \mathrm{CH}_{2}\right)_{2} \mathrm{CHCH}_{2} \mathrm{OH}\).
Quá trình nung một muối hydrate trong khí quyển Ar ở các nhiệt độ khác nhau và phần trăm khối lượng chất rắn còn lại so với khối lượng ban đầu (100\%) được cho trong sơ đồ sau:
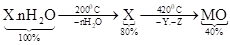
Cho biết MO là một oxide của kim loại M , trong đó M chiếm \(77,78 \%\) khối lượng. Y và Z là các chất khí được tạo thành có số mol bằng nhau. Y cháy trong không khí tạo thành Z. Cho hỗn hợp khí Y và Z vào nước vôi trong, thấy có tạo thành kết tủa. Cho các phát biểu sau:
Trong hai khí Y hoặc \(Z\) có một khí là \(\mathrm{SO}_{2}\)
Trong tinh thể \(\mathrm{X} . \mathrm{nH}_{2} \mathrm{O}\) thì giá trị n là 2
Công thức phân tử của X là \(\mathrm{CaC}_{2} \mathrm{O}_{4}\)
Thành phần phần trăm theo khối lượng của kim loại trong tinh thể \(\mathrm{X}. \mathrm{nH}_{2} \mathrm{O}\) là \(31,1 \%\) (cho phép làm tròn đáp án đến hàng phần mười)
Theo đề cho ta có: \(77,78=\frac{\mathrm{M}_{\mathrm{M}}}{\mathrm{M}_{\mathrm{M}}+16} . 100 \Rightarrow \mathrm{M}_{\mathrm{M}}=56 \xrightarrow{\text { CToxide }} \mathrm{FeO}\)
Theo sơ đồ nung ta có: \(\left\{\begin{array}{l}m_{\mathrm{FeO}}=40 \% m_{\mathrm{X}. n \mathrm{H}_{2} \mathrm{O}} \Rightarrow 40=\frac{M_{\mathrm{FeO}}}{M_{\mathrm{X}. n \mathrm{H}_{2} \mathrm{O}}}.100 \Rightarrow M_{\mathrm{X}. n \mathrm{H}_{2} \mathrm{O}}=180 \\ m_{\mathrm{X}}=80 \% m_{\mathrm{X}. n \mathrm{H}_{2} \mathrm{O}} \Rightarrow 80=\frac{M_{\mathrm{X}}}{M_{\mathrm{X}. n \mathrm{H}_{2} \mathrm{O}}}.100 \Leftrightarrow 80=\frac{M_{\mathrm{X}}}{180}.100 \Rightarrow M_{\mathrm{X}}=144\end{array}\right.\)
Từ giai đoạn: \(\underbrace{\mathrm{X}. \mathrm{nH}_{2} \mathrm{O}}_{100 \%} \xrightarrow{-{ }^{200^{\circ} \mathrm{C}}} \mathrm{X} \mathrm{H}_{2} \mathrm{O} \underset{80 \%}{\mathrm{X}} \Rightarrow \mathrm{n}.18=180-144 \Rightarrow \mathrm{n}=2\)
Từ giai đoạn: \(\underset{80 \%}{\mathrm{X}} \xrightarrow[-\mathrm{Y}. \mathrm{Z}]{420^{\circ} \mathrm{C}} \underset{40 \%}{\mathrm{FeO}} \Rightarrow \mathrm{M}_{\mathrm{Y}}+\mathrm{M}_{\mathrm{Z}}=144-72=72\)
Theo đề thì cho \(\mathrm{Y}, \mathrm{Z}\) vào nước vôi trong thì có kết tủa \(\Rightarrow\) Trong hỗn hợp khí có thể chứa \(\mathrm{CO}_{2}\) hoặc \(\mathrm{SO}_{2}\).
Tuy nhiên \(\mathrm{M}_{\mathrm{SO}_{2}}=72=\mathrm{M}_{\mathrm{Y}}+\mathrm{M}_{\mathrm{Z}} \Rightarrow\) vô lí nên khí chọn là \(\mathrm{CO}_{2}\).
Khí Y cháy trong không khí tạo Z nên Z là \(\mathrm{CO}_{2}\) và Y là \(\mathrm{CO} \Rightarrow \mathrm{X}\) chứa \(\mathrm{FeO}, \mathrm{CO}_{2}, \mathrm{CO}\)
CTTQ của X là \(\mathrm{FeC}_{2} \mathrm{O}_{4} \Rightarrow\) tinh thể là \(\mathrm{FeC}_{2} \mathrm{O}_{4} . 2 \mathrm{H}_{2} \mathrm{O}\)
a. Sai
vì trong hai khí \(\mathrm{Y}, \mathrm{Z}\) không có khí nào là \(\mathrm{CO}_{2}\).
b. Đúng.
c. Sai.
d. Đúng
vì %Fe trong \(\mathrm{FeC}_{2} \mathrm{O}_{4} . 2 \mathrm{H}_{2} \mathrm{O}=\frac{56}{180} . 100=31,1 \%\).
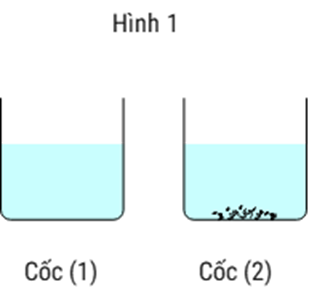
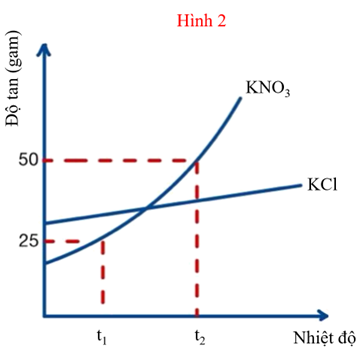
Ở nhiệt độ \(\mathrm{t}_{1}{ }^{\circ} \mathrm{C}\), cho cùng khối lượng m gam hai chất \(\mathrm{KNO}_{3}\) và KCl vào 2 cốc có chứa 100 gam nước và khuấy đều. Hiện tượng thể hiện ở hình 1 và cho đường cong hòa tan của 2 chất ở hình 2.
Cho các phát biểu:
Chất tan trong cốc (1) là potassium chloride
Ở \(\mathrm{t}_{1}{ }^{\circ} \mathrm{C}\), nồng độ phần trăm của chất tan trong cốc (2) là \(20 \%\)
Khi tăng nhiệt độ từ \(\mathrm{t}_{1}{ }^{\circ} \mathrm{C}\) lên \(\mathrm{t}_{2}{ }^{\circ} \mathrm{C}\), khuấy đều thì khối lượng chất tan trong 2 cốc là như nhau
Nếu \(\mathrm{KNO}_{3}\) có lẫn một ít KCl thì có thể tinh chế \(\mathrm{KNO}_{3}\) bằng phương pháp bay hơi và kết tinh
a. Đúng
vì theo đường cong độ tan thì tại \(\mathrm{t}_{1}{ }^{\circ} \mathrm{C}\) thì độ tan của KCl lớn hơn hơn \(\mathrm{KNO}_{3}\)
Theo hình (1) thì có 1 cốc tan hết còn 1 cốc vẫn còn chất rắn chưa tan.
Từ đồ thị ta thấy: độ tan của KCl tại \(\mathrm{t}_{1}\) là 25 gam và \(\mathrm{KNO}_{3}\) có độ tan \(>25\) gam (khoảng 32 gam).
nếu khối lượng 2 chất đã lấy \(m<25\) gam thì cả 2 chất đều sẽ tan hoàn toàn : loại vì không khớp với hình (1).
Nếu khối lượng 2 chất đã lấy \(\mathrm{m}>32\) thì cả 2 chất đều sẽ còn 1 phần không tan (do vượt độ tan để tạo dung dịch bão hòa).
Nếu khối lượng 2 chất đã lấy \(25 \leq \mathrm{m}<32\) thì \(\mathrm{KNO}_{3}\) sẽ tan hoàn toàn và \(\mathrm{KNO}_{3}\) sẽ còn 1 phần không tan.
b. Đúng
vì theo ý a thì cốc (2) là cốc chứa \(\mathrm{KNO}_{3}\), tại \(\mathrm{t}_{1}{ }^{\circ} \mathrm{C}\) lượng chất tan là 25 gam nên nồng độ phần trăm là \(\% \mathrm{C}=\frac{25}{100+25}.100=20 \%\).
c. Đúng
vì theo suy luận ở (a) thì \(25 \leq \mathrm{m}<32\) mà tại \(\mathrm{t}_{2}\) thì độ tan các chất đều lớn hơn 32 nên 2 chất tan hoàn toàn.
d. Đúng
vì độ tan của \(\mathrm{KNO}_{3}\) và KCl khác nhau và sự thay đổi theo nhiệt độ cũng khác nhau nên có thể tách bằng phương pháp bay hơi và kết tinh.

Bộ 50 Đề Thi Thử Tốt Nghiệp THPT Giáo Dục Kinh Tế Và Pháp Luật Năm 2026 – Theo Cấu Trúc Đề Minh Họa Bộ GD&ĐT

Bộ 50 Đề Thi Thử Tốt Nghiệp THPT Lịch Sử Học Năm 2026 – Theo Cấu Trúc Đề Minh Họa Bộ GD&ĐT

Bộ 50 Đề Thi Thử Tốt Nghiệp THPT Công Nghệ Năm 2026 – Theo Cấu Trúc Đề Minh Họa Bộ GD&ĐT

Bộ 50 Đề Thi Thử Tốt Nghiệp THPT Môn Hóa Học Năm 2026 – Theo Cấu Trúc Đề Minh Họa Bộ GD&ĐT

Bộ 50 Đề Thi Thử Tốt Nghiệp THPT Môn Sinh Học Năm 2026 – Theo Cấu Trúc Đề Minh Họa Bộ GD&ĐT

Bộ 50 Đề Thi Thử Tốt Nghiệp THPT Môn Vật Lí Năm 2026 – Theo Cấu Trúc Đề Minh Họa Bộ GD&ĐT
ĐĂNG KÝ GÓI THI VIP
- Truy cập hơn 100K đề thi thử và chính thức các năm
- 2M câu hỏi theo các mức độ: Nhận biết – Thông hiểu – Vận dụng
- Học nhanh với 10K Flashcard Tiếng Anh theo bộ sách và chủ đề
- Đầy đủ: Mầm non – Phổ thông (K12) – Đại học – Người đi làm
- Tải toàn bộ tài liệu trên TaiLieu.VN
- Loại bỏ quảng cáo để tăng khả năng tập trung ôn luyện
- Tặng 15 ngày khi đăng ký gói 3 tháng, 30 ngày với gói 6 tháng và 60 ngày với gói 12 tháng.