Câu hỏi:
Cho độ âm điện của N bằng 3,04; của H bằng 2,2; của C bằng 2,55; của O bằng 3,44.
Phân tử \(\mathrm{NO}_2\) và \(\mathrm{NH}_3\) tuân theo quy tắc octet; \(\mathrm{CH}_4\) và \(\mathrm{H}_2 \mathrm{O}\) vi phạm quy tắc octet.
Dung dịch \(\mathrm{NH}_3\) có thể tạo được tối đa 4 loại liên kết hydrogen.
Nhiệt độ sôi của \(\mathrm{H}_2 \mathrm{O}\) cao hơn nhiều so với \(\mathrm{CH}_4\) nhờ có liên kết hydrogen.
Nguyên tử C trong phân tử \(\mathrm{CH}_4\) còn một cặp electron chưa tham gia liên kết.
Đáp án đúng: Sai, Đúng, Đúng, Sai
- \(\mathrm{NH}_3, \mathrm{CH}_4, \mathrm{H}_2 \mathrm{O}: \mathrm{N}, \mathrm{C}, \mathrm{O}\) trong các phân tử này đều có 8 electron lớp ngoài cùng (tuân theo octet).Nguyên tử N trong \(\mathrm{NO}_2\) chỉ có 7 electron lớp ngoài cùng, nên vi phạm quy tắc octet. \(\Rightarrow\) a) Sai.
- Dung dịch \(\mathrm{NH}_3\) có thể tạo tối đa 4 loại liên kết hydrogen \(\Rightarrow\) b) Đúng.
- \(\mathrm{H}_2 \mathrm{O}\) tạo được liên kết hydrogen mạnh mẽ (nhờ O có độ âm điện cao và kích thước nhỏ), làm tăng nhiệt độ sôi. \(\mathrm{CH}_4\) là phân tử không phân cực, chỉ có lực van der Waals rất yếu. \(\Rightarrow \mathrm{c}\) ) Đúng.
- C đã sử dụng hết 4 electron hóa trị để tạo liên kết và không còn cặp electron không liên kết nào. \(\Rightarrow \mathrm{d})\) Sai.
Câu hỏi này thuộc đề thi trắc nghiệm dưới đây, bấm vào Bắt đầu thi để làm toàn bài
Bộ Đề Kiểm Tra Học Kì I - Hóa Học 10 - Kết Nối Tri Thức Với Cuộc Sống - Bộ Đề 01 gồm các đề luyện tập bám sát chương trình học. Nội dung bao quát các chuyên đề trọng tâm như cấu tạo nguyên tử, bảng tuần hoàn và liên kết hóa học. Các dạng câu hỏi trắc nghiệm và tự luận giúp học sinh ôn tập, củng cố kiến thức và rèn luyện kỹ năng làm bài. Bộ đề phù hợp cho việc chuẩn bị trước kỳ kiểm tra học kì I.
Câu hỏi liên quan

Trọn Bộ Giáo Án Word & PowerPoint Tiếng Anh 12 – I-Learn Smart World – Năm Học 2025-2026

Trọn Bộ Giáo Án Word & PowerPoint Tiếng Anh 12 – Global Success – Năm Học 2025-2026

Trọn Bộ Giáo Án Word & PowerPoint Hóa Học 12 – Kết Nối Tri Thức – Năm Học 2025-2026

Trọn Bộ Giáo Án Word & PowerPoint Hóa Học 12 – Chân Trời Sáng Tạo – Năm Học 2025-2026

Trọn Bộ Giáo Án Word & PowerPoint Công Nghệ 12 – Kết Nối Tri Thức – Năm Học 2025-2026

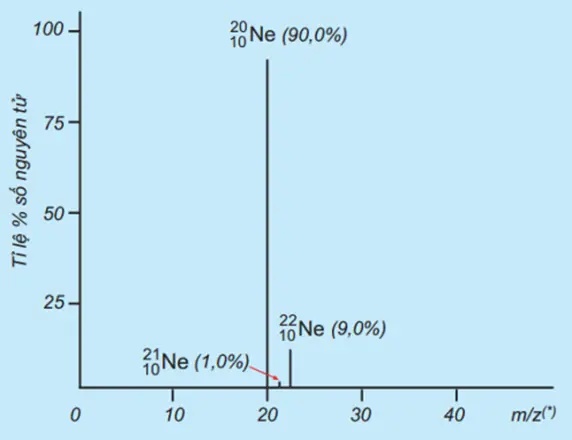 Trục tung biểu thị hàm lượng phần trăm về số nguyên tử của từng đòng vị, trục hoành biểu thị tỉ số của nguyên tử khối (m) của mỗi đồng vị với điện tích của các ion đồng vị tương ứng (điện tích z của các ion đồng vị neon đều bằng +1). Nguyên tử khối trung bình của Neon là?
Trục tung biểu thị hàm lượng phần trăm về số nguyên tử của từng đòng vị, trục hoành biểu thị tỉ số của nguyên tử khối (m) của mỗi đồng vị với điện tích của các ion đồng vị tương ứng (điện tích z của các ion đồng vị neon đều bằng +1). Nguyên tử khối trung bình của Neon là?