Câu hỏi:
Sáp ong do ong thợ tiết ra, xây dựng thành tổ ong để lưu trữ mật ong và bảo vệ ấu trùng. Sáp ong có thành phần chính là triacontanyl palmitate \(\left( {{{\rm{C}}_{15}}{{\rm{H}}_{31}}{\rm{COO}}{{\rm{C}}_{30}}{{\rm{H}}_{61}}} \right)\). Ester này thuộc loại
Đáp án đúng: C
Triacontanyl palmitate: \(\mathrm{C}_{15} \mathrm{H}_{31}-\mathrm{COO}-\mathrm{C}_{30} \mathrm{H}_{61}\) : gốc acid no \(\left(\mathrm{C}_{15} \mathrm{H}_{31} \mathrm{CO}-\right)\) và gốc rượu no \(\left(\mathrm{C}_{30} \mathrm{H}_{61}-\right) \rightarrow\) ester no, đơn chức.
Đáp án đúng là C.
Câu hỏi này thuộc đề thi trắc nghiệm dưới đây, bấm vào Bắt đầu thi để làm toàn bài
Tuyển Tập Đề Thi Tham Khảo Tốt Nghiệp THPT Năm 2026 – Hoá Học – Bộ Đề 01Tài liệu tổng hợp các đề thi tham khảo bám sát cấu trúc đề tốt nghiệp THPT mới nhất năm 2026.Nội dung bao quát đầy đủ các chuyên đề Hoá học lớp 10, 11 và 12.Câu hỏi được phân hóa hợp lý, giúp rèn luyện kỹ năng tư duy và làm bài.Phù hợp cho học sinh ôn tập, tự đánh giá năng lực và chuẩn bị cho kỳ thi chính thức.
Câu hỏi liên quan
A. Đúng: Hexamethylenediamine và adipic acid đều là monomer đa chức (diamin và diacid).
Đáp án đúng là A.
(a) Acid formic (Y) có nhóm carboxyl ( \(-C O O H\)) tạo liên kết hydrogen với nước bền vững và mạnh hơn so với nhóm hydroxyl ( \(-O H\)) của ethanol (X).→ (a) sai.
(b) \(\mathrm{HCOOH}\left(100,8^{\circ} \mathrm{C}\right), \mathrm{C}_2 \mathrm{H}_5 \mathrm{OH}\left(78^{\circ} \mathrm{C}\right), \mathrm{C}_2 \mathrm{H}_5 \mathrm{NH}_2 \left(17^{\circ} \mathrm{C}\right), \mathrm{C}_3 \mathrm{H}_8\left(-42^{\circ} \mathrm{C}\right) \rightarrow\) đúng.
(c) \(\mathrm{Y}(\mathrm{HCOOH})\) cho môi trường acid. Tuy nhiên, \(\mathrm{T}\left(\mathrm{CH}_3 \mathrm{CH}_2 \mathrm{NH}_2\right)\) là một amine, khi tan trong nước sẽ cho môi trường base. Chỉ có \(X\) và \(Z\) là trung tính ( \(Z\) thực tế gần như không tan). → sai.
(d) \(\mathrm{X}+\mathrm{Y}\) (có \(\mathrm{H}_2 \mathrm{SO}_4\) đặc) → ester etyl fomiat \(\left(\mathrm{HCOOC}_2 \mathrm{H}_5\right)\) mùi thơm → đúng.
(e) Z là \(\mathrm{C}_3 \mathrm{H}_8\) (khí) có áp suất hơi cao nhất → đúng.
Vậy có 3 phát biểu đúng.
Đáp án đúng là B.
Dựa vào công thức \(Q_C=\frac{\left[\mathrm{NH}_3\right]^2}{\left[\mathrm{~N}_2\right] \cdot\left[\mathrm{H}_2\right]^3}\) :
- Nồng độ các chất (\(C=\frac{n}{V}\) với \(V=1 \mathrm{~L}\)): \(\left[N_2\right]=0,28 \mathrm{M}\); \(\left[H_2\right]=0,16 \mathrm{M}\); \(\left[N H_3\right]= 0,54 \mathrm{M}\).
- \(Q_C=\frac{(0,54)^2}{0,28 \cdot(0,16)^3}=\frac{0,2916}{0,28 \cdot 0,004096}=\frac{0,2916}{0,00114688} \approx 254,26\).
Ta thấy \(Q_C \approx 254,26>K_C=64\).
Kết luận: Hệ chưa đạt trạng thái cân bằng. Vì \(Q_C>K_C\), phản ứng sẽ chuyển dịch theo chiểu nghịch (từ phải sang trái) để làm giảm nồng độ \(\mathrm{NH}_3\) và tăng nồng độ \(\mathrm{N}_2, \mathrm{H}_2\) cho đến khi đạt cân bằng.
Phản ứng nghịch: \(2 \mathrm{NH}_3(\mathrm{g}) \rightarrow \mathrm{N}_2(\mathrm{g})+3 \mathrm{H}_2(\mathrm{g})\).
Tổng số mol khí tăng từ 2 mol lên \(4\ \mathrm{mol}\ (1+3)\). Do đó, áp suất của hệ sẽ tăng lên.
Đáp án đúng là C.
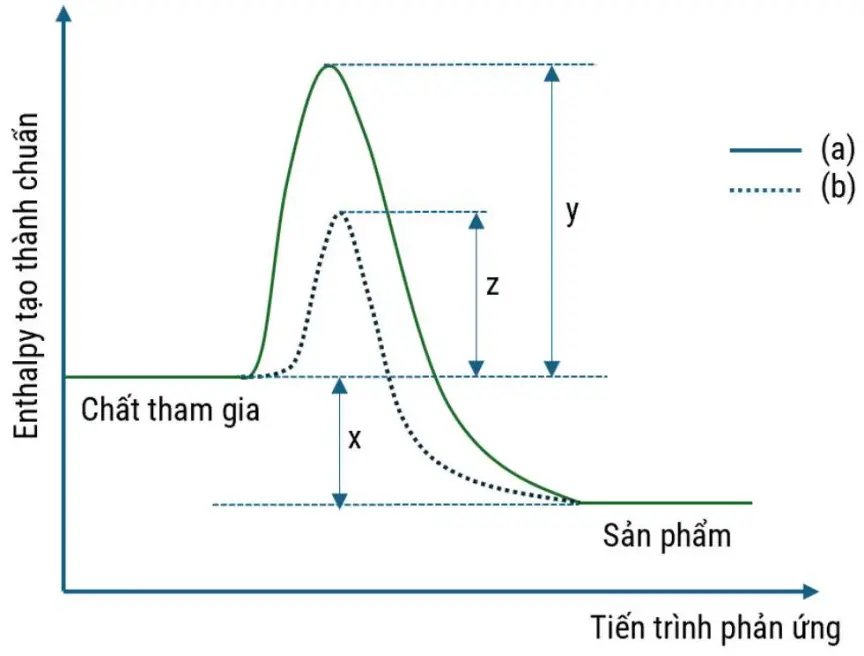
Năng lượng hoạt hóa của phản ứng khi không dùng xúc tác có giá trị là y và \({\rm{y}} > 0\) là phát biểu đúng.
Đáp án đúng là C.
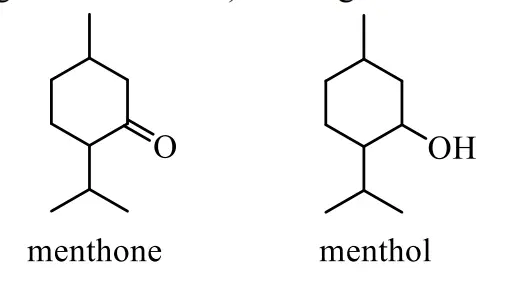
A. Phổ IR của menthol có hấp thụ \(\sim 1700 \mathrm{~cm}^{-1} \rightarrow \text{sai}\), vì \(1700 \mathrm{~cm}^{-1}\) là đặc trưng nhóm \(\mathrm{C}=\mathrm{O}\) (ketone), menthol không có \(\mathrm{C}=\mathrm{O}\), chỉ có nhóm \(\mathrm{OH}\left(\sim 3200-3600 \mathrm{~cm}^{-1}\right)\).
B. Oxi hóa menthone bằng \(\mathrm{NaBH}_4\) hoặc \(\mathrm{LiAlH}_4\) thu được menthol → sai, vì \(\mathrm{NaBH}_4\), \(\mathrm{LiAlH}_4\) là chất khử, không phải oxi hóa. Khử menthone (ketone) → menthol (ancol) mới đúng.
C . Đúng.
D. Menthol thuộc phenol → sai, vì phenol có nhóm -OH gắn trực tiếp vào vòng thơm, menthol là alcol no (vòng không thơm).
Đáp án đúng là C.
Cho phản ứng tách nước của ethanol (có xúc tác \({\rm{A}}{{\rm{l}}_2}{{\rm{O}}_3}\) ở nhiệt độ cao \( > 500{\rm{\;K}}\)) như sau: \(\mathrm{C}_2 \mathrm{H}_5 \mathrm{OH}_{(\mathrm{g})} \longrightarrow \mathrm{C}_2 \mathrm{H}_4(\mathrm{~g})+\mathrm{H}_2 \mathrm{O}_{(\mathrm{g})}\)
Nếu phản ứng thực hiện trong một bình kín, tổng áp suất khí trong bình đo được tại các thời điểm khác nhau thể hiện ở đồ thị sau đây:
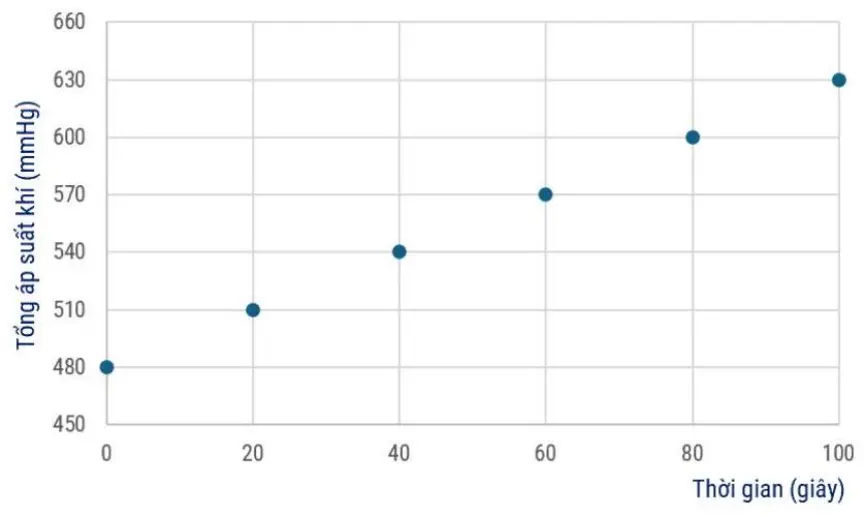
Cho biết công thức tính vận tốc tức thời của phản ứng trên là \(v = k \cdot {P_{{{\rm{C}}_2}{{\rm{H}}_5}{\rm{OH}}}}\) và \(k = \frac{{{{\rm{P}}_{{{\rm{C}}_2}{{\rm{H}}_5}{\rm{OH}}\left( {{{\rm{t}}_1}} \right)}} - {{\rm{P}}_{{{\rm{C}}_2}{{\rm{H}}_5}{\rm{OH}}\left( {{{\rm{t}}_2}} \right)}}}}{{{t_2} - {t_1}}}\)
Cho các phát biểu sau:
Thời gian để lượng ethanol giảm đi một nửa so với ban đầu là 160 giây
Hằng số tốc độ của phản ứng là \(15\ {\rm{mmHg}}/{\text{s}}\)
Ở giây thứ 40, tốc độ tạo thành của \({{\rm{C}}_2}{{\rm{H}}_4}\) là \(1,5\ {\rm{mmHg}}/{\text{s}}\)
Khi thời gian phản ứng là 50 giây thì áp suất riêng của ethanol là \(405\ {\rm{mmHg}}/{\text{s}}\)
Dầu diesel sinh học là một trong những nguồn năng lượng bền vững có tiềm năng phát triển để thay thế dầu mỏ. Nó có thể được sử dụng làm nhiên liệu trực tiếp hoặc trộn với dầu diesel hóa dầu. Biodiesel là este monoalkyl của acid béo và có thể thu được từ dầu ăn và chất béo thải thông qua phản ứng trao đổi ester,như sau: Phản ứng trao đổi ester có thể được thực hiện bằng xúc tác kiếm hoặc enzyme. Người ta thường dùng nó để chế tạo nhiên liệu sinh học.
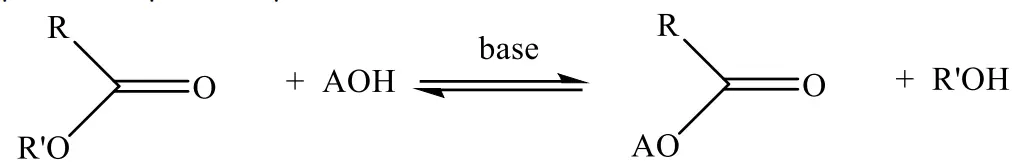
Thực hiện điều chế biodiesel trong phòng thí nghiệm như sau: Hòa tan 0,12 gam potassium hydroxide trong 3 mL methanol (khoảng \(0,074{\rm{\;mol}}\) ) rồi cho vào ống nghiệm, sau đó thêm 12 mL dầu ăn thải (khoảng 0,012 mol), trộn đều và đun nóng để hoàn tất phản ứng. Phương trình phản ứng như sau:
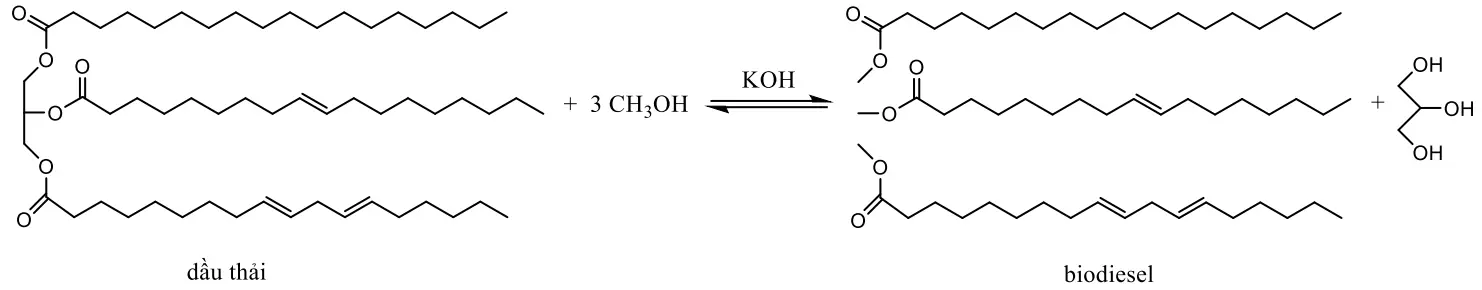
Cho biết thành phần chính của dầu diesel từ dầu mỏ là alkane mạch thẳng, alkane vòng hoặc hydrocacbon thơm chứa 15 đến 20 nguyên tử carbon. Cho các phát biểu sau:
Biodiesel có liên kết đôi \({\rm{C}} = {\rm{C}}\) không no có thể tham gia quá trình hydrogen hóa
Biodiesel là một hợp chất hữu cơ có tính acid
Lượng glycerol thu được sau phản ứng là 1,1 gam (cho phép làm tròn đáp án đến hàng phần mười)
Hàm lượng nguyên tử oxygen của biodiesel cao hơn so với dầu diesel từ dầu mỏ (xét cùng 1 mol chất)
Để khám phá tính chất của Cu, người ta tiến hành thì nghiệm sau đây:
Thí nghiệm 1: Lấy một lượng bột đồng thích hợp cho vào ống nghiệm chứa dung dịch \({\rm{FeC}}{{\rm{l}}_3}\) màu vàng nâu \(0,1{\rm{M}}\). Sau khi phản ứng xảy ra, dung dịch chuyển sang màu xanh, cho thấy \({\rm{CuC}}{{\rm{l}}_2}\) được tạo thành. Sau 2 ngày, dung dịch chuyển sang màu xanh nhạt và xuất hiện kết tủa màu trắng. Sau khi kiểm tra, thấy kết tủa màu trắng là CuCl .
Thí nghiệm 2: Cho dung dịch màu xanh lam trong suốt ở thí nghiệm 1 vào ống nghiệm, nhỏ dung dịch KSCN \(0,10\ {\rm{M}}\) vào ống nghiệm, dung dịch lập tức chuyển sang màu đỏ và xuất hiện kết tủa màu trắng. Lắc ống nghiệm, màu đỏ dần mất đi và kết tủa trắng tăng lên. Sau khi thử nghiệm, người ta phát hiện kết tủa màu trắng đó chính là CuSCN .
Thí nghiệm 3: Nhỏ dung dịch KSCN \(0,10{\rm{M}}\) vào ống nghiệm chứa 2 mL dung dịch \({\rm{CuS}}{{\rm{O}}_4}\ 0,1{\rm{M}}\), không thấy có kết tủa trắng xuất hiện.
Cho biết rằng CuCl và CuSCN đều là chất rắn màu trắng, ít tan trong nước. Cho các phát biểu sau:
Các phản ứng xảy ra trong thí nghiệm 1 là:
\(\mathrm{Cu}+2 \mathrm{Fe}^{3+} \longrightarrow \mathrm{Cu}^{2+}+2 \mathrm{Fe}^{2+}\)
\(\mathrm{Cu}+\mathrm{Cu}^{2+}+2 \mathrm{Cl}^{-} \longrightarrow 2 \mathrm{CuCl}\)
Dung dịch màu đỏ trong thí nghiệm 2 là do phản ứng của Fe và \({\rm{SC}}{{\rm{N}}^ - }\)tạo ra \({[{\rm{Fe}}\left( {{\rm{SCN}}} \right)]^ + }\)
Lý do tại sao màu đỏ dần phai trong thí nghiệm 2 là do \({\rm{F}}{{\rm{e}}^{3 + }}\) đã tham gia hết
Dựa trên kết quả của thí nghiệm 3 , có thể suy ra rằng kết tủa trắng trong thí nghiệm 2 không phải được tạo ra bởi phản ứng của \({\rm{C}}{{\rm{u}}^{2 + }}\) và \({\rm{SC}}{{\rm{N}}^ - }\)
Trong công nghiệp, sodium hydrogencarbonate (baking soda) và sodium carbonate (soda) được sản xuất bằng phương pháp Solvay từ nguyên liệu chính là đá vôi, muối ăn, ammonia và nước.
Quá trình Solvay sản xuất soda gồm hai giai đoạn chính:
Giai đoạn tạo \(\mathrm{NaHCO}_3: \mathrm{CO}_{2(\mathrm{aq})}+\mathrm{H}_2 \mathrm{O}_{(\mathrm{l})}+\mathrm{NH}_{3(\mathrm{aq})}+\mathrm{NaCl}_{(\mathrm{aq})} \rightleftharpoons \mathrm{NH}_4 \mathrm{Cl}_{(\mathrm{aq})}+\mathrm{NaHCO}_{3(\mathrm{~s})}\) (1)
Giai đoạn tạo \(\mathrm{Na}_2 \mathrm{CO}_3: 2 \mathrm{NaHCO}_{3(\mathrm{~s})} \longrightarrow \mathrm{Na}_2 \mathrm{CO}_{3(\mathrm{~s})}+\mathrm{CO}_{2(\mathrm{~g})}+\mathrm{H}_2 \mathrm{O}_{(\mathrm{g})}\) (2)
Cho các phát biểu sau:
Phương pháp Solvay được gọi là phương pháp tuần hoàn amonia vì phương pháp này có sự quay vòng các sản phẩm trung gian (như \({\rm{C}}{{\rm{O}}_2}\) và \({\rm{N}}{{\rm{H}}_3}\) ) để tái sử dụng trong quá trình sản xuất
Trong phản ứng ở giai đoạn (1): Nếu dùng dư \({\rm{N}}{{\rm{H}}_3}\) để cân bằng chuyển dịch sang chiều thuận, nhưng điều này lại làm giảm lượng \({\rm{C}}{{\rm{O}}_2}\) trong hệ
Phương pháp Solvay có hiệu suất phản ứng khá cao ( trung bình hiệu suất khoảng hơn 90%). Từ nguyên liệu ban đầu là \(12,395{\rm{\;}}{{\rm{m}}^3}\ {\rm{N}}{{\rm{H}}_3}\left( {{\rm{dkc}}} \right)\) và \(76,8{\rm{\;kg}}\) NaCl thu được \(62,62{\rm{\;kg}}\ {{\rm{Na}}_2}{\rm{C}}{{\rm{O}}_3}\)
Sử dụng muối KCl thay cho NaCl trong quy trình Solvay sẽ thu được \({{\rm{K}}_2}{\rm{C}}{{\rm{O}}_3}\) thay vì \({\rm{N}}{{\rm{a}}_2}{\rm{C}}{{\rm{O}}_3}\)

Bộ 50 Đề Thi Thử Tốt Nghiệp THPT Giáo Dục Kinh Tế Và Pháp Luật Năm 2026 – Theo Cấu Trúc Đề Minh Họa Bộ GD&ĐT

Bộ 50 Đề Thi Thử Tốt Nghiệp THPT Lịch Sử Học Năm 2026 – Theo Cấu Trúc Đề Minh Họa Bộ GD&ĐT

Bộ 50 Đề Thi Thử Tốt Nghiệp THPT Công Nghệ Năm 2026 – Theo Cấu Trúc Đề Minh Họa Bộ GD&ĐT

Bộ 50 Đề Thi Thử Tốt Nghiệp THPT Môn Hóa Học Năm 2026 – Theo Cấu Trúc Đề Minh Họa Bộ GD&ĐT

Bộ 50 Đề Thi Thử Tốt Nghiệp THPT Môn Sinh Học Năm 2026 – Theo Cấu Trúc Đề Minh Họa Bộ GD&ĐT

Bộ 50 Đề Thi Thử Tốt Nghiệp THPT Môn Vật Lí Năm 2026 – Theo Cấu Trúc Đề Minh Họa Bộ GD&ĐT
ĐĂNG KÝ GÓI THI VIP
- Truy cập hơn 100K đề thi thử và chính thức các năm
- 2M câu hỏi theo các mức độ: Nhận biết – Thông hiểu – Vận dụng
- Học nhanh với 10K Flashcard Tiếng Anh theo bộ sách và chủ đề
- Đầy đủ: Mầm non – Phổ thông (K12) – Đại học – Người đi làm
- Tải toàn bộ tài liệu trên TaiLieu.VN
- Loại bỏ quảng cáo để tăng khả năng tập trung ôn luyện
- Tặng 15 ngày khi đăng ký gói 3 tháng, 30 ngày với gói 6 tháng và 60 ngày với gói 12 tháng.