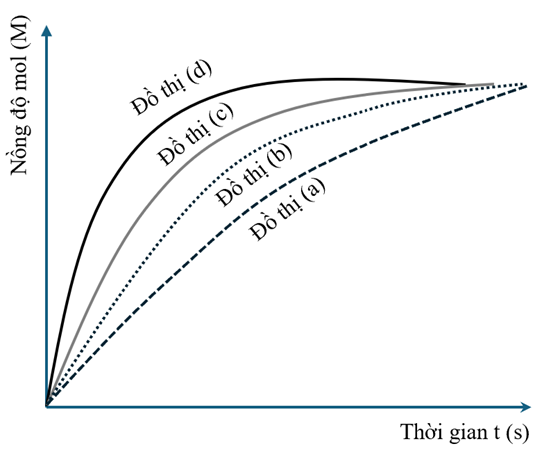
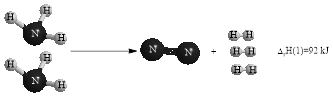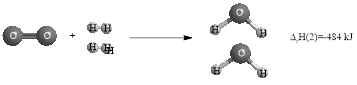Câu hỏi:
Cho các cặp oxi hoá - khử và thế điện cực chuẩn tương ứng:
|
Cặp oxi hóa – khử |
2H+/H2 |
Cu2+/Cu |
Fe2+/Fe |
Ag+/Ag |
|
Thế điện cực chuẩn (V) |
0,00 |
+0,34 |
-0,44 |
+0,799 |
Khi điện phân dung dịch chứa đồng thời bốn loại cation trên với nồng độ mol bằng nhau, cation bị điện phân đầu tiên ở cathode là
Đáp án đúng: B
Chọn B.
Câu hỏi này thuộc đề thi trắc nghiệm dưới đây, bấm vào Bắt đầu thi để làm toàn bài
Tuyển Tập Đề Thi Tham Khảo Tốt Nghiệp THPT Năm 2025 - Hóa Học - Bộ Đề 05 được biên soạn theo định hướng mới nhất của kỳ thi tốt nghiệp THPT. Mỗi đề đều có cấu trúc ba phần: trắc nghiệm nhiều lựa chọn, trắc nghiệm đúng – sai, và trắc nghiệm trả lời ngắn, kết hợp cùng hệ thống câu hỏi đa dạng, phân hóa rõ rệt theo các mức độ nhận thức từ cơ bản đến nâng cao. Điểm nổi bật của bộ đề là các câu hỏi bám sát thực tế giảng dạy, đề cập đến nhiều chủ đề quen thuộc như hợp chất hữu cơ, amino acid – protein, ester, polymer, ăn mòn kim loại, phản ứng điện hóa, cân bằng hóa học, chất điện li và môi trường. Mỗi đề đều có đáp án và hướng dẫn giải chi tiết, giúp học sinh tự ôn tập, rèn kỹ năng giải nhanh và nắm vững bản chất kiến thức. Đây là tài liệu ôn luyện lý tưởng giúp học sinh lớp 12 hệ thống hóa kiến thức toàn diện và sẵn sàng bước vào kỳ thi quan trọng với sự tự tin cao nhất.
Câu hỏi liên quan
Cho \(R\) thuộc nhóm IVA trong bảng tuần hoàn (thuộc chu kì nhỏ). Oxide cao nhất của \(R\) là một chất khí có mặt trong không khí. Trong oxide cao nhất thì phần trăm O gấp 2,622 lần phần trăm của R về khối lượng.
Cho chuỗi phản ứng sau đây:
Oxide cao nhất của \(\mathrm{R} \xrightarrow{+\mathrm{M}(\mathrm{OH})_{2}} \mathrm{MCO}_{3}\) (kết tủa màu trắng) \(\xrightarrow{+ \text { oxide cao nhất } \mathrm{R}+\mathrm{H}_{2} \mathrm{O}} \mathrm{M}\left(\mathrm{HRO}_{3}\right)_{2}\).
Cho biết kim loại M là trong hai nguyên tố có trong thành phân chính của đất đèn.
Cho các phát biểu sau:
Khối lượng nguyên tử của R là 12 amu
Hydroxide ứng với oxide cao nhất của R có dạng \(\mathrm{HRO}_{3}\) va có tính acid
Kim loại M là Barium
Hợp chất \(\mathrm{MCO}_{3}\) là thành phần chính của đá phấn
Theo đề oxide cao nhất của R dạng \(\mathrm{RO}_{2}\).
Ta có: \(\frac{M_{R}}{2 M_{0}}=\frac{\% R}{\% O} \Leftrightarrow \frac{M_{R}}{2.16}=\frac{1}{2,622} \Rightarrow M_{R}=12,2\)
Vậy R là Carbon.
a. Đúng.
b. Sai
vì hydroxide cao nhất của C là \(\mathrm{H}_{2} \mathrm{CO}_{3}\).
c. Sai
vì M là Calcium.
d. Đúng
vì \(\mathrm{CaCO}_{3}\) là thành phần chính của đá phấn.
Nhựa Y là một loại polymer có độ bền co học cao. Đặc điểm nhận dạng của nhựa Y là những sản phẩm nhựa màu trắng trong suốt, không màu, không mùi, không vị và không độc. Nhựa Y được điều chế từ hydrocarbon X.
\(X\) là một hydrocarbon mạch hở trong phân tử chỉ có liên kết đơn hoặc liên kết đôi, phương trình nhiệt hóa học của phản ứng cháy của \(X\) như sau:
\(\mathrm{C}_{n} \mathrm{H}_{2 n+2-2 \mathrm{k}}+\frac{3 n+1-\mathrm{k}}{2} \mathrm{O}_{2} \longrightarrow \mathrm{nCO}_{2}+(\mathrm{n}+1-\mathrm{k}) \mathrm{H}_{2} \mathrm{O} \quad \Delta \mathrm{H}=-1852 \mathrm{kJ}\)
Trong đó n là số nguyên tử carbon và k là số liên kết đôi \(\mathrm{C}=\mathrm{C}\) trong X.
Bảng năng lượng các liên kết như sau:
|
Liên kết |
O=O |
H-O |
C-H |
C=O |
C=C |
C-C |
|
Năng lượng liên kết (kJ/mol) |
498 |
467 |
413 |
799 |
611 |
414 |
Cho các phát biểu sau:
Trong \(X\) sẽ có một liên kết \(\pi\)
Công thức cấu tạo của X là \(\mathrm{CH}_{3}-\mathrm{CH}=\mathrm{CH}_{2}\)
Nhựa Y là nhựa PE
Nếu dùng 60 kg hydrocarbon X để thu được nhựa Y với hiệu suất \(60 \%\) thì sẽ thu được 36 kg nhựa
a. Đúng vì
Ta có:
\(\mathrm{C}_{\mathrm{n}} \mathrm{H}_{2 \mathrm{n}+2-2 \mathrm{k}} \quad+\frac{3 \mathrm{n}+1-\mathrm{k}}{2} \mathrm{O}_{2} \longrightarrow \mathrm{n} \mathrm{CO}_{2}+(\mathrm{n}+1-\mathrm{k}) \mathrm{H}_{2} \mathrm{O}\)
(n-1-k) lk C-C 1 lk O=O 2 lk C=O 2 lk H-O
k lk C=C
( \(2 \mathrm{n}+2-2 \mathrm{k}\) ) lk C-H
Bước 2. Xác định enthalpy
Theo CT tính enthalpy: \(\Delta_{\mathrm{r}} \mathrm{H}_{298}^{\rho}=\sum \mathrm{E}_{\mathrm{k} \text { thamgia }}-\sum \mathrm{E}_{\mathrm{k} \mathrm{kp}}\)
\(\Delta_{r} H_{298}^{0}=(n-1-k) E_{C-C}+k E_{C=C}+(2 n+2-2 k) E_{C-H}+\left(\frac{3 n+1-k}{2}\right) E_{O=O}-n . 2 E_{C=O}-(n+1-k) . 2 E_{O-H}\)
\(\Leftrightarrow-1852=(n-1-k) . 414+k . 611+(2 n+2-2 k) . 413+\left(\frac{3 n+1-k}{2}\right) . 498-n . 2 . 799-(n+1-k) . 2 . 467\)
\(\Leftrightarrow-1579=-545 n+56 k \Leftrightarrow k=\frac{545 n-1579}{56}\)
Theo đề cho thì \(X\) chỉ có liên kết đơn và liên kết đôi nên ta có: \(0 \leq k \leq n-1\)
\(\Leftrightarrow 0 \leq \frac{545 n-1579}{56} \leq n-1 \Rightarrow\left\{\begin{array}{l}0 \leq \frac{545 n-1579}{56} \Rightarrow 2,89 \leq n \\ \frac{545 n-1579}{56} \leq n-1 \Rightarrow n \leq 3,11\end{array} \Leftrightarrow 2,89 \leq n \leq 3,11 \Rightarrow\left\{\begin{array}{l}n=3 \\ k=1\end{array}\right.\right.\)
b. Đúng
vì theo dữ kiện giải câu a thì CTPT của X là \(\mathrm{C}_{3} \mathrm{H}_{6} \xrightarrow{\mathrm{CTCT}} \mathrm{CH}_{3}-\mathrm{CH}=\mathrm{CH}_{2}\)
c. Sai vì phương trình tạo ra Y :
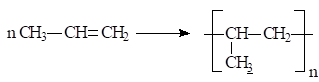
Vậy từ X người ta tổng hợp polymer tạo nhựa PP.
d. Đúng
vì theo BTKL thì khối lượng nhựa theo lý thuyết là 60 kg nhưng hiệu suất \(60 \%\) nên khối lượng nhựa thu được là \(60.60 \%=36 \mathrm{kg}\)
Các vụ hỏa hoạn ở các chung cư và nhà cao tầng hiện đang xảy ra liên tục với quy mô và mức độ tổn thất ngày càng cao. Các nạn nhân bị tử vong trong các vụ hỏa hoạn có thể do ngạt khí, bỏng nhiệt, nhảy từ trên cao xuống đất, bị vật nặng đè, giẫm đạp,... và số người chết thường không tập trung nhiều ở tâm đám cháy mà thường tập trung nhiều ở những nơi tích tụ khói hoặc có luồng khói đi qua. Khói từ đám cháy chứa các khí độc như carbon monoxide \((\mathrm{CO})\), hydrogen cyanide \((\mathrm{HCN})\) và các khí gây kích ứng khác.
Cho các phát biểu sau :
Nguyên nhân chủ yếu gây tử vong trong các vụ hỏa hoạn là khí CO vì CO sẽ liên kết với hemoglobin tạo thành HbCO , làm Hb không thể vận chuyển oxygen nên sẽ gây ngạt thở
Khi xảy ra cháy thì cần đi khom người và dùng khăn ướt bịt mũi do khói từ đám cháy sẽ bốc lên trên
Một trong những biện pháp chữa cháy thường dùng là sử dụng khí \(\mathrm{CO}_{2}\) được sinh ra từ phản ứng nhiệt phân bột rắn chứa \(\mathrm{NaHCO}_{3}\) theo phương trình: \(2 \mathrm{NaHCO}_{3} \rightarrow \mathrm{Na}_{2} \mathrm{CO}_{3}+\mathrm{CO}_{2} \uparrow+\mathrm{H}_{2} \mathrm{O}\)
Để thu được 4,958 L CO2 (đkc) thì sẽ cần 33,6 gam khối lượng bột rắn (chứa \(80 \%\ \mathrm{NaHCO}_{3}\), còn lại là chất trơ). Cho rằng phản ứng nhiệt phân xảy ra hoàn toàn
Để xác định thành phần của khí trong đám cháy, người ta đã tiến hành phân tích nhanh 7,437 lít hỗn hợp khí được thu thập từ đám cháy (coi rằng chỉ chứa \(\mathrm{N}_{2}, \mathrm{O}_{2}, \mathrm{CO}_{2}, \mathrm{CO}\) ) và tiến hành các thí nghiệm sau:
Thí nghiệm 1: Cho hỗn hợp khí qua phosphorus dư thấy khối lượng chất rắn sau phản ứng tăng 1,44 gam. Dẫn khí thoát ra qua CuO dư nung nóng, thu được 0,0192 gam Cu.
Thí nghiệm 2: Cho hỗn hợp qua dung dịch \(\mathrm{Ca}(\mathrm{OH})_{2}\) dư, thu được 0,3 gam kết tủa. Xác định thành phần \% về thể tích của mỗi khí có trong đám cháy.
Kết quả phân tích cho thấy cả khí \(\mathrm{CO}, \mathrm{CO}_{2}\) đều vượt mức nguy hiểm.
Bảng thành phần các khí như sau:
|
Chất khí |
Thành phần % về thể tích trong khí |
Tác hại với người |
|
O2 |
|
Nguy hiểm |
|
CO2 |
|
Nguy hiểm |
|
CO |
|
Nguy hiểm |
a. Đúng.
b. Đúng.
c. Sai
vì ta có: \(\mathrm{n}_{\mathrm{CO}_{2}}=\frac{4,958}{24,79}=0,2 \Rightarrow \mathrm{n}_{\mathrm{NaHCO}_{3}}=0,2.2=0,4 \mathrm{mol} \Rightarrow \mathrm{m}_{\mathrm{NaHCO}_{3}}=0.4.84=33,6 \mathrm{gam}\)
Khối lượng bột rắn là \(33,6 . \frac{100}{80}=42 \mathrm{gam}\)
d. Sai vì
Thí nghiệm 2: chỉ có khí \(\mathrm{CO}_{2}\) bị hấp thụ:
Ta có: \(\mathrm{n}_{\mathrm{CaCO}_{3}}=\frac{0,3}{100}=0,003 \mathrm{mol} \Rightarrow \mathrm{n}_{\mathrm{CO}_{2}}=0,003 \mathrm{mol}\)
Thí nghiệm 1.
Khi qua P thì O 2 phản ứng: khối lượng chất rắn tăng là \(\mathrm{mo}_{\mathrm{O}}\)
\(\Rightarrow \mathrm{m}_{\mathrm{o}}=1,44 \Rightarrow \mathrm{n}_{\mathrm{o}}=\frac{1,44}{16}=0,09 \mathrm{mol} \Rightarrow \mathrm{n}_{\mathrm{o}_{2}}=\frac{0,09}{2}=0,045 \mathrm{mol}\)
Ta có: 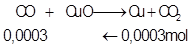
Như vậy ta có:
Theo bảng thì chỉ có \(\mathrm{CO}(1>0,066 \%)\) là nguy hiểm.
Cho cơ chế phản ứng của urea với kiềm như sau:
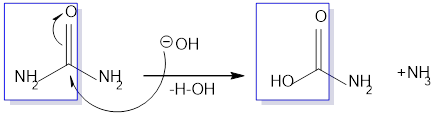
Đồng thời người ta có thể chuyển nhóm - \(\mathrm{CONH}_{2}\) thành nhóm amine bậc I bằng cách dùng \(\mathrm{Br}_{2} / \mathrm{NaOH}\) gọi là chuyển vị Hofman (đặt theo tên của nhà Hóa học A.W. Hofmann).
Từ các protein thực vật người ta tách ra được một chất Y có công thức \(\mathrm{C}_{5} \mathrm{H}_{10} \mathrm{O}_{3} \mathrm{N}_{2}\). Kết quả nghiên cứu chứng tỏ rằng \(Y\) có một nhóm amino. Đun nóng \(Y\) với kiềm thì giải phóng \(\mathrm{NH}_{3}\) đồng thời tạo thành \(\alpha\)-acid amin X (theo cơ chế như urea). Cho biết X có 1 nhóm amino, có tỷ khối so với Ne là 14,7. Thực hiện chuyển vị Hofman \(Y\) thì thu được \(\alpha, \gamma\)-diaminobutyric acid.
Cho các phát biểu sau:
Công thức cấu tạo của \(\alpha, \gamma\)-diaminobutyric acid là \(\mathrm{H}_{2} \mathrm{N}-\mathrm{CH}_{2}-\mathrm{CH}_{2}-\mathrm{CH}\left(\mathrm{NH}_{2}\right)-\mathrm{COOH}\)
Công thức phân tử của urea là \(\mathrm{CH}_{4} \mathrm{ON}_{2}\) và là phân đạm có độ dinh dưỡng cao nhất trong các phân đạm sau: \(\mathrm{NH}_{4} \mathrm{NO}_{3}\), \(\left(\mathrm{NH}_{4}\right)_{2} \mathrm{SO}_{4}\), urea, \(\mathrm{NH}_{4} \mathrm{Cl}\)
Acid X có thể làm quỳ tím ẩm hóa đỏ
Công thức cấu tạo của Y là \(\mathrm{H}_{2} \mathrm{NCO}-\mathrm{CH}_{2}-\mathrm{CH}\left(\mathrm{NH}_{2}\right)-\mathrm{COOH}\)
a. Đúng.
b. Đúng.
c. Đúng
vì theo đề CTTQ X có dạng \(\mathrm{NH}_{2}\)-R- \((\mathrm{COOH})_{2}\)
Ta có: \(14,7=\frac{M_{X}}{M_{N e}} \Leftrightarrow 14,7=\frac{M_{X}}{10} \Rightarrow M_{X}=147 \Leftrightarrow 16+M_{R}+90=147 \Rightarrow M_{R}=41\)
Vậy R là \(\mathrm{C}_{3} \mathrm{H}_{5}\). Nên CTCT của X là \(\mathrm{NH}_{2}-\mathrm{C}_{3} \mathrm{H}_{5}-(\mathrm{COOH})_{2}\) : Glutamic aicd.
d. Sai vì
Theo đề thì Y chức gốc acid \(\alpha, \gamma\)-diaminobutyric có CTCT sau:
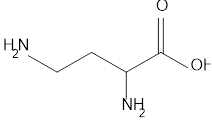
Khi đun nóng Y với kiềm thì thu \(\mathrm{C}_{3} \mathrm{H}_{5}\left(\mathrm{NH}_{2}\right)(\mathrm{COOH})_{2}\). Theo ảnh mô tả cơ thế thì sẽ biến một nhóm \(\mathrm{NH}_{2}\) gắn với CO thành OH để tạo thành nhóm COOH. Vậy suy ra Y ban đầu có 1 nhóm COOH và có 1 nhóm -CONH \({ }_{2}\)
Vậy CTCT của Y là
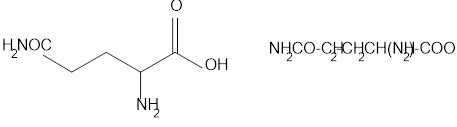
![]()
Hiệu suất chuyển hóa là \(90 \%\) nên khối lượng glucose là \(\mathrm{m}_{\text {glucose }}=\frac{850}{3} . \frac{100}{90}=314,8 \approx 315 \mathrm{gam}\).

Bộ 50 Đề Thi Thử Tốt Nghiệp THPT Giáo Dục Kinh Tế Và Pháp Luật Năm 2026 – Theo Cấu Trúc Đề Minh Họa Bộ GD&ĐT

Bộ 50 Đề Thi Thử Tốt Nghiệp THPT Lịch Sử Học Năm 2026 – Theo Cấu Trúc Đề Minh Họa Bộ GD&ĐT

Bộ 50 Đề Thi Thử Tốt Nghiệp THPT Công Nghệ Năm 2026 – Theo Cấu Trúc Đề Minh Họa Bộ GD&ĐT

Bộ 50 Đề Thi Thử Tốt Nghiệp THPT Môn Hóa Học Năm 2026 – Theo Cấu Trúc Đề Minh Họa Bộ GD&ĐT

Bộ 50 Đề Thi Thử Tốt Nghiệp THPT Môn Sinh Học Năm 2026 – Theo Cấu Trúc Đề Minh Họa Bộ GD&ĐT

Bộ 50 Đề Thi Thử Tốt Nghiệp THPT Môn Vật Lí Năm 2026 – Theo Cấu Trúc Đề Minh Họa Bộ GD&ĐT
ĐĂNG KÝ GÓI THI VIP
- Truy cập hơn 100K đề thi thử và chính thức các năm
- 2M câu hỏi theo các mức độ: Nhận biết – Thông hiểu – Vận dụng
- Học nhanh với 10K Flashcard Tiếng Anh theo bộ sách và chủ đề
- Đầy đủ: Mầm non – Phổ thông (K12) – Đại học – Người đi làm
- Tải toàn bộ tài liệu trên TaiLieu.VN
- Loại bỏ quảng cáo để tăng khả năng tập trung ôn luyện
- Tặng 15 ngày khi đăng ký gói 3 tháng, 30 ngày với gói 6 tháng và 60 ngày với gói 12 tháng.