Câu hỏi:
Nhiệt hydrate hoá là lượng nhiệt kèm theo quá trình tạo thành 1 mol muối ngậm nước từ muối khan và lượng nước tương ứng. Ví dụ, sự tạo thành dung dịch \({\rm{CuS}}{{\rm{O}}_4}\) trong n mol \({{\rm{H}}_2}{\rm{O}}\) :
Quá trình hòa tan \(\mathrm{CuSO}_4\) khan: \(\mathrm{CuSO}_{4(\mathrm{~s})}+\mathrm{nH}_2 \mathrm{O} \longrightarrow \mathrm{CuSO}_{4(\mathrm{aq})} \Delta \mathrm{H}_1\)
Quá trình hòa tan \(\mathrm{CuSO}_4 .5 \mathrm{H}_2 \mathrm{O}\) khan: \(\mathrm{CuSO}_4 .5 \mathrm{H}_2 \mathrm{O}+(n-5) \mathrm{H}_2 \mathrm{O} \longrightarrow \mathrm{CuSO}_4\) (aq) \(\Delta \mathrm{H}_2\)
Quá trình hydrate hóa: \(\mathrm{CuSO}_4{ }_{(\mathrm{s})}+5 \mathrm{H}_2 \mathrm{O} \longrightarrow \mathrm{CuSO}_4 .5 \mathrm{H}_2 \mathrm{O}_{(\mathrm{s})} \Delta \mathrm{H}_{\text {hydrate hoá }}\)
Theo định luật Hess ta có: \(\Delta \mathrm{H}_{\text {hydrate hoá }}+\Delta \mathrm{H}_2=\Delta \mathrm{H}_1 \Leftrightarrow \Delta \mathrm{H}_{\text {hydrate hoá }}=\Delta \mathrm{H}_1-\Delta \mathrm{H}_2\)
Xác định bằng thực nghiệm nhiệt hoà tan của muối khan và muối ngậm nước sẽ tính được nhiệt hydrate hoá.
Thực hiện thực nghiệm để xác định nhiệt hydrate hóa của \({\rm{CuS}}{{\rm{O}}_4}\) với các thông tin như sau:
Thí nghiệm 1: Xác định nhiệt hòa \({\rm{CuS}}{{\rm{O}}_4}\) khan.
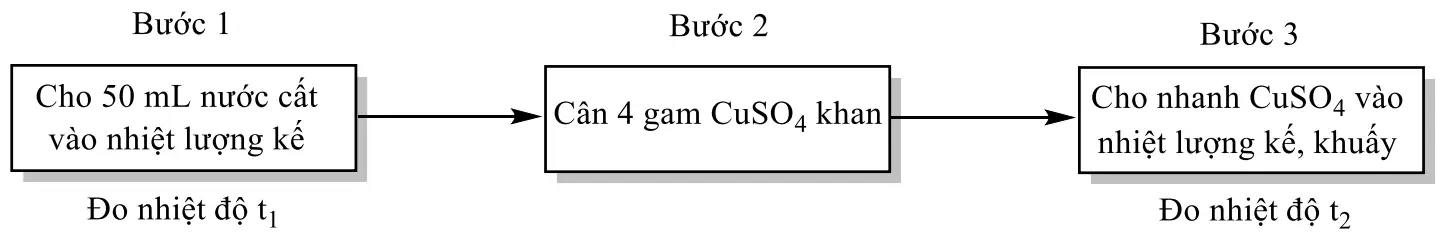
Thí nghiệm 2. Xác định nhiệt hòa \({\rm{CuS}}{{\rm{O}}_4}.5{{\rm{H}}_2}{\rm{O}}\) khan : thực hiện tương tự sơ đồ trên chỉ thay bằng 10 gam \({\rm{CuS}}{{\rm{O}}_4}.5{{\rm{H}}_2}{\rm{O}}\).
Bảng số liệu thực nghiệm đo được như sau:
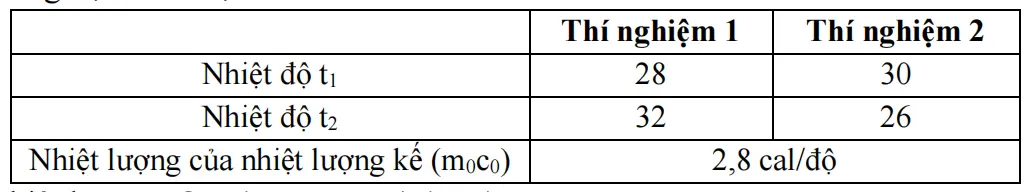
Công thức tính nhiệt lượng : \({\rm{Q}} = \left( {{{\rm{m}}_0}{{\rm{c}}_0} + {\rm{m}}.{\rm{c}}} \right) .\left( {{{\rm{t}}_2} - {{\rm{t}}_1}} \right)\)
Với \({{\rm{m}}_0}{{\rm{c}}_0}\) là nhiệt của nhiệt lượng kế.
m là khối lượng trong bình nhiệt lượng kế (gồm khối lượng chất + khối lượng nước).
c là \(1{\rm{cal}}/\) độ.
Hãy tính enthalpy hydrate hóa của \({\rm{CuS}}{{\rm{O}}_4}\) bằng đơn vị kcal/mol. (cho biết 1 cal \( = 4,184{\rm{\;J}}\) và \({\rm{\Delta H}} = - \frac{{\rm{Q}}}{{\rm{n}}}\) với n là số mol chất).(làm tròn kết quả đến hàng đơn vị)
Đáp án đúng: -15
Thí nghiệm 1:
Từ bảng số liệu ta có : \({{\rm{Q}}_1} = \left[ {2,8 + \left( {50 + 4} \right) \cdot 1} \right]\left( {32 - 28} \right) = 227,2\ {\rm{cal}} \Rightarrow {\rm{\Delta }}{{\rm{H}}_1} = - \frac{{227,2}}{{\frac{4}{{160}}}} = - 9088\ {\rm{cal}}/{\rm{mol}}\).
Thí nghiệm 2:
Từ bảng số liệu ta có : \({{\rm{Q}}_1} = \left[ {2,8 + \left( {50 + 10} \right) \cdot 1} \right]\left( {26 - 30} \right) = - 251,2\ {\rm{cal}} \Rightarrow {\rm{\Delta }}{{\rm{H}}_1} = - \frac{{219,2}}{{\frac{{10}}{{250}}}} = 6280\ {\rm{cal}}/{\rm{mol}}\).
Theo dữ kiện đề cho: \({\rm{\Delta }}{{\rm{H}}_{{\text{hydrate hoá}}}} = {\rm{\Delta }}{{\rm{H}}_1} - {\rm{\Delta }}{{\rm{H}}_2} = - 9088 - \left( {6280} \right) = - 15368\ {\rm{cal}}/{\rm{mol}} \approx - 15\ {\rm{kcal}}/{\rm{mol}}\).
Đáp án đúng là -15.
Câu hỏi này thuộc đề thi trắc nghiệm dưới đây, bấm vào Bắt đầu thi để làm toàn bài
Tuyển Tập Đề Thi Tham Khảo Tốt Nghiệp THPT Năm 2026 – Hoá Học – Bộ Đề 01Tài liệu tổng hợp các đề thi tham khảo bám sát cấu trúc đề tốt nghiệp THPT mới nhất năm 2026.Nội dung bao quát đầy đủ các chuyên đề Hoá học lớp 10, 11 và 12.Câu hỏi được phân hóa hợp lý, giúp rèn luyện kỹ năng tư duy và làm bài.Phù hợp cho học sinh ôn tập, tự đánh giá năng lực và chuẩn bị cho kỳ thi chính thức.
Câu hỏi liên quan

Bộ 50 Đề Thi Thử Tốt Nghiệp THPT Giáo Dục Kinh Tế Và Pháp Luật Năm 2026 – Theo Cấu Trúc Đề Minh Họa Bộ GD&ĐT

Bộ 50 Đề Thi Thử Tốt Nghiệp THPT Lịch Sử Học Năm 2026 – Theo Cấu Trúc Đề Minh Họa Bộ GD&ĐT

Bộ 50 Đề Thi Thử Tốt Nghiệp THPT Công Nghệ Năm 2026 – Theo Cấu Trúc Đề Minh Họa Bộ GD&ĐT

Bộ 50 Đề Thi Thử Tốt Nghiệp THPT Môn Hóa Học Năm 2026 – Theo Cấu Trúc Đề Minh Họa Bộ GD&ĐT

Bộ 50 Đề Thi Thử Tốt Nghiệp THPT Môn Sinh Học Năm 2026 – Theo Cấu Trúc Đề Minh Họa Bộ GD&ĐT